名校
解题方法
1 . 常温下,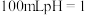 的
的 ,要使溶液的
,要使溶液的
①需要加入水___________  。
。
②需要加入 的盐酸
的盐酸___________  。需要加入
。需要加入 的
的
___________  。
。
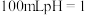 的
的 ,要使溶液的
,要使溶液的
①需要加入水
 。
。②需要加入
 的盐酸
的盐酸 。需要加入
。需要加入 的
的
 。
。
您最近半年使用:0次
解题方法
2 . 过氧化氢是淡蓝色的黏稠液体,可。与水以任意比例混溶,是一种强氧化剂。其一般以30%~60%的水溶液形式存放,水溶液俗称双氧水,适用于医用伤口消毒,环境消毒和食品消毒等。回答下列问题:
(1)实验室中利用反应2H2O2 2H2O+O2↑制取O2,可选用的发生装置是
2H2O+O2↑制取O2,可选用的发生装置是___________ (填字母,下同),收集O2可选用的装置是___________ (填字母)。___________ mL(保留三位有效数字)。
(3)过氧化氢是一种二元弱酸,写出H2O2的第一步电离方程式:___________
(4)某课外兴趣小组欲探究温度对H2O2电离平衡的影响,进行如下实验:
①实验任务:利用灵敏pH计测量溶液的pH,并探究电离过程是否吸热。
②查阅资料:20℃时,Ka1(H2O2)=2.4×10-12,lg6≈0.778。
③提出猜想:反应物浓度相同时;温度越高,酸性越强,pH越小。
④设计实验、验证猜想。取试样进行表正实验1~3,记录数据。
⑤数据分析、交流讨论。
实验结果:X2<X1<X3且X1=___________ ,测得pH数据中能证明上述猜想的是___________ (用X1、X2、X3的大小关系表示);pH出现X1<X3的原因是___________ 。
⑥优化实验。在20℃下进行下列实验:
若实验中测得△T1___________ △T2(填“>”或“<”),则说明H2O2电离过程吸热。
(1)实验室中利用反应2H2O2
 2H2O+O2↑制取O2,可选用的发生装置是
2H2O+O2↑制取O2,可选用的发生装置是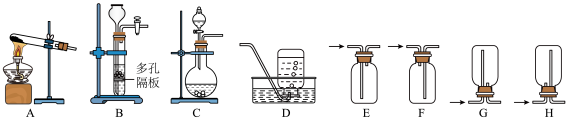
(3)过氧化氢是一种二元弱酸,写出H2O2的第一步电离方程式:
(4)某课外兴趣小组欲探究温度对H2O2电离平衡的影响,进行如下实验:
①实验任务:利用灵敏pH计测量溶液的pH,并探究电离过程是否吸热。
②查阅资料:20℃时,Ka1(H2O2)=2.4×10-12,lg6≈0.778。
③提出猜想:反应物浓度相同时;温度越高,酸性越强,pH越小。
④设计实验、验证猜想。取试样进行表正实验1~3,记录数据。
| 试祥 | 温度/℃ | pH | |
| 1 | 10mL1.5mol/L的双氧水 | 20 | X1 |
| 2 | 10mL1.5mol/L的双氧水 | 30 | X2 |
| 3 | 10mL1.5mol/L的双氧水 | 50 | X3 |
实验结果:X2<X1<X3且X1=
⑥优化实验。在20℃下进行下列实验:
| 试样 | 反应前后温度变化/℃ | |
| 4 | 10mL1.5mol/L的双氧水、10mL1.5mol/L的NaOH溶液 | △T1 |
| 5 | 10mL1.5mol/L的H2SO4溶液10mL1.5mol/L的NaOH溶液 | △T2 |
您最近半年使用:0次
3 . 常温下,分别取未知浓度的 和
和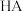 溶液,加水稀释至原体积的
溶液,加水稀释至原体积的 倍,稀释过程中,两溶液
倍,稀释过程中,两溶液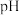 的变化如图所示。下列叙述正确的是
的变化如图所示。下列叙述正确的是

 和
和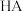 溶液,加水稀释至原体积的
溶液,加水稀释至原体积的 倍,稀释过程中,两溶液
倍,稀释过程中,两溶液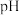 的变化如图所示。下列叙述正确的是
的变化如图所示。下列叙述正确的是
A. 为弱碱, 为弱碱,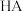 为强酸 为强酸 |
| B.将X点溶液与Z点溶液等体积混合,所得溶液呈碱性 |
C.若升高温度,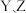 点对应溶液的 点对应溶液的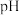 均不变 均不变 |
D.水的电离程度: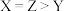 |
您最近半年使用:0次
4 . 常温下,下列关于 的
的 溶液说法正确的是
溶液说法正确的是
 的
的 溶液说法正确的是
溶液说法正确的是A.将 的 的 溶液稀释10倍,溶液的 溶液稀释10倍,溶液的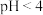 |
B.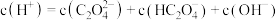 |
C.与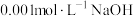 溶液等体积混合后,溶液呈碱性 溶液等体积混合后,溶液呈碱性 |
D.加水稀释时,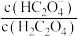 逐渐减小 逐渐减小 |
您最近半年使用:0次
解题方法
5 . 草酸 是一种白色粉末,
是一种白色粉末,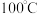 左右开始少量升华,熔点为
左右开始少量升华,熔点为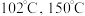 左右分解产生
左右分解产生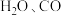 和
和 ;可与酸性
;可与酸性 溶液反应;其钠盐易溶于水,钙盐难溶于水;电离平衡常数为
溶液反应;其钠盐易溶于水,钙盐难溶于水;电离平衡常数为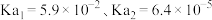 。
。
1.草酸可用于实验室制备少量 气体,应选择的发生装置为
气体,应选择的发生装置为___________ 。
常温下,向某浓度的草酸溶液中加入一定量等浓度的 溶液。
溶液。
3.当 时,溶液呈___________。
时,溶液呈___________。
A.酸性 B.碱性 C.中性 D.无法判断
此时,溶液中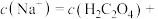
___________ 。
4.当 时,计算该溶液的
时,计算该溶液的
___________ 。(结果保留两位小数)计算过程。
 是一种白色粉末,
是一种白色粉末,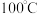 左右开始少量升华,熔点为
左右开始少量升华,熔点为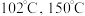 左右分解产生
左右分解产生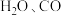 和
和 ;可与酸性
;可与酸性 溶液反应;其钠盐易溶于水,钙盐难溶于水;电离平衡常数为
溶液反应;其钠盐易溶于水,钙盐难溶于水;电离平衡常数为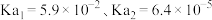 。
。1.草酸可用于实验室制备少量
 气体,应选择的发生装置为
气体,应选择的发生装置为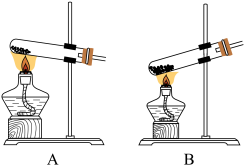
A.用足量的 溶液充分吸收后,可收集得到纯净的 溶液充分吸收后,可收集得到纯净的 |
| B.通过灼热的氧化铜,若出现黑色变红色现象,则产生的气体中一定有CO |
C.通入足量的澄清石灰水中,若能产生白色沉淀,则产生的气体中一定有 |
D.通入酸性 溶液中,若能使溶液褪色,说明草酸具有还原性 溶液中,若能使溶液褪色,说明草酸具有还原性 |
常温下,向某浓度的草酸溶液中加入一定量等浓度的
 溶液。
溶液。3.当
 时,溶液呈___________。
时,溶液呈___________。A.酸性 B.碱性 C.中性 D.无法判断
此时,溶液中
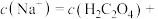
4.当
 时,计算该溶液的
时,计算该溶液的
您最近半年使用:0次
名校
解题方法
6 . 已知水在100℃时,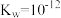 。
。
(1)在100℃,某溶液中由水电离产生的 mol/L,则该溶液的
mol/L,则该溶液的
___________ 。
(2)100℃时,若100体积 的某强酸溶液与1体积
的某强酸溶液与1体积 的某强碱溶液混合后溶液呈中性,则a与b之间应满足的关系是
的某强碱溶液混合后溶液呈中性,则a与b之间应满足的关系是___________ 。
(3)100℃时,将 的
的 溶液与
溶液与 的
的 溶液混合,若所得混合溶液的
溶液混合,若所得混合溶液的 ,则
,则 溶液与
溶液与 溶液的体积比为
溶液的体积比为___________ 。
(4)常温下,将 的
的 溶液与等物质的量浓度的
溶液与等物质的量浓度的 溶液等体积混合,所得混合液的
溶液等体积混合,所得混合液的
___________ 。
(5)已知HA的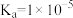 ,常温下,取
,常温下,取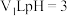 的
的 溶液与
溶液与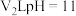 的
的 溶液混合,若混合后溶液
溶液混合,若混合后溶液 ,则大小关系:V1
,则大小关系:V1___________ V2(填“大于”“小于”或“等于”)。
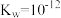 。
。(1)在100℃,某溶液中由水电离产生的
 mol/L,则该溶液的
mol/L,则该溶液的
(2)100℃时,若100体积
 的某强酸溶液与1体积
的某强酸溶液与1体积 的某强碱溶液混合后溶液呈中性,则a与b之间应满足的关系是
的某强碱溶液混合后溶液呈中性,则a与b之间应满足的关系是(3)100℃时,将
 的
的 溶液与
溶液与 的
的 溶液混合,若所得混合溶液的
溶液混合,若所得混合溶液的 ,则
,则 溶液与
溶液与 溶液的体积比为
溶液的体积比为(4)常温下,将
 的
的 溶液与等物质的量浓度的
溶液与等物质的量浓度的 溶液等体积混合,所得混合液的
溶液等体积混合,所得混合液的
(5)已知HA的
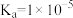 ,常温下,取
,常温下,取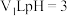 的
的 溶液与
溶液与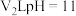 的
的 溶液混合,若混合后溶液
溶液混合,若混合后溶液 ,则大小关系:V1
,则大小关系:V1
您最近半年使用:0次
7 . 下列说法中正确的是
| A.在100℃时,pH约为6的纯水呈酸性 |
B.将1mL 盐酸稀释至1000mL,所得溶液的pH为9 盐酸稀释至1000mL,所得溶液的pH为9 |
C.在常温下,当水电离出的 为 为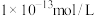 时,此溶液的pH可能为1或13 时,此溶液的pH可能为1或13 |
| D.将pH=2的盐酸和醋酸各1mL分别稀释至100mL,所得醋酸的pH略大 |
您最近半年使用:0次
名校
8 . 常温下,某 溶液的
溶液的 ,下列关于该溶液的说法中
,下列关于该溶液的说法中,不正确 的是
 溶液的
溶液的 ,下列关于该溶液的说法中
,下列关于该溶液的说法中| A.显酸性 | B.水电离出的 |
C. | D.加热, 变小 变小 |
您最近半年使用:0次
名校
9 . 25℃时,用NaOH溶液分别滴定HA(弱酸)、 、
、 三种溶液,pM[
三种溶液,pM[ ,M表示
,M表示 、
、 或
或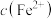 ]随pH变化关系如图所示。下列有关分析不正确的是
]随pH变化关系如图所示。下列有关分析不正确的是
已知:①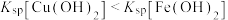 ;②溶液中离子浓度小于
;②溶液中离子浓度小于 可以认为已经除尽。
可以认为已经除尽。
 、
、 三种溶液,pM[
三种溶液,pM[ ,M表示
,M表示 、
、 或
或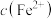 ]随pH变化关系如图所示。下列有关分析不正确的是
]随pH变化关系如图所示。下列有关分析不正确的是已知:①
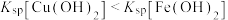 ;②溶液中离子浓度小于
;②溶液中离子浓度小于 可以认为已经除尽。
可以认为已经除尽。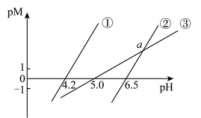
A.图中②代表滴定 溶液的变化关系 溶液的变化关系 |
B.25℃时,要除尽工业废水中的 ,需调整溶液的pH至少为6.7 ,需调整溶液的pH至少为6.7 |
| C.图中a点pH=7 |
D.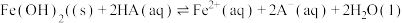 的平衡常数为 的平衡常数为 |
您最近半年使用:0次
10 . 常温下,向20mL 0.1mol/L H2S溶液中缓慢加入少量易溶于水的MSO4粉末(已知MSO4难溶,忽略溶液体积变化),溶液中c(H+)与c(M2+)变化关系如图所示。已知:Ka1(H2S)=1.0×10-9,Ka2(H2S)=1.0×10-13。下列说法错误的是
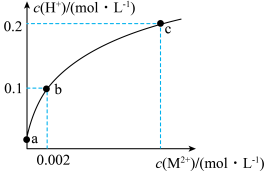
| A.a点溶液的pH约为5 | B.从a点到c点,c(HS⁻)逐渐减小 |
| C.b点溶液中,c(S2-):c(H2S)=1:1020 | D.c点溶液中,c(S2-)+c(HS⁻)+c(H2S)=0.1mol/L |
您最近半年使用:0次



