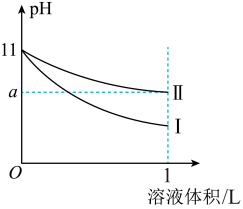
1 . 室温下,体积均为10mL、pH均为11的氨水和NaOH溶液分别加水稀释至原体积的100倍,溶液的pH随溶液体积变化的曲线如图所示。下列说法正确的是

A. |
| B.Ⅱ为NaOH溶液稀释时溶液的pH变化曲线 |
| C.完全中和1L两溶液,消耗相同浓度的稀盐酸溶液的体积:NaOH溶液<氨水 |
| D.稀释后氨水中水的电离程度比NaOH溶液中水的电离程度大 |
您最近半年使用:0次
名校
解题方法
2 . 化学与生活、工农业生产息息相关,下列说法正确的是
| A.洁厕灵和食醋是家庭中常见的两种生活用品,食醋比洁厕灵的酸性强 |
| B.增大空气的进入量,可以减少汽车尾气中由于不完全燃烧排放的氨氧化物 |
| C.在冰醋酸中加水制成食醋的过程中,pH随加水量的增大而增大 |
D.利用反应 制氢,相同时间内,使用纳米CaO(催化剂)比微米CaO产率更高 制氢,相同时间内,使用纳米CaO(催化剂)比微米CaO产率更高 |
您最近半年使用:0次
2024-01-23更新
|
153次组卷
|
2卷引用:湖北省武汉市东华中师范大学第一附属中学2023-2024学年高二上学期11月期中化学试题
名校
解题方法
3 . 在25℃和100℃时,某溶液的pH和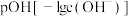 的关系如图所示。
的关系如图所示。
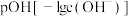 的关系如图所示。
的关系如图所示。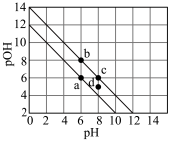
A.100℃时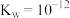 |
| B.c点对应溶液显碱性 |
| C.若将b点溶液稀释,可沿所在的线移到c点 |
| D.某温度下,d点对应的溶液可能是碱溶液或盐溶液 |
您最近半年使用:0次
2023-12-24更新
|
474次组卷
|
7卷引用:湖北省武汉市常青联合体联考2023-2024学年高二上学期1月期末考试化学试题
4 . 根据图象所得结论正确的是


A.图甲是反应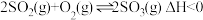 中 中 的平衡转化率随温度、压强的变化曲线,说明X代表温度,Y代表压强,且 的平衡转化率随温度、压强的变化曲线,说明X代表温度,Y代表压强,且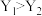 |
B.图乙是常温下用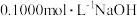 溶液滴定 溶液滴定 溶液的滴定曲线,说明Q点表示酸碱中和滴定终点 溶液的滴定曲线,说明Q点表示酸碱中和滴定终点 |
C.图丙是室温下稀释冰醋酸时溶液的导电能力随加入水的体积的变化曲线,说明醋酸的电离程度: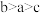 |
D.图丁是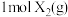 、 、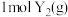 反应生成 反应生成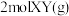 的能量变化曲线,说明反应物所含化学键的键能总和小于生成物所含化学键的键能总和 的能量变化曲线,说明反应物所含化学键的键能总和小于生成物所含化学键的键能总和 |
您最近半年使用:0次
解题方法
5 . 查阅文献数据可知:25℃时,部分常见物质的电离平衡常数如表:
回答下列问题:
(1)当三种酸的物质的量浓度相同时,c(H+)由大到小的顺序是_______ (用化学式表示,下同)。
(2)同体积、同物质的量浓度的三种酸中和NaOH溶液时所需NaOH的物质的量由大到小的顺序是_______ 。
(3)在一条件下,CH3COOH溶液中存在电离平衡:
 ,下列方法中,可以使0.10mol/LCH3COOH溶液中CH3COOH电离程度增大的是
,下列方法中,可以使0.10mol/LCH3COOH溶液中CH3COOH电离程度增大的是_______ 。
A.加入少量0.10mol/L的稀盐酸
B.加热
C.加水稀释至0.010mol/L
D.加入少量冰醋酸
E.加入少量氯化钠固体
(4)常温下,0.1mol/L的CH3COOH液加水稀释过程中,下列表达式的数据一定变小的是_______。
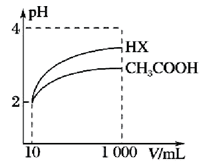
(5)体积为10mL、pH=2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程pH变化如图,则HX的电离平衡常数_______ (填“大于”“小于”或“等于”,下同)醋酸的电离平衡常数,稀释后,HX溶液中水电离出来的
_______ 醋酸溶液中水电离出来的 。
。
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.8×10-5 | K1=4.4×10-7,K2=4.7×10-11 | 3.0×10-8 |
回答下列问题:
(1)当三种酸的物质的量浓度相同时,c(H+)由大到小的顺序是
(2)同体积、同物质的量浓度的三种酸中和NaOH溶液时所需NaOH的物质的量由大到小的顺序是
(3)在一条件下,CH3COOH溶液中存在电离平衡:

 ,下列方法中,可以使0.10mol/LCH3COOH溶液中CH3COOH电离程度增大的是
,下列方法中,可以使0.10mol/LCH3COOH溶液中CH3COOH电离程度增大的是A.加入少量0.10mol/L的稀盐酸
B.加热
C.加水稀释至0.010mol/L
D.加入少量冰醋酸
E.加入少量氯化钠固体
(4)常温下,0.1mol/L的CH3COOH液加水稀释过程中,下列表达式的数据一定变小的是_______。
A. | B. | C. | D. |

 。
。
您最近半年使用:0次
解题方法
6 . 常温下,有体积均为1mL、pH均为9的烧碱溶液和氨水,下列叙述中正确的是
| A.两溶液物质的量浓度相同 |
| B.用同浓度的盐酸恰好完成中和时,消耗盐酸的体积相同 |
| C.两溶液均加水稀释到1000 mL,烧碱溶液的pH=6,氨水的pH>6 |
| D.加水稀释后若两溶液的pH仍相等,则烧碱溶液中加的水少 |
您最近半年使用:0次
2021-10-09更新
|
465次组卷
|
3卷引用:湖北省石首市2021-2022学年高二上学期期中考试化学试题
名校
7 . 取pH=11的X、Y两种碱溶液各10 mL,将其分别稀释至1000 mL,稀释过程中其pH与溶液体积(V)的关系如图所示。下列说法中,正确的是
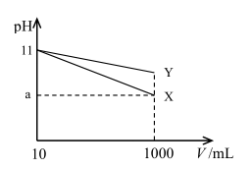
| A.稀释前,X、Y两种碱溶液的物质的量浓度一定相等 |
| B.稀释后,X溶液中c(OH- )比Y溶液中c(OH-)大 |
| C.若a>9,则X、Y都是弱碱 |
| D.用同浓度盐酸中和X、Y两溶液,完全中和时消耗的盐酸体积Vx> Vy |
您最近半年使用:0次
2021-08-01更新
|
2604次组卷
|
13卷引用:湖北省十堰市汉江中学2021-2022学年高二上学期期中考试化学试题
湖北省十堰市汉江中学2021-2022学年高二上学期期中考试化学试题2016年广东和广西高中学生化学竞赛试题(已下线)第三章 第二节水的电离和溶液的酸碱性(第2课时 溶液的pH的计算)(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版选修4)(已下线)第3章 水溶液中的离子平衡(选拔卷)-【单元测试】2021-2022学年高二化学尖子生选拔卷(人教版选修4)河北省大名县第一中学2021-2022学年高二上学期10月半月考化学试题(已下线)3.2.1 溶液的酸碱性-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)(已下线)3.2.2 溶液的pH(素养提优B练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)宁夏青铜峡市高级中学2021-2022学年高二下学期开学考试化学试题四川省资阳中学2021-2022学年高二下学期3月月考化学试题大庆市肇州县肇州中学2021-2022学年高二上学期第二次月考化学试题河北省石家庄新乐市第一中学2022-2023学年高二上学期第一次月考化学试题福建省泉州市石狮市石光中学2022-2023学年高二上学期期中考试化学试题江西省南昌十九中2023-2024学年高二上学期期中考试化学试卷
名校
解题方法
8 . 下列叙述及对应图示正确的是
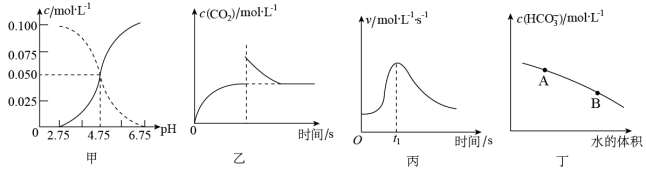

| A.图甲是某温度下c(CH3COOH)+c(CH3COO-)=0.100mol•L-1的醋酸与醋酸钠混合溶液中c(CH3COOH)、c(CH3COO-)与pH的关系曲线,pH=3的溶液中:Ka<10-4.75 |
| B.图乙是恒温密闭容器中发生CaCO3(s)=CaO(s)+CO2(g)反应时,c(CO2)随反应时间变化的曲线,t1时刻改变的条件可能是缩小容器的体积 |
| C.图丙是铁条与盐酸反应的反应速率随反应时间变化的曲线,t1时刻溶液的温度最高 |
D.图丁是在0.1mol•L-1Na2CO3溶液中加水稀释,随着加水量的增加,溶液中c(HCO )的变化曲线,则Na2CO3的水解程度A点大于B点 )的变化曲线,则Na2CO3的水解程度A点大于B点 |
您最近半年使用:0次
2021-07-01更新
|
1845次组卷
|
8卷引用:湖北省武汉市第二中学2023-2024学年高二上学期10月月考化学试题
名校
9 . 0.1 mol·L-1氨水10 mL,加蒸馏水稀释到1 L后,下列变化正确的是
①电离程度增大 ②c(NH3·H2O)增大 ③ 数目增多 ④c(OH-)增大 ⑤导电性增强 ⑥
数目增多 ④c(OH-)增大 ⑤导电性增强 ⑥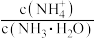 增大
增大
①电离程度增大 ②c(NH3·H2O)增大 ③
 数目增多 ④c(OH-)增大 ⑤导电性增强 ⑥
数目增多 ④c(OH-)增大 ⑤导电性增强 ⑥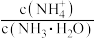 增大
增大| A.①②③ | B.①③⑤ | C.①③⑥ | D.②④⑥ |
您最近半年使用:0次
2021-06-02更新
|
2033次组卷
|
37卷引用:湖北省长阳县第一高级中学2017-2018学年高二9月月考化学试题
湖北省长阳县第一高级中学2017-2018学年高二9月月考化学试题(已下线)2014年化学高考总复习课时演练 8-1弱电解质的电离练习卷(已下线)2014高考化学专题突破训练 专题7电解质溶液练习卷黑龙江省大庆中学2018届高三上学期开学考试化学试题陕西省黄陵中学高新部2019-2020学年高二上学期期中考试化学试题云南省曲靖市宣威市第九中学2019-2020学年高二上学期第二次段考化学试题云南省曲靖市富源县第六中学2019-2020学年高二上学期期末考试化学试题沪科版化学高二拓展性课程3《化学中的平衡》测试题人教版(2019)高二化学选择性必修1第三章 水溶液中的离子反应与平衡 第一节 电离平衡 课时2 电离平衡常数黑龙江省大庆中学2020-2021学年高二上学期期中考试化学试题河北省石家庄市藁城区第一中学2019-2020学年高二上学期第二次月考化学试题安徽省合肥市第十一中学2020-2021学年高二上学期第二次月考化学试题山东省东营市胜利第二中学2020-2021学年高二上学期期中考试化学试题广西南宁市第四中学2020-2021学年高二下学期开学考试化学试题云南省丽江市第一中学2020-2021学年高二下学期期中考试化学试题云南省新平县一中2020-2021学年高二下学期期中考试化学试题选择性必修1(SJ)专题3第一单元课时2 电离平衡常数辽宁省沈阳市郊联体2021-2022学年高二上学期期中考试化学试题山东省济南市商河县第一中学2020-2021学年高二10月月考化学试题山东省临沂市兰陵县2021-2022学年高二上学期期中考试化学试题山东省临沂市兰山区、罗庄区2021-2022学年高二上学期中考试化学试题黑龙江省绥化市第一中学2021-2022学年高二上学期期中考试化学试卷云南省玉溪市第二中学2021-2022学年高二上学期期中考试化学试题云南省玉溪市江川区第二中学2021-2022学年高二上学期期中考试化学试题甘肃省永昌县第一高级中学2020-2021学年高二上学期期中考试化学(理)试题甘肃省永昌县第一高级中学2020-2021学年高二上学期期末考试化学试题山西省晋中市平遥县第二中学2021-2022学年高二上学期12月考试化学试题甘肃省民乐县第一中学2021--2022学年高二上学期期中考试化学试题(已下线)专题23 强酸(碱)与弱酸(碱)的比较-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)山西省朔州市朔城区第一中学校2021-2022学年高二下学期开学检测化学试题新疆师范大学附属中学2021-2022学年高二12月月考化学试题吉林省长春市第二实验中学2021-2022学年高二上学期10月月考化学试题甘肃省永昌县第一高级中学2021-2022学年高二上学期期末考试化学试题四川省凉山州宁南中学2022-2023学年高二上学期第二次月考化学试题黑龙江省饶河县高级中学2021-2022学年高二上学期期中考试化学试题江苏省南通市通州区金沙中学2021-2022学年高二上学期第二次调研考试化学试题安徽省怀宁县第二中学2023-2024学年高二上学期期中考试化学试题
10 . 室温下,分别向体积均为20mL、 浓度均为0.1mol·L-1的HX、HY溶液中,滴加相同浓度的Ba(OH)2溶液(Ba2+与X-、Y-均不反应)。随着Ba(OH)2溶液的加入,由水电离产生的c(H+)的变化趋势如图所示。下列说法错误的是
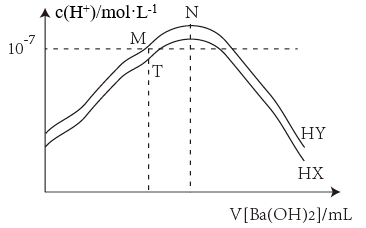

| A.相同条件下,Ka(HX)>Ka(HY) |
| B.M点溶液显中性,溶液中c(Y-)<c(Ba2+) |
| C.N点对应Ba(OH)2溶液的体积为10mL |
| D.T点溶液中阴离子浓度之和大于M点 |
您最近半年使用:0次
2021-05-31更新
|
601次组卷
|
3卷引用:湖北省鄂东南三校2022届高三下学期5月联考化学试题



