23. 我国是个钢铁大国,钢铁产量为世界第一,高炉炼铁是最为普遍的炼铁方法。
I.已知:2CO(g)+O
2(g)=2CO
2(g)
△H =-566kJ/mol
2Fe(s)+

O
2(g)=Fe
2O
3(s)
△H =-825.5 kJ/mol
则,(1)反应:Fe
2O
3(s)+3CO(g)
⇌2Fe(s)+3CO
2(g)
△H =
____________。
(2)反应

Fe
2O
3(s)+CO(g)
⇌
Fe(s)+CO
2(g)在1000℃的平衡常数等于4.0。在
一个容积为10L的密闭容器中,1000℃时加入Fe、Fe
2O
3、CO、CO
2各1.0mol,反应经过10min后达到平衡,则CO的平衡转化率=
____________。
II.高炉炼铁产生的废气中的CO可进行回收,使其在一定条件下和H
2反应制备甲醇:

。请根据图示回答下列问题:
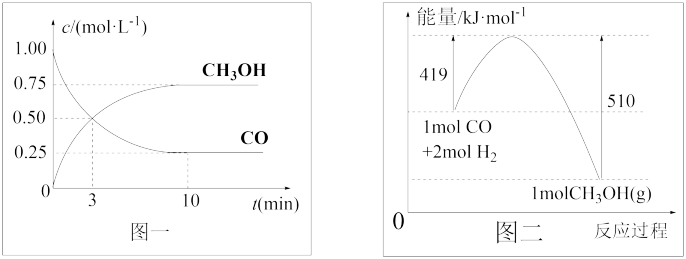
(1)从反应开始到平衡,用H
2浓度变化表示平均反应速率v(H
2)=
____________ △
△H =
____________。
(2)若在温度和容积相同的三个密闭容器中,按不同方式投入反应物,测得反应达到平衡时的有关数据如下表:
| 容器 | 反应物投入的量 | 反应物的转化率 | CH3OH的浓度 | 能量变化(Q1、Q2、Q3均大于0) |
| 甲 | 1molCO和2molH2 | a1 | c1 | 放出Q1kJ热量 |
| 乙 | 1molCH3OH | a2 | c2 | 吸收Q2kJ热量 |
| 丙 | 2molCO和4molH2 | a3 | c3 | 放出Q3kJ热量 |
则下列关系正确的是
____________。
A c
1=c
2 B.2Q
1=Q
3 C. 2a
1=a
3D. a
1 +a
2 =1 E. 该反应若生成1mol CH
3OH,则放出(Q
1+Q
2)kJ热量
(3)若在一体积可变的密闭容器中充入l molCO、 2mol H
2和1mol CH
3OH,达到平衡时测得混合气体的密度是同温同压下起始的1.6倍,则该反应向
____________ (填“正”、“逆”)反应方向移动。
III.在一个密闭容器中,有一个左右可滑动隔板,两边分别进行可逆反应,各物质的物质的量分别如下:M、N、P为2.5mol、3.0mol、1.0mol。A、C、D各为0.50mol,B的物质的量为x mol,当x在一定范围内变化,均可以通过调节反应器的温度,使两侧反应均达到平衡,且隔板在反应器的正中位置。达到平衡后,测得M的转化率为75%,填写空白:

(1)达到平衡后,反应器左室气体总的物质的量为
____________mol。
(2)若要使右室反应开始时V
正>V
逆,x的取值范围
____________。
(3)若要使右室反应开始时V
正逆,x的取值范围
____________。