33. 甲醇的研究成为当代社会的热点.
Ⅰ.甲醇燃料电池(DNFC)被认为是21世纪电动汽车最佳候选动力源.
(1)101kP 时,1mol CH
3OH完全燃烧生成稳定的氧化物放出热量726.51kJ/mol,则甲醇燃烧的热化学方程式为
__________.
(2)甲醇质子交换膜燃料电池中将甲醇蒸汽转化为氢气的两种反应原理是:
①CH
3OH(g)+H
2O(g)=CO
2(g)+3H
2(g)△H
1=+49.0kJ•mol
﹣1②CH
3OH(g)+

O
2(g)=CO
2(g)+2H
2(g)△H
2已知H
2(g)+

O
2(g)=H
2O(g)△H=﹣241.8kJ•mol
﹣1则反应②的△H
2=
__________.
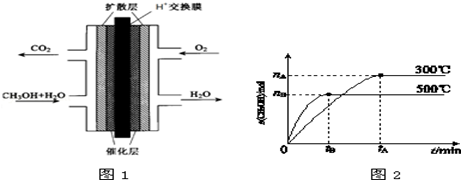
(3)甲醇燃料电池的结构示意图如图1.负极发生的电极反应为
____________________.
Ⅱ.一定条件下,在体积为3L的密闭容器中反应CO(g)+2H
2(g)⇌CH
3OH(g)达到化学平衡状态.
(1)根据图2,纵坐标为CH
3OH的物质的量,升高温度,K值将
__________(填“增大”、“减小”或“不变”).
(2)500℃时,从反应开始到达到化学平衡,以H
2的浓度变化表示的化学反应速率是
__________(用n
B、t
B表示).
(3)判断该可逆反应达到化学平衡状态的标志是
__________(填字母).
a.CO、H
2、CH
3OH的浓度均不再变化
b.混合气体的密度不再改变
c.混合气体的平均相对分子质量不再改变
d.v
生成(CH
3OH)=v
消耗(CO)
e.混合气中n(CO):n(H
2):n(CH
3OH)=1:2:1
(4)300℃时,将容器的容积压缩到原来的

,在其他条件不变的情况下,对平衡体系产生的影响是
__________(填字母).
a.c(H
2)减少 b.正反应速率加快,逆反应速率减慢
c.CH
3OH 的物质的量增加 d.重新平衡时

减小.