26. 在容积为1.00L的容器中,通入一定量的N
2O
4,发生反应N
2O
4(g)

2NO
2(g),随温度升高,混合气体的颜色变深。
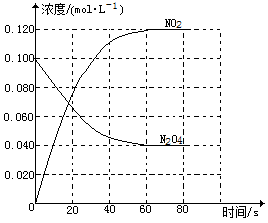
回答下列问题:
(1)反应的
△H___0(填“大于”“小于”);100℃时,体系中各物质浓度随时间变化如图所示。在0~60s时段,反应速率
v(N
2O
4)为
___mol·L
-1·s
-1,反应的平衡常数
K1为
___。
(2)100℃时达到平衡后,改变反应温度为T,
c(N
2O
4)以0.0020mol·L
-1·s
-1的平均速率降低,经10s又达到平衡。
a:T
___100℃(填“大于”“小于”),判断理由是
___。
b:列式计算温度T时反应的平衡常数
K2=
___。
(3)温度T时反应达平衡后,将反应容器的容积减少一半,平衡向(填“正反应”或“逆反应”)
___方向移动,判断理由是
___。
(4)D为含有足量AgCl固体的饱和溶液,AgCl在水中存在沉淀溶解平衡:AgCl(s)

Ag
+(aq)+Cl
-(aq),在25℃时,
Ksp(AgCl)=1.8×10
-10。现将足量氯化银分别放入:①100mL蒸馏水中;②100mL0.2mol/LAgNO
3溶液中;③100mL0.1mol/L氯化铝溶液中;④100mL0.1mol/L盐酸中,充分搅拌后,相同温度下
c(Ag
+)由大到小的顺序是
___(填写序号);②中氯离子的浓度为
__mol/L。