27. 某同学设计实验以探究元素性质的递变规律,实验装置如图所示。
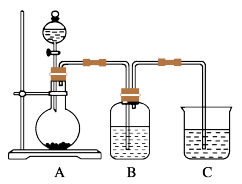
实验Ⅰ:根据元素最高价含氧酸的酸性强弱探究元素非金属性递变规律。已知A装置的烧瓶里装有大理石,分液漏斗里装有稀HNO
3,B装置中装有饱和碳酸氢钠溶液,装置C中装有Na
2SiO
3溶液,试回答:
(1)A中反应的离子方程式为
___________,C中可观察到的现象是
___________(2)B装置的作用是
___________(3)根据实验现象推知,碳酸、硝酸、硅酸的酸性强弱顺序是
___________,由此得出碳、硅、氮三种元素非金属性的强弱顺序是
___________实验Ⅱ:已知常温下高锰酸钾与浓盐酸混合可产生氯气,利用该装置探究氯和溴元素的非金属性强弱。
(4)写出B装置中发生反应的离子方程式:
___________(5)C装置的作用是
___________(6)实验结论:氧化性
___________,非金属性:
___________