18. I.下表是元素周期表的一部分, 回答下列问题:
(1)d、e、f对应简单离子的半径由大到小的顺序为
_______(用具体微粒符号表示)。
(2)元素i的单质溶于水,生成一种具有漂白作用的化合物,该化合物的电子式为
_____;写出a与c形成的一种含18电子且既含极性键又含非极性键的化合物的分子式
_________。
(3)以元素a的单质为燃料,以f的最高价氧化物对应的水化物为电解质溶液,请写出该燃料电池的负极反应方程式
_________。
II. (1)如图是甲烷燃料电池原理示意图,回答下列问题:
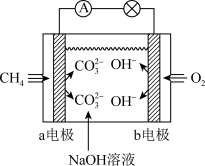
①电池的负极是
_____(填“a”或“b”)电极,该极的电极反应式为
_____。
②电池工作一段时间后电解质溶液的pH
______(填“增大”“减小”或“不变”)。
(2)熔融盐燃料电池具有很高的发电效率,因而受到重视。可用碳酸锂和碳酸钠的熔融盐混合物作电解质,一氧化碳为负极燃气,空气与二氧化碳的混合气为正极助燃气,制得在650 ℃下工作的燃料电池,其负极反应式为2CO+2CO

-4e
-=4CO
2。
①正极反应式是
_____;
②总电池反应式是
______。