名校
1 . 氮气和氧气反应生成一氧化氮的能量变化如图所示,下列说法正确的是
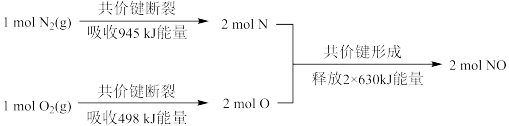
A. 是大气污染物之一,在空气中能稳定存在 是大气污染物之一,在空气中能稳定存在 |
B.该反应生成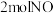 时,应吸收 时,应吸收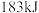 能量 能量 |
C. 氮原子结合生成 氮原子结合生成 时需吸收 时需吸收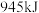 能量 能量 |
D.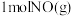 分子中的化学键断裂时吸收 分子中的化学键断裂时吸收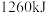 能量 能量 |
您最近半年使用:0次
名校
2 . 低碳经济已成为人们一种新的生活理念,二氧化碳的捕捉和利用是能源领域的一个重要研究方向。回答下列问题:
(1)用 催化加氢可以制取乙烯:
催化加氢可以制取乙烯: ,该反应体系的能量随反应过程变化关系如图所示,则该反应的
,该反应体系的能量随反应过程变化关系如图所示,则该反应的
_______ (用含a、b的式子表示)。相关化学键的键能如下表,实验测得上述反应的 ,则表中反应过程的x=
,则表中反应过程的x=_______ 。
(2)工业上用 和
和 反应合成二甲醚。
反应合成二甲醚。



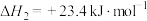
则

_______  。
。
(3)用 表示阿伏加德罗常数的值,在
表示阿伏加德罗常数的值,在 (g)完全燃烧生成
(g)完全燃烧生成 和液态水的反应中,每有5
和液态水的反应中,每有5 个电子转移时,放出650kJ的热量。则
个电子转移时,放出650kJ的热量。则 (g)的燃烧热为
(g)的燃烧热为_______ 。
(4)一定条件下,在水溶液中1mol 、1mol
、1mol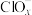 (
( 、2、3、4)的相对能量(kJ)大小如图所示:
、2、3、4)的相对能量(kJ)大小如图所示:_______ (用离子符号表示)。
(1)用
 催化加氢可以制取乙烯:
催化加氢可以制取乙烯: ,该反应体系的能量随反应过程变化关系如图所示,则该反应的
,该反应体系的能量随反应过程变化关系如图所示,则该反应的
 ,则表中反应过程的x=
,则表中反应过程的x=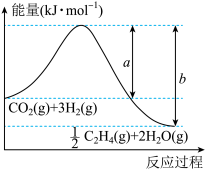
| 化学键 | C=O | H—H | C=C | C—H | H—O |
键能( ) ) | x | 436 | 764 | 414 | 464 |
(2)工业上用
 和
和 反应合成二甲醚。
反应合成二甲醚。


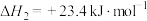
则


 。
。(3)用
 表示阿伏加德罗常数的值,在
表示阿伏加德罗常数的值,在 (g)完全燃烧生成
(g)完全燃烧生成 和液态水的反应中,每有5
和液态水的反应中,每有5 个电子转移时,放出650kJ的热量。则
个电子转移时,放出650kJ的热量。则 (g)的燃烧热为
(g)的燃烧热为(4)一定条件下,在水溶液中1mol
 、1mol
、1mol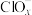 (
( 、2、3、4)的相对能量(kJ)大小如图所示:
、2、3、4)的相对能量(kJ)大小如图所示: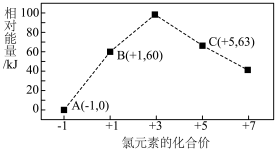
您最近半年使用:0次
3 .  在光照条件下与
在光照条件下与 反应,可得到各种氯代甲烷。取一支硬质大试管,通过排饱和食盐水的方法先后收集半试管甲烷和半试管氯气,并置于光亮处(如图)。回答下列问题:
反应,可得到各种氯代甲烷。取一支硬质大试管,通过排饱和食盐水的方法先后收集半试管甲烷和半试管氯气,并置于光亮处(如图)。回答下列问题:
(2)生成 的化学方程式为
的化学方程式为___________ 。
(3) 氯代的机理为自由基(带有单电子的原子或原子团,如
氯代的机理为自由基(带有单电子的原子或原子团,如 、
、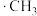 )反应,包括以下几步:
)反应,包括以下几步:
①写出由 生成
生成 过程中链传递的方程式:
过程中链传递的方程式: 、
、___________ 。
②已知:25℃、 时,
时, 中
中 键和
键和 中
中 键的键能分别是
键的键能分别是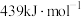 和
和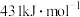 。则反应
。则反应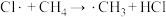 完全反应
完全反应___________ (填“放出”或“吸收”)热量。
(4)丙烷氯代反应中链传递的一步反应能量变化如图。___________ (填序号)。
①其一氯取代物不存在同分异构体 ②其二氯取代物不存在同分异构体
 在光照条件下与
在光照条件下与 反应,可得到各种氯代甲烷。取一支硬质大试管,通过排饱和食盐水的方法先后收集半试管甲烷和半试管氯气,并置于光亮处(如图)。回答下列问题:
反应,可得到各种氯代甲烷。取一支硬质大试管,通过排饱和食盐水的方法先后收集半试管甲烷和半试管氯气,并置于光亮处(如图)。回答下列问题: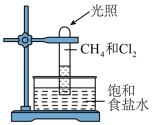
| A.反应过程中试管内黄绿色逐渐变浅,试管壁上有油珠产生 |
B.将该装置放在黑暗处, 与 与 也能反应 也能反应 |
| C.该实验发生了取代反应 |
D. 和 和 完全反应后试管内液面上升,液体充满试管 完全反应后试管内液面上升,液体充满试管 |
 的化学方程式为
的化学方程式为(3)
 氯代的机理为自由基(带有单电子的原子或原子团,如
氯代的机理为自由基(带有单电子的原子或原子团,如 、
、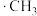 )反应,包括以下几步:
)反应,包括以下几步:| Ⅰ.链引发 | Ⅱ.链传递 | Ⅲ.链终止 |
 | 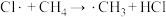 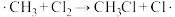 … |   … |
 生成
生成 过程中链传递的方程式:
过程中链传递的方程式: 、
、②已知:25℃、
 时,
时, 中
中 键和
键和 中
中 键的键能分别是
键的键能分别是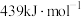 和
和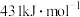 。则反应
。则反应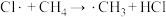 完全反应
完全反应(4)丙烷氯代反应中链传递的一步反应能量变化如图。
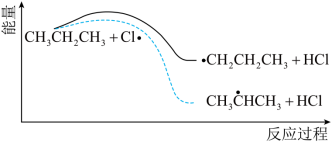
分析上图可知, 中
中 键能比
键能比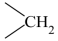 中
中 键能
键能
①其一氯取代物不存在同分异构体 ②其二氯取代物不存在同分异构体
您最近半年使用:0次
名校
4 . 有机化合物的组成、结构、性质及转化是学习有机化学的必备知识。
Ⅰ. 与
与 混合在光照条件下发生反应生成多种氯代烃。
混合在光照条件下发生反应生成多种氯代烃。
(1)写出生成具有正四面体构型的有机产物的结构式:______ 。
(2)写出反应生成 的化学方程式:
的化学方程式:______ ,其反应类型是______
(3) 与
与 反应生成
反应生成 的反应过程、中间态物质的能量关系如图所示(
的反应过程、中间态物质的能量关系如图所示( 、
、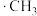 表示带有单电子的原子或原子团)。
表示带有单电子的原子或原子团)。 是由
是由 在光照下化学键断裂生成的,该过程
在光照下化学键断裂生成的,该过程______ (填“放出”或“收”)能量。
②该反应过程可能会生成一种副产物烃,该烃的结构简式为______ 。
Ⅱ.丙烯(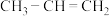 )在一定条件下有如图所示的转化关系,根据图示完成下列问题。
)在一定条件下有如图所示的转化关系,根据图示完成下列问题。 的
的 溶液反应生成A的化学方程式为
溶液反应生成A的化学方程式为____________ ,该反应类型是______ 。
(5)写出B所有可能的结构简式:______ 。
(6)C的一氯代物有______ 种。
Ⅰ.
 与
与 混合在光照条件下发生反应生成多种氯代烃。
混合在光照条件下发生反应生成多种氯代烃。(1)写出生成具有正四面体构型的有机产物的结构式:
(2)写出反应生成
 的化学方程式:
的化学方程式:(3)
 与
与 反应生成
反应生成 的反应过程、中间态物质的能量关系如图所示(
的反应过程、中间态物质的能量关系如图所示( 、
、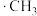 表示带有单电子的原子或原子团)。
表示带有单电子的原子或原子团)。
 是由
是由 在光照下化学键断裂生成的,该过程
在光照下化学键断裂生成的,该过程②该反应过程可能会生成一种副产物烃,该烃的结构简式为
Ⅱ.丙烯(
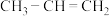 )在一定条件下有如图所示的转化关系,根据图示完成下列问题。
)在一定条件下有如图所示的转化关系,根据图示完成下列问题。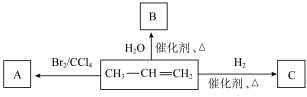
 的
的 溶液反应生成A的化学方程式为
溶液反应生成A的化学方程式为(5)写出B所有可能的结构简式:
(6)C的一氯代物有
您最近半年使用:0次
5 . 电喷雾电离得到的 (
(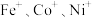 等)与
等)与 反应可得
反应可得 。
。 分别与
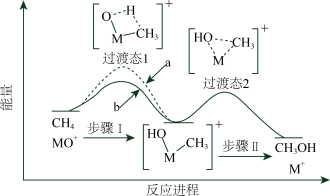
分别与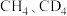 反应制备甲醇,体系的能量随反应进程的变化如下图所示(两者历程相似,图中以
反应制备甲醇,体系的能量随反应进程的变化如下图所示(两者历程相似,图中以 示例)。已知:直接参与化学键变化的元素被替换为更重的同位素时,反应速率会变慢。下列说法正确的是
示例)。已知:直接参与化学键变化的元素被替换为更重的同位素时,反应速率会变慢。下列说法正确的是
 (
(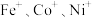 等)与
等)与 反应可得
反应可得 。
。 分别与
分别与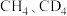 反应制备甲醇,体系的能量随反应进程的变化如下图所示(两者历程相似,图中以
反应制备甲醇,体系的能量随反应进程的变化如下图所示(两者历程相似,图中以 示例)。已知:直接参与化学键变化的元素被替换为更重的同位素时,反应速率会变慢。下列说法正确的是
示例)。已知:直接参与化学键变化的元素被替换为更重的同位素时,反应速率会变慢。下列说法正确的是
| A.步骤Ⅰ和Ⅱ中均涉及氢原子成键变化 |
B. 与 与 反应的能量变化为图中曲线 反应的能量变化为图中曲线 |
C. 与 与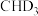 反应,生成的氘代甲醇有三种 反应,生成的氘代甲醇有三种 |
D. 与 与 反应,生成的氘代甲醇: 反应,生成的氘代甲醇: |
您最近半年使用:0次
名校
解题方法
6 . NH3催化还原NO是重要的烟气脱硝技术,其反应过程与能量关系如图;研究发现在以Fe2O3为主的催化剂上可能发生的反应过程如图。下列说法正确的是

| A.NH3催化还原NO为吸热反应 |
| B.过程I中NH3断裂N—H键 |
| C.过程Ⅱ中NO为氧化剂,Fe2+为还原剂 |
| D.脱硝的总反应为:4NH3(g)+4NO(g)+2O2(g)⇌4N2(g)+6H2O(g) |
您最近半年使用:0次
名校
解题方法
7 . 根据下面的信息,下列叙述正确的是
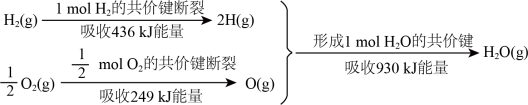
A. 跟 跟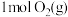 反应生成 反应生成 放出能量为 放出能量为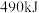 |
| B.化学反应中能量变化的大小与反应物的质量多少无关 |
C.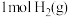 跟 跟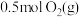 反应生成 反应生成 释放能量为 释放能量为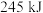 |
D. 的能量比 的能量比 与 与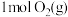 的能量之和低 的能量之和低 |
您最近半年使用:0次
8 . 化学反应过程中都伴随能量变化,吸热或放热是化学反应中能量变化的重要形式。回答下列问题:
(1)化学反应中伴随热量变化的本质原因是反应过程中形成化学键___________ ,断裂化学键___________ 。
(2)已知拆开1mol H—H键、1mol Cl—Cl键、1mol H—Cl键分别需要的能量是436kJ、243kJ、432kJ,则反应 的
的 =
=___________  。
。
(3)已知:
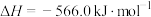 ;
;
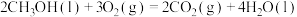
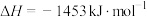 。
。
则 (l)不完全燃烧生成CO和
(l)不完全燃烧生成CO和 (l)的热化学方程式为
(l)的热化学方程式为___________ 。
(4)已知常温常压下,稀的强酸与稀的强碱溶液生成1mol (l)的反应热
(l)的反应热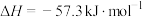 。
。
①表示稀硫酸与稀烧碱溶液生成1mol (l)的热化学方程式为
(l)的热化学方程式为___________ 。
②若用98%浓硫酸代替稀硫酸与稀烧碱溶液进行中和反应反应热测定,则所测得的
___________ (填“偏大”或“偏小”)。
(1)化学反应中伴随热量变化的本质原因是反应过程中形成化学键
(2)已知拆开1mol H—H键、1mol Cl—Cl键、1mol H—Cl键分别需要的能量是436kJ、243kJ、432kJ,则反应
 的
的 =
= 。
。(3)已知:

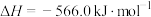 ;
;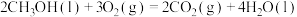
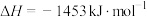 。
。则
 (l)不完全燃烧生成CO和
(l)不完全燃烧生成CO和 (l)的热化学方程式为
(l)的热化学方程式为(4)已知常温常压下,稀的强酸与稀的强碱溶液生成1mol
 (l)的反应热
(l)的反应热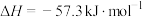 。
。①表示稀硫酸与稀烧碱溶液生成1mol
 (l)的热化学方程式为
(l)的热化学方程式为②若用98%浓硫酸代替稀硫酸与稀烧碱溶液进行中和反应反应热测定,则所测得的

您最近半年使用:0次
名校
解题方法
9 . 合成氨的热化学方程式为
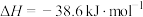 ,下列有关叙述错误的是
,下列有关叙述错误的是

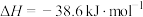 ,下列有关叙述错误的是
,下列有关叙述错误的是| A.反应物的总能量大于生成物的总能量 |
B.生成1mol  (g)时放出19.3kJ的热量 (g)时放出19.3kJ的热量 |
| C.形成化学键放出的总能量大于断裂化学键吸收的总能量 |
D.将1mol  (g)与3mol (g)与3mol  (g)置于密闭容器中充分反应后放出热量为38.6kJ (g)置于密闭容器中充分反应后放出热量为38.6kJ |
您最近半年使用:0次
解题方法
10 . 舍勒发现氯气是在1774年,当他使软锰矿与浓盐酸混合并加热时,产生了一种黄绿色的气体,发生的反应为MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O,这种气体有强烈的刺激性气味。舍勒制备出氯气以后,把它溶解在水里,发现这种水溶液对纸张、蔬菜和花都具有永久性的漂白作用;他还发现氯气能与金属、非金属、碱等发生化学反应。氢气在氯气中燃烧为放热反应,下列说法正确的是
MnCl2+Cl2↑+2H2O,这种气体有强烈的刺激性气味。舍勒制备出氯气以后,把它溶解在水里,发现这种水溶液对纸张、蔬菜和花都具有永久性的漂白作用;他还发现氯气能与金属、非金属、碱等发生化学反应。氢气在氯气中燃烧为放热反应,下列说法正确的是
 MnCl2+Cl2↑+2H2O,这种气体有强烈的刺激性气味。舍勒制备出氯气以后,把它溶解在水里,发现这种水溶液对纸张、蔬菜和花都具有永久性的漂白作用;他还发现氯气能与金属、非金属、碱等发生化学反应。氢气在氯气中燃烧为放热反应,下列说法正确的是
MnCl2+Cl2↑+2H2O,这种气体有强烈的刺激性气味。舍勒制备出氯气以后,把它溶解在水里,发现这种水溶液对纸张、蔬菜和花都具有永久性的漂白作用;他还发现氯气能与金属、非金属、碱等发生化学反应。氢气在氯气中燃烧为放热反应,下列说法正确的是| A.断开Cl-Cl键放出能量 | B.形成H-Cl键吸收能量 |
| C.燃烧都是放热反应 | D.反应物的总能量小于生成物的总能量 |
您最近半年使用:0次



