名校
解题方法
1 . 合成氨的热化学方程式为
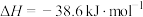 ,下列有关叙述错误的是
,下列有关叙述错误的是

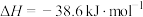 ,下列有关叙述错误的是
,下列有关叙述错误的是| A.反应物的总能量大于生成物的总能量 |
B.生成1mol  (g)时放出19.3kJ的热量 (g)时放出19.3kJ的热量 |
| C.形成化学键放出的总能量大于断裂化学键吸收的总能量 |
D.将1mol  (g)与3mol (g)与3mol  (g)置于密闭容器中充分反应后放出热量为38.6kJ (g)置于密闭容器中充分反应后放出热量为38.6kJ |
您最近半年使用:0次
2 . 深入研究碳、氮元素的物质转化有着重要的实际意义,按要求回答下列问题:
(1)CO用于处理大气污染物N2O的反应为CO(g)+N2O(g)⇌CO2(g)+N2(g)。在Zn+作用下该反应的具体过程如图1所示,反应过程中能量变化情况如图2所示。
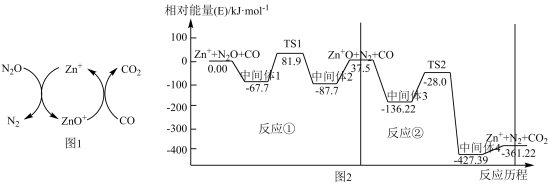
总反应:CO(g)+N2O(g)⇌CO2(g)+N2(g) △H=_______ kJ•mol-1;该总反应的决速步是反应______ (填“①”或“②”)。
(2)已知:CO(g)+N2O(g) CO2(g)+N2(g)的速率方程为v=k•c(N2O),k为速率常数,只与温度有关。为提高反应速率,可采取的措施是_______(填字母序号)。
CO2(g)+N2(g)的速率方程为v=k•c(N2O),k为速率常数,只与温度有关。为提高反应速率,可采取的措施是_______(填字母序号)。
(3)在催化剂作用下,以CO2和H2为原料合成CH3OH,主要反应为:
反应I:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) △H1=-49kJ•mol-1
反应Ⅱ:CO2(g)+H2(g)=CO(g)+H2O(g) △H2=+4kJ•mol-1
保持压强3MPa,将起始n(CO2):n(H2)=1:3的混合气体匀速通过装有催化剂的反应管,测得出口处CO2的转化率和甲醇的选择性[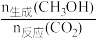 ×100%]与温度的关系如题图3、题图4所示。
×100%]与温度的关系如题图3、题图4所示。

①在T℃下,恒压反应器中,若按初始投料n(CO2):n(H2)=1:1只发生反应I,初始总压为2MPa,反应平衡后,H2的平衡转化率为60%,则该反应的平衡常数Kp=______ (MPa)-2(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
②随着温度的升高,CO2转化率增大、但甲醇选择性降低的原因是______ 。
③假设定义催化剂催化效率η ×100%,计算340℃时三种催化剂的催化效率之比η(In2O3):η(Mg/In2O3):η(Mn/In2O3)=
×100%,计算340℃时三种催化剂的催化效率之比η(In2O3):η(Mg/In2O3):η(Mn/In2O3)=_______ 。
(4)一种基于铜基金属簇催化剂电催化还原CO2制备甲醇的装置如图5所示。控制其他条件相同,将一定量的CO2通入该电催化装置中,阴极所得产物及其物质的量与电压的关系如图6所示。

①b电极生成CH3OH的电极反应式为______ 。
②控制电压为0.8V,电解时转移电子的物质的量为______ mol。
(1)CO用于处理大气污染物N2O的反应为CO(g)+N2O(g)⇌CO2(g)+N2(g)。在Zn+作用下该反应的具体过程如图1所示,反应过程中能量变化情况如图2所示。

总反应:CO(g)+N2O(g)⇌CO2(g)+N2(g) △H=
(2)已知:CO(g)+N2O(g)
 CO2(g)+N2(g)的速率方程为v=k•c(N2O),k为速率常数,只与温度有关。为提高反应速率,可采取的措施是_______(填字母序号)。
CO2(g)+N2(g)的速率方程为v=k•c(N2O),k为速率常数,只与温度有关。为提高反应速率,可采取的措施是_______(填字母序号)。| A.升温 | B.恒容时,再充入CO |
| C.恒容时,再充入N2O | D.恒压时,再充入N2 |
反应I:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) △H1=-49kJ•mol-1
反应Ⅱ:CO2(g)+H2(g)=CO(g)+H2O(g) △H2=+4kJ•mol-1
保持压强3MPa,将起始n(CO2):n(H2)=1:3的混合气体匀速通过装有催化剂的反应管,测得出口处CO2的转化率和甲醇的选择性[
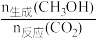 ×100%]与温度的关系如题图3、题图4所示。
×100%]与温度的关系如题图3、题图4所示。
①在T℃下,恒压反应器中,若按初始投料n(CO2):n(H2)=1:1只发生反应I,初始总压为2MPa,反应平衡后,H2的平衡转化率为60%,则该反应的平衡常数Kp=
②随着温度的升高,CO2转化率增大、但甲醇选择性降低的原因是
③假设定义催化剂催化效率η
 ×100%,计算340℃时三种催化剂的催化效率之比η(In2O3):η(Mg/In2O3):η(Mn/In2O3)=
×100%,计算340℃时三种催化剂的催化效率之比η(In2O3):η(Mg/In2O3):η(Mn/In2O3)=(4)一种基于铜基金属簇催化剂电催化还原CO2制备甲醇的装置如图5所示。控制其他条件相同,将一定量的CO2通入该电催化装置中,阴极所得产物及其物质的量与电压的关系如图6所示。

①b电极生成CH3OH的电极反应式为
②控制电压为0.8V,电解时转移电子的物质的量为
您最近半年使用:0次
3 . 已知2H2(g)+O2(g)=2H2O(l) ΔΔH=-571.6kJ/mol,则2H2O(l)= 2H2(g)+O2(g) ΔH=
| A.-571.6KJ/mol | B.+571.6KJ/mol |
| C.-285.8KJ/mol | D.+285.8KJ/mol |
您最近半年使用:0次
4 . 一定条件下,可逆反应
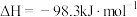 。下列有关叙述错误的是
。下列有关叙述错误的是

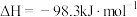 。下列有关叙述错误的是
。下列有关叙述错误的是A.相同条件下, 和 和 反应生成2mol 反应生成2mol ,放出的热量为 ,放出的热量为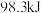 |
B.恒容条件下,向平衡体系中通入一定量 , , 的平衡转化率减小 的平衡转化率减小 |
C.恒压条件下,向平衡体系中通入一定量 ,平衡不移动 ,平衡不移动 |
D.及时分离出 ,平衡正向移动,平衡常数不变 ,平衡正向移动,平衡常数不变 |
您最近半年使用:0次
名校
5 . 下列有关说法正确的是
A.常温下,向 溶液中加入少量盐酸,溶液中 溶液中加入少量盐酸,溶液中 的值增大 的值增大 |
B.反应 常温下能自发进行,则该反应的 常温下能自发进行,则该反应的 |
C.一定条件下, 碘蒸气和 碘蒸气和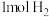 充分混合反应生成HI并放热 充分混合反应生成HI并放热 ,则该反应的热化学方程式为: ,则该反应的热化学方程式为: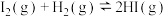 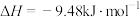 |
D.同温同压下, 在光照和点燃条件下的 在光照和点燃条件下的 不同 不同 |
您最近半年使用:0次
名校
解题方法
6 .  为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.常温下, 的 的 溶液中由水电离出的 溶液中由水电离出的 数为 数为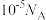 |
B.标准状况下将22.4 L  溶于水配成1 mol/L的溶液,则 溶于水配成1 mol/L的溶液,则 mol/L mol/L |
C.电解 溶液,阴极生成2.24 L气体(标况),外电路中通过电子的数目为 溶液,阴极生成2.24 L气体(标况),外电路中通过电子的数目为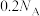 |
D. 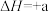 kJ⋅mol kJ⋅mol ,若参加反应的 ,若参加反应的 数目为 数目为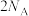 ,反应会吸收a kJ热量 ,反应会吸收a kJ热量 |
您最近半年使用:0次
名校
7 . 羰基硫是一种粮食熏蒸剂,能防治某些害虫和真菌的危害。一定条件下, 与CO能反应生成羰基硫:
与CO能反应生成羰基硫:
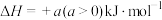 ,设
,设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 与CO能反应生成羰基硫:
与CO能反应生成羰基硫:
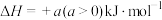 ,设
,设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.每转移 个 个 ,吸收akJ能量 ,吸收akJ能量 |
B. 溶液中含有的 溶液中含有的 数目为 数目为 |
C.1mol COS中含有的双键数目为 |
D.1mol CO与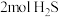 充分反应可生成COS分子的数目为 充分反应可生成COS分子的数目为 |
您最近半年使用:0次
2024-01-11更新
|
126次组卷
|
2卷引用:河南省创新发展联盟2023-2024学年高二上学期第四次联考化学试题
名校
8 . 完成下列问题
(1)如图中,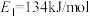 ,
,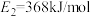 ,根据要求回答问题:
,根据要求回答问题:
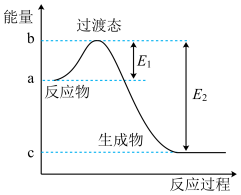
如图是1mol NO2和1molCO反应生成CO2和NO过程中的能量变化示意图,若在反应体系中加入催化剂,反应速率增大, 的变化是
的变化是___________ (填“增大”“减小”或“不变”),请写出NO2和CO反应的热化学方程式:___________ 。
(2)在某温度下,将H2和I2各1mol的气态混合物充入10L的密闭容器中发生反应H2(g)+I2(g) 2HI(g) ΔH<0,达到平衡后,测得c(H2)=0.08mol/L。
2HI(g) ΔH<0,达到平衡后,测得c(H2)=0.08mol/L。
 保持容器容积不变,向其中再加入1molH2,反应速率
保持容器容积不变,向其中再加入1molH2,反应速率___________ (填“增大”、“减小”或“不变”),平衡___________ 移动(填“向正反应方向”、“向逆反应方向”或“不”)。
②保持容器内气体压强不变,向其中加入1molN2(N2不参加反应),反应速率___________ (填“增大”、“减小”或“不变”),平衡___________ 移动(填“向正反应方向”、“向逆反应方向”或“不”)。
③该反应的化学平衡常数K=___________ 。
(1)如图中,
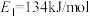 ,
,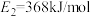 ,根据要求回答问题:
,根据要求回答问题:
如图是1mol NO2和1molCO反应生成CO2和NO过程中的能量变化示意图,若在反应体系中加入催化剂,反应速率增大,
 的变化是
的变化是(2)在某温度下,将H2和I2各1mol的气态混合物充入10L的密闭容器中发生反应H2(g)+I2(g)
 2HI(g) ΔH<0,达到平衡后,测得c(H2)=0.08mol/L。
2HI(g) ΔH<0,达到平衡后,测得c(H2)=0.08mol/L。 保持容器容积不变,向其中再加入1molH2,反应速率
保持容器容积不变,向其中再加入1molH2,反应速率②保持容器内气体压强不变,向其中加入1molN2(N2不参加反应),反应速率
③该反应的化学平衡常数K=
您最近半年使用:0次
名校
解题方法
9 . 下列说法中正确的是
| A.热化学方程式未注明温度和压强时,∆H表示标准状况下的数据 |
| B.热化学方程式中各物质前的化学计量数不表示分子个数,只代表物质的量 |
| C.钙钛矿太阳能电池和锂离子电池的工作原理相同 |
| D.非自发反应在任何条件下都不能发生 |
您最近半年使用:0次
10 . 现有如下3个热化学方程式:
H2(g)+ O2(g)=H2O(g) ΔH1=-akJ/mo ①
O2(g)=H2O(g) ΔH1=-akJ/mo ①
H2(g)+ O2(g)=H2O(l) ΔH2=-bkJ/mol ②
O2(g)=H2O(l) ΔH2=-bkJ/mol ②
2H2(g)+O2(g)=2H2O(l) ΔH3=-ckJ/mol ③
则由下表所列的原因能推导出后面结论的是
H2(g)+
 O2(g)=H2O(g) ΔH1=-akJ/mo ①
O2(g)=H2O(g) ΔH1=-akJ/mo ①H2(g)+
 O2(g)=H2O(l) ΔH2=-bkJ/mol ②
O2(g)=H2O(l) ΔH2=-bkJ/mol ②2H2(g)+O2(g)=2H2O(l) ΔH3=-ckJ/mol ③
则由下表所列的原因能推导出后面结论的是
| 选项 | 原因 | 结论 |
| A | H2的燃烧是放热反应 | a、b、c均大于0 |
| B | ①和②中物质的化学计量数均相同 | a=b |
| C | ③中H2O的状态不同,化学计最数不同 | a、b、c不会有任何等量或不等量关系 |
| D | ③的化学计量数是②的2倍 | ΔH2<ΔH1 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次



