1 . 已知反应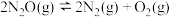 的势能曲线示意图如下(…表示吸附作用,A表示催化剂,
的势能曲线示意图如下(…表示吸附作用,A表示催化剂, 表示过渡态分子):
表示过渡态分子):
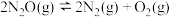 的势能曲线示意图如下(…表示吸附作用,A表示催化剂,
的势能曲线示意图如下(…表示吸附作用,A表示催化剂, 表示过渡态分子):
表示过渡态分子):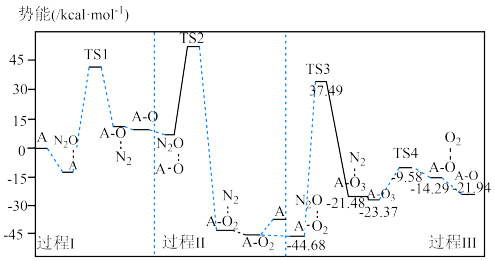
A.过程Ⅰ、Ⅱ、Ⅲ中都有 生成 生成 |
| B.若在任意温度下均能自发进行,则反应为吸热反应 |
C.该反应中只有两种物质能够吸附 分子 分子 |
D.过程Ⅲ中最大势能垒(活化能)为 |
您最近半年使用:0次
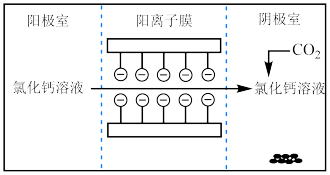
2 . I.电解法可处理氯化钙废液同时,吸收CO2,装置如图所示。_______ 和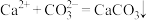 。
。
II.工业含硫烟气污染大气,研究烟气脱硫具有重要意义。
方法一、H2还原脱硫:
(2)300℃,发生反应:①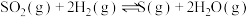

②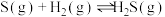

③

请用一个等式来表示三个反应的 之间的关系
之间的关系_______ 。
(3)反应③,在恒温、恒容的密闭容器中,充入 和
和 ,平衡常数
,平衡常数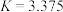 ,测得平衡时
,测得平衡时 和
和 的浓度均为
的浓度均为 ,则平衡时
,则平衡时 的值为
的值为_______ 。
方法二、O2氧化脱硫:
(4)某同学探究活性炭吸附催化氧化 ,以N2作稀释剂,一定温度下,通入
,以N2作稀释剂,一定温度下,通入 、
、 和
和 反应生成
反应生成 ,其中不同温度下,
,其中不同温度下, 在活性炭上的吸附情况如图,下列说法正确的是_______。
在活性炭上的吸附情况如图,下列说法正确的是_______。
(5)在SO2与O2反应过程中掺入少量CH4有利于提高SO2转化成SO3,其中一种解释是甲烷参与氧化反应过程中存在如图机理。原料以一定流速通过反应容器,出口处测SO3的含量,结合机理说明甲烷体积分数增大,SO3体积分数也增大的理由_______ 。
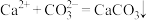 。
。II.工业含硫烟气污染大气,研究烟气脱硫具有重要意义。
方法一、H2还原脱硫:
(2)300℃,发生反应:①
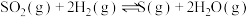

②
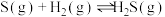

③


请用一个等式来表示三个反应的
 之间的关系
之间的关系(3)反应③,在恒温、恒容的密闭容器中,充入
 和
和 ,平衡常数
,平衡常数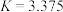 ,测得平衡时
,测得平衡时 和
和 的浓度均为
的浓度均为 ,则平衡时
,则平衡时 的值为
的值为方法二、O2氧化脱硫:
(4)某同学探究活性炭吸附催化氧化
 ,以N2作稀释剂,一定温度下,通入
,以N2作稀释剂,一定温度下,通入 、
、 和
和 反应生成
反应生成 ,其中不同温度下,
,其中不同温度下, 在活性炭上的吸附情况如图,下列说法正确的是_______。
在活性炭上的吸附情况如图,下列说法正确的是_______。
| A.温度越低,SO2的吸附量越高,SO2氧化反应速率越快 |
| B.已知:SO2的物理吸附过程能自发进行,可推断该过程是熵减、放热的过程,温度过高不利 |
| C.原料中水蒸气的含量越大,脱硫速率一定越快 |
D.随着时间的推移,SO2吸附速率降低,可能是由于生成的 占据了吸附位点没及时脱出导致 占据了吸附位点没及时脱出导致 |
(5)在SO2与O2反应过程中掺入少量CH4有利于提高SO2转化成SO3,其中一种解释是甲烷参与氧化反应过程中存在如图机理。原料以一定流速通过反应容器,出口处测SO3的含量,结合机理说明甲烷体积分数增大,SO3体积分数也增大的理由

您最近半年使用:0次
7日内更新
|
123次组卷
|
2卷引用:浙江绍兴市2023-2024学年高三下学期选考科目适应性考试化学试题
名校
3 . 哈伯法合成氨技术是德国诺贝尔化学奖获得者哈伯发明的。其合成原理为:N2(g)+3H2(g) 2NH3(g)
2NH3(g)  H<0,
H<0, S<0。下列有关工业合成氨的说法正确的是
S<0。下列有关工业合成氨的说法正确的是
 2NH3(g)
2NH3(g)  H<0,
H<0, S<0。下列有关工业合成氨的说法正确的是
S<0。下列有关工业合成氨的说法正确的是A.因为 H<0,所以该反应一定能自发进行 H<0,所以该反应一定能自发进行 |
B.因为 S<0,所以该反应一定不能自发进行 S<0,所以该反应一定不能自发进行 |
| C.在低温下进行是为了提高反应物的转化率 |
| D.使用催化剂加快反应速率是因为催化剂降低了反应的活化能 |
您最近半年使用:0次
名校
4 . 工业上以CO2和NH3为原料合成尿素,在尿素合成塔中的主要反应可表示如下:
反应Ⅰ:2NH3(g)+CO2(g) H2NCOONH4(s)(氨基甲酸铵) ΔH1=-272kJ·mol -1
H2NCOONH4(s)(氨基甲酸铵) ΔH1=-272kJ·mol -1
反应Ⅱ:H2NCOONH4(s) CO(NH2)2(s)+H2O(g) ΔH2=+138kJ·mol-1;
CO(NH2)2(s)+H2O(g) ΔH2=+138kJ·mol-1;
总反应Ⅲ:2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g) ∆H3
CO(NH2)2(s)+H2O(g) ∆H3
(1)反应Ⅰ的熵变ΔS___________  填“
填“ ”“
”“ ”或“
”或“ ”
” 。反应Ⅲ的
。反应Ⅲ的 H3=
H3=___________ ,反应Ⅲ自发进行的条件是___________ (填“低温”、“高温”、“任何温度”)。
(2)下列关于尿素合成的说法正确的是___________。
(3)1mol CO(NH2)2(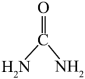 )中含有
)中含有___________ molπ键。NH 离子的VSEPR模型是
离子的VSEPR模型是___________ ,空间构型是___________ 。
(4)对于尿素分子中N、O两种基态原子,下列说法正确的是___________。
反应Ⅰ:2NH3(g)+CO2(g)
 H2NCOONH4(s)(氨基甲酸铵) ΔH1=-272kJ·mol -1
H2NCOONH4(s)(氨基甲酸铵) ΔH1=-272kJ·mol -1反应Ⅱ:H2NCOONH4(s)
 CO(NH2)2(s)+H2O(g) ΔH2=+138kJ·mol-1;
CO(NH2)2(s)+H2O(g) ΔH2=+138kJ·mol-1;总反应Ⅲ:2NH3(g)+CO2(g)
 CO(NH2)2(s)+H2O(g) ∆H3
CO(NH2)2(s)+H2O(g) ∆H3(1)反应Ⅰ的熵变ΔS
 填“
填“ ”“
”“ ”或“
”或“ ”
” 。反应Ⅲ的
。反应Ⅲ的 H3=
H3=(2)下列关于尿素合成的说法正确的是___________。
| A.及时分离出尿素可促使反应Ⅱ向正反应方向移动 |
| B.从合成塔出来的混合气体分离出水蒸气后其余气体可以循环使用 |
| C.保持容积不变,充入惰性气体增大压强,可提高总反应Ⅲ的反应速率 |
| D.保持压强不变,降低氨碳比[n(NH3)/n(CO2)]可提高反应Ⅰ中NH3的平衡转化率 |
 )中含有
)中含有 离子的VSEPR模型是
离子的VSEPR模型是(4)对于尿素分子中N、O两种基态原子,下列说法正确的是___________。
| A.N的半径较小 | B.N的未成对电子数较多 |
| C.N的电负性较大 | D.N的第一电离能较高 |
您最近半年使用:0次
名校
解题方法
5 . 已知“凡气体分子总数增加的反应都是熵增大的反应”。下列反应在任何温度下都不自发进行的是
A.2O3(g)=3O2(g)  H<0 H<0 |
B.2CO(g)=2C(s)+O2(g)  H>0 H>0 |
C.N2(g)+3H2(g)=2NH3(g)  H<0 H<0 |
D.CaCO3(s)=CaO(s)+CO2(g)  H>0 H>0 |
您最近半年使用:0次
2024-04-21更新
|
21次组卷
|
2卷引用:江苏省徐州市沛县湖西中学2023-2024学年高二下学期第一次调研考试化学试题
2024高三下·全国·专题练习
6 . 钛(Ti)及其合金是理想的高强度、低密度结构材料。以钛渣(主要成分为 ,含少量V、Si和Al的氧化物杂质)为原料,制备金属钛的工艺流程如下:
,含少量V、Si和Al的氧化物杂质)为原料,制备金属钛的工艺流程如下: 中含有的几种物质的沸点:
中含有的几种物质的沸点:
回答下列问题:
(1)已知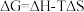 ,
, 的值只决定于反应体系的始态和终态,忽略
的值只决定于反应体系的始态和终态,忽略 、
、 随温度的变化。若
随温度的变化。若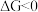 ,则该反应可以自发进行。根据下图判断:
,则该反应可以自发进行。根据下图判断: 时,下列反应不能自发进行的是_______。
时,下列反应不能自发进行的是_______。
(2) 与C、
与C、 ,在
,在 的沸腾炉中充分反应后,混合气体中各组分的分压如下表:
的沸腾炉中充分反应后,混合气体中各组分的分压如下表:
①该温度下, 与C、
与C、 反应的总化学方程式为
反应的总化学方程式为_______ ;
②随着温度升高,尾气中 的含量升高,原因是
的含量升高,原因是_______ 。
 ,含少量V、Si和Al的氧化物杂质)为原料,制备金属钛的工艺流程如下:
,含少量V、Si和Al的氧化物杂质)为原料,制备金属钛的工艺流程如下: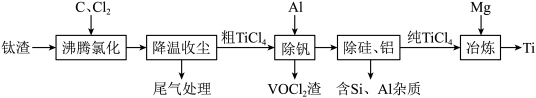
 中含有的几种物质的沸点:
中含有的几种物质的沸点:| 物质 |  |  |  |  |
沸点/ | 136 | 127 | 57 | 180 |
(1)已知
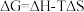 ,
, 的值只决定于反应体系的始态和终态,忽略
的值只决定于反应体系的始态和终态,忽略 、
、 随温度的变化。若
随温度的变化。若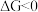 ,则该反应可以自发进行。根据下图判断:
,则该反应可以自发进行。根据下图判断: 时,下列反应不能自发进行的是_______。
时,下列反应不能自发进行的是_______。
A. | B. |
C. | D. |
(2)
 与C、
与C、 ,在
,在 的沸腾炉中充分反应后,混合气体中各组分的分压如下表:
的沸腾炉中充分反应后,混合气体中各组分的分压如下表:| 物质 |  |  |  |  |
分压 | 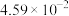 | 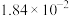 |  |  |
 与C、
与C、 反应的总化学方程式为
反应的总化学方程式为②随着温度升高,尾气中
 的含量升高,原因是
的含量升高,原因是
您最近半年使用:0次
7 . 二氧化碳催化加氢制取清洁燃料甲醇的反应为: 。在一密闭容器中,按起始
。在一密闭容器中,按起始 通入反应物,250℃时
通入反应物,250℃时 (甲醇在平衡体系中的物质的量分数)随压强变化的曲线和
(甲醇在平衡体系中的物质的量分数)随压强变化的曲线和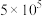 Pa时
Pa时 随温度变化的曲线如图所示。下列说法正确的是
随温度变化的曲线如图所示。下列说法正确的是
 。在一密闭容器中,按起始
。在一密闭容器中,按起始 通入反应物,250℃时
通入反应物,250℃时 (甲醇在平衡体系中的物质的量分数)随压强变化的曲线和
(甲醇在平衡体系中的物质的量分数)随压强变化的曲线和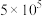 Pa时
Pa时 随温度变化的曲线如图所示。下列说法正确的是
随温度变化的曲线如图所示。下列说法正确的是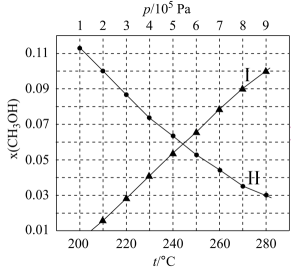
A.Ⅰ表示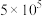 Pa时 Pa时 随温度变化的曲线 随温度变化的曲线 |
| B.该反应在较高温度下才能自发进行 |
C.250℃、 Pa达平衡时, Pa达平衡时,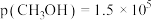 Pa Pa |
D.当 时, 时, 的平衡转化率为40% 的平衡转化率为40% |
您最近半年使用:0次
解题方法
8 . 二氯乙烷为原料制备氯乙烯是合成氯乙烯的一种重要的方法。请回答:
(1)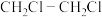 热裂解反应为:
热裂解反应为: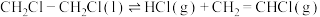

已知相关物质的标准熵数值如下表:
①该反应的标准熵变
___________ 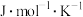 ;
;
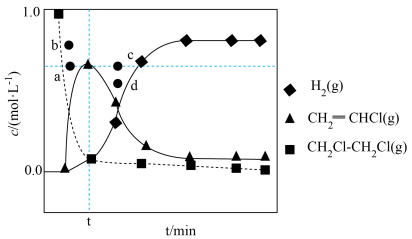
②已知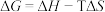 ,该反应在下列哪些温度下能自发进行?
,该反应在下列哪些温度下能自发进行?________ (填标号);
A.0.39K B.0.49K C.500K D.525K
(2)密闭恒容容器中充满1.0mol/L CH2Cl-CH2Cl(g),保持温度773K,只发生以下反应。
反应Ⅰ: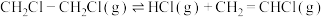

反应Ⅱ:
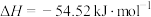
研究发现,反应Ⅰ活化能远小于反应Ⅱ,近似认为反应Ⅰ建立平衡后始终处于平衡状态。未加入催化剂下进行反应,各物质的浓度与反应时间的变化关系如图所示,t时刻测得CH2=CHCl、H2的浓度分别为0.80 mol/L、0.10 mol/L。___________ mol/L。
②其他条件不变,若反应温度高于773K且保持不变,则图示点a、b中,CH2=CHCl的浓度峰值点可能是________ (填标号)。
③相同条件下,若反应起始时加入足量的氮掺杂活性炭催化剂(该催化剂仅对反应Ⅰ有加速作用),则图示点a、b、c、d中,CH2=CHCl的浓度峰值点可能是________ (填标号),解释原因____________ 。
(3)现投入CH≡CH与CH2Cl-CH2Cl于密闭恒容中,可能发生的反应如下:
反应Ⅰ: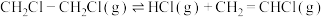

反应Ⅱ: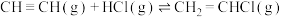
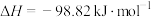
反应Ⅲ:
若用氮掺杂活性炭作催化剂,只发生反应Ⅰ和Ⅱ;若用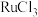 和
和 作催化剂,只发生反应Ⅲ。不考虑催化剂活性降低或丧失,下列说法不正确的是 。
作催化剂,只发生反应Ⅲ。不考虑催化剂活性降低或丧失,下列说法不正确的是 。
(1)
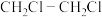 热裂解反应为:
热裂解反应为: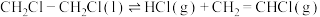

已知相关物质的标准熵数值如下表:
化学式 |
| HCl(g) |
|
标准熵:S/( | 305.90 | 186.90 | 264.00 |

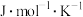 ;
;②已知
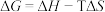 ,该反应在下列哪些温度下能自发进行?
,该反应在下列哪些温度下能自发进行?A.0.39K B.0.49K C.500K D.525K
(2)密闭恒容容器中充满1.0mol/L CH2Cl-CH2Cl(g),保持温度773K,只发生以下反应。
反应Ⅰ:
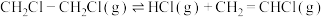

反应Ⅱ:

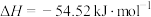
研究发现,反应Ⅰ活化能远小于反应Ⅱ,近似认为反应Ⅰ建立平衡后始终处于平衡状态。未加入催化剂下进行反应,各物质的浓度与反应时间的变化关系如图所示,t时刻测得CH2=CHCl、H2的浓度分别为0.80 mol/L、0.10 mol/L。
②其他条件不变,若反应温度高于773K且保持不变,则图示点a、b中,CH2=CHCl的浓度峰值点可能是
③相同条件下,若反应起始时加入足量的氮掺杂活性炭催化剂(该催化剂仅对反应Ⅰ有加速作用),则图示点a、b、c、d中,CH2=CHCl的浓度峰值点可能是
(3)现投入CH≡CH与CH2Cl-CH2Cl于密闭恒容中,可能发生的反应如下:
反应Ⅰ:
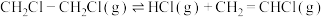

反应Ⅱ:
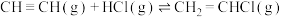
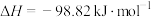
反应Ⅲ:

若用氮掺杂活性炭作催化剂,只发生反应Ⅰ和Ⅱ;若用
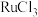 和
和 作催化剂,只发生反应Ⅲ。不考虑催化剂活性降低或丧失,下列说法不正确的是 。
作催化剂,只发生反应Ⅲ。不考虑催化剂活性降低或丧失,下列说法不正确的是 。| A.温度升高,反应Ⅲ的平衡常数K增大 |
| B.其他条件不变,氮掺杂活性炭作催化剂,HCl平衡浓度随温度升高而增大 |
C.其他条件不变,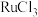 和 和 作催化剂,减少容器体积对 作催化剂,减少容器体积对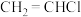 平衡产率不影响 平衡产率不影响 |
D.其他条件不变,CH2Cl-CH2Cl的平衡转化率大小比较:氮掺杂活性炭作催化剂>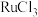 和 和 作催化剂 作催化剂 |
您最近半年使用:0次
解题方法
9 . 黑火药爆炸发生反应为: ,下列说法不正确的是
,下列说法不正确的是
 ,下列说法不正确的是
,下列说法不正确的是| A.该反应任意温度下自发 | B.S和 氧化剂,C是还原剂 氧化剂,C是还原剂 |
C. 和 和 是氧化产物 是氧化产物 | D.生成1mol  转移12mol电子 转移12mol电子 |
您最近半年使用:0次
解题方法
10 . 下列内容与结论相对应的是
| 选项 | 内容 | 结论 |
| A |  | 该过程的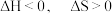 |
| B | 常温下,硝酸铵固体溶于水可自发进行 | 该过程的 |
| C | 一个反应的 | 反应一定不能自发进行 |
| D |  能自发进行 能自发进行 | 则该反应的 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次



