1 . 下列过程属于吸热反应的是
| A.浓硫酸溶于水 | B.硝酸铵溶于水 |
| C.碳酸氢钠溶于盐酸 | D.铁粉溶于盐酸 |
您最近半年使用:0次
名校
解题方法
2 . 研究化学能与热能、电能的转化具有重要价值。回答下列问题:
(1)下列化学反应过程中的能量变化符合图示的是___________ (填序号)。
⑤灼热的碳与二氧化碳反应 ⑥ 与
与 反应
反应
(2) 的反应过程如图所示:
的反应过程如图所示: (g)和1mol
(g)和1mol  (g)充分反应,该反应为
(g)充分反应,该反应为___________ (填“吸热”或“放热”)反应。
(3)依据NaOH与HCl的反应原理设计原电池,你认为是否合理?___________ (填“是”或“否”),理由是___________ 。
(4)利用反应 设计一个原电池(正极材料用碳棒),回答下列问题:
设计一个原电池(正极材料用碳棒),回答下列问题:
①电池的负极材料是___________ ,负极电极反应式为___________ ,电解质溶液是___________ 。
②正极上出现的现象是___________ 。
③若导线上转移1mol电子时,则电解质溶液改变的质量为___________ g。
(1)下列化学反应过程中的能量变化符合图示的是
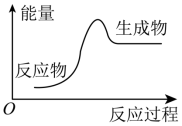
⑤灼热的碳与二氧化碳反应 ⑥
 与
与 反应
反应(2)
 的反应过程如图所示:
的反应过程如图所示: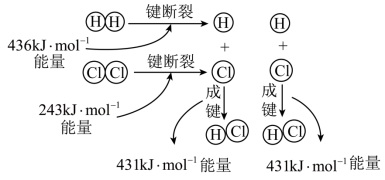
 (g)和1mol
(g)和1mol  (g)充分反应,该反应为
(g)充分反应,该反应为(3)依据NaOH与HCl的反应原理设计原电池,你认为是否合理?
(4)利用反应
 设计一个原电池(正极材料用碳棒),回答下列问题:
设计一个原电池(正极材料用碳棒),回答下列问题:①电池的负极材料是
②正极上出现的现象是
③若导线上转移1mol电子时,则电解质溶液改变的质量为
您最近半年使用:0次
名校
解题方法
3 . 人类活动离不开能量,能量的利用与化学反应中能量变化密切相关。
Ⅰ.某小组研究氨氮废水的处理(氮元素主要为 和
和 ),实验流程如图。
),实验流程如图。 溶液,调节
溶液,调节 至9后,升温至
至9后,升温至 ,再通空气将氨赶出并回收。用离子方程式表示加
,再通空气将氨赶出并回收。用离子方程式表示加 溶液的作用:
溶液的作用:_______ 。
(2)过程Ⅱ:在微生物作用下, 经过两步反应被氧化成
经过两步反应被氧化成 。能量变化示意图如图:
。能量变化示意图如图:_____ 反应(选填“放热”或“吸热”)。
② 全部被氧化成
全部被氧化成 的热离子方程式是
的热离子方程式是_______ 。
Ⅱ.某小组研究 片与稀硫酸反应中的能量变化,进行实验。
片与稀硫酸反应中的能量变化,进行实验。
(3)实验Ⅰ:将 片和
片和 片分别插入2个盛有
片分别插入2个盛有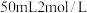 稀硫酸的烧杯中。观察到
稀硫酸的烧杯中。观察到 片表面产生气泡,溶液温度由
片表面产生气泡,溶液温度由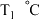 升到
升到 片表面无明显变化,溶液温度无变化。
片表面无明显变化,溶液温度无变化。 片与稀硫酸反应的能量变化关系符合图
片与稀硫酸反应的能量变化关系符合图______ (填“A”或“B”)。 片、
片、 片相连接,插入盛有
片相连接,插入盛有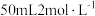 稀硫酸的烧杯中(如图
稀硫酸的烧杯中(如图 所示)。
所示)。 片表面产生气泡,溶液温度由
片表面产生气泡,溶液温度由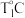 升到
升到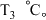
②结合电子的移动方向,解释 片表面产生气泡的原因:该原电池中
片表面产生气泡的原因:该原电池中 失电子,
失电子,_______ 。
(5)实验Ⅰ和Ⅱ产生等量气体时,测得 。结合能量的转化形式,分析两溶液温度变化幅度
。结合能量的转化形式,分析两溶液温度变化幅度不同 的原因______ 。
(6)将 片和
片和 片换成
片换成 片和石墨棒,重复实验Ⅱ,请判断电流表指针是否发生偏转。若不偏转,说明理由;若偏转,写出
片和石墨棒,重复实验Ⅱ,请判断电流表指针是否发生偏转。若不偏转,说明理由;若偏转,写出 片表面发生的电极反应式。理由或电极反应式是
片表面发生的电极反应式。理由或电极反应式是______ 。
Ⅰ.某小组研究氨氮废水的处理(氮元素主要为
 和
和 ),实验流程如图。
),实验流程如图。
 溶液,调节
溶液,调节 至9后,升温至
至9后,升温至 ,再通空气将氨赶出并回收。用离子方程式表示加
,再通空气将氨赶出并回收。用离子方程式表示加 溶液的作用:
溶液的作用:(2)过程Ⅱ:在微生物作用下,
 经过两步反应被氧化成
经过两步反应被氧化成 。能量变化示意图如图:
。能量变化示意图如图: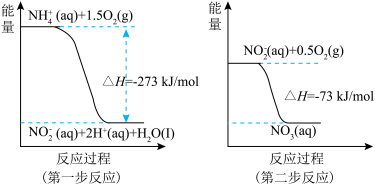
②
 全部被氧化成
全部被氧化成 的热离子方程式是
的热离子方程式是Ⅱ.某小组研究
 片与稀硫酸反应中的能量变化,进行实验。
片与稀硫酸反应中的能量变化,进行实验。(3)实验Ⅰ:将
 片和
片和 片分别插入2个盛有
片分别插入2个盛有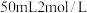 稀硫酸的烧杯中。观察到
稀硫酸的烧杯中。观察到 片表面产生气泡,溶液温度由
片表面产生气泡,溶液温度由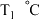 升到
升到 片表面无明显变化,溶液温度无变化。
片表面无明显变化,溶液温度无变化。 片与稀硫酸反应的能量变化关系符合图
片与稀硫酸反应的能量变化关系符合图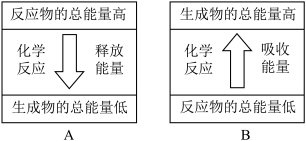
 片、
片、 片相连接,插入盛有
片相连接,插入盛有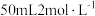 稀硫酸的烧杯中(如图
稀硫酸的烧杯中(如图 所示)。
所示)。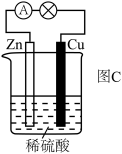
 片表面产生气泡,溶液温度由
片表面产生气泡,溶液温度由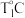 升到
升到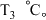
②结合电子的移动方向,解释
 片表面产生气泡的原因:该原电池中
片表面产生气泡的原因:该原电池中 失电子,
失电子,(5)实验Ⅰ和Ⅱ产生等量气体时,测得
 。结合能量的转化形式,分析两溶液温度变化幅度
。结合能量的转化形式,分析两溶液温度变化幅度(6)将
 片和
片和 片换成
片换成 片和石墨棒,重复实验Ⅱ,请判断电流表指针是否发生偏转。若不偏转,说明理由;若偏转,写出
片和石墨棒,重复实验Ⅱ,请判断电流表指针是否发生偏转。若不偏转,说明理由;若偏转,写出 片表面发生的电极反应式。理由或电极反应式是
片表面发生的电极反应式。理由或电极反应式是
您最近半年使用:0次
4 . 下列反应中,属于吸热反应的是
| A.铝与盐酸的反应 | B.氢气在氯气中燃烧 |
| C.氢氧化钠与盐酸的反应 | D.煅烧石灰石 |
您最近半年使用:0次
5 . 工业上由CO2和H2合成气态甲醇的热化学方程式为CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH<0。已知该反应是放热反应。下列表示合成甲醇的反应的能量变化示意图正确的是
A. | B.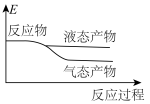 | C. | D.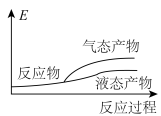 |
您最近半年使用:0次
6 . 化学反应伴随能量变化,获取反应能量变化有多种途径。
(1)下列反应中,属于吸热反应的是___________(填字母)。
(2)获取能量变化的途径
①通过化学键的键能计算。已知:
则2H2(g)+O2(g)=2H2O(g)ΔH=___________ kJ·mol-1。
②通过物质所含能量计算。
已知反应A+B=C+D中A、B、C、D所含能量依次可表示为EA、EB、EC、ED,该反应ΔH=___________ 。
③通过盖斯定律计算。已知在25℃、101kPa时:
Ⅰ.2Na(s)+ O2(g)=Na2O(s)ΔH=-414kJ·mol-1
O2(g)=Na2O(s)ΔH=-414kJ·mol-1
Ⅱ.2Na(s)+O2(g)=Na2O2(s)ΔH=-511kJ·mol-1
写出Na2O2与Na反应生成Na2O的热化学方程式:___________ 。
④利用实验装置测量。测量盐酸与NaOH溶液反应的热量变化的过程中,若取50mL0.50mol·L-1盐酸,则还需加入___________ (填字母)。
A.50mL0.50mol·L-1NaOH溶液
B.50mL0.55mol·L-1NaOH溶液
C.1.0gNaOH固体
(1)下列反应中,属于吸热反应的是___________(填字母)。
| A.Na2O与水反应 | B.甲烷的燃烧反应 | C.CaCO3受热分解 | D.锌与盐酸反应 |
①通过化学键的键能计算。已知:
| 化学键 | H—H | O=O | O—H |
| 键能/(kJ·mol-1) | 436 | 498 | 463.4 |
②通过物质所含能量计算。
已知反应A+B=C+D中A、B、C、D所含能量依次可表示为EA、EB、EC、ED,该反应ΔH=
③通过盖斯定律计算。已知在25℃、101kPa时:
Ⅰ.2Na(s)+
 O2(g)=Na2O(s)ΔH=-414kJ·mol-1
O2(g)=Na2O(s)ΔH=-414kJ·mol-1Ⅱ.2Na(s)+O2(g)=Na2O2(s)ΔH=-511kJ·mol-1
写出Na2O2与Na反应生成Na2O的热化学方程式:
④利用实验装置测量。测量盐酸与NaOH溶液反应的热量变化的过程中,若取50mL0.50mol·L-1盐酸,则还需加入
A.50mL0.50mol·L-1NaOH溶液
B.50mL0.55mol·L-1NaOH溶液
C.1.0gNaOH固体
您最近半年使用:0次
7 . 下列关于热化学反应的描述正确的是
A.稀盐酸和 稀溶液反应的中和反应反应热 稀溶液反应的中和反应反应热 ,则1mol的稀硫酸与足量氢氧化钡溶液反应放出的热量为 ,则1mol的稀硫酸与足量氢氧化钡溶液反应放出的热量为 |
B. 的燃烧热为 的燃烧热为 ,则反应2H2O(l)=2H2(g)+O2(g)的 ,则反应2H2O(l)=2H2(g)+O2(g)的 |
| C.放热反应比吸热反应容易发生 |
| D.丙烷燃烧生成水和二氧化碳所放出的热量是丙烷的燃烧热 |
您最近半年使用:0次
解题方法
8 . 已知反应 的反应过程如图所示,下列说法错误的是
的反应过程如图所示,下列说法错误的是
 的反应过程如图所示,下列说法错误的是
的反应过程如图所示,下列说法错误的是
A.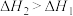 | B.R、M可能互为同素异形体 |
| C.总反应为放热反应 | D.M的稳定性在R、X、M中是最强的 |
您最近半年使用:0次
名校
解题方法
9 . Ⅰ.反应 的能量变化如图所示:
的能量变化如图所示:______ 反应(填“吸热”或“放热”)。
(2)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为______ (填“正”或“负”)极,铜电极上反应的电极反应式为:____________ 。
(3)若要使Fe与稀硫酸的反应速率加快,下列措施可行的是______。
Ⅱ.在一定温度下将2 mol A气体和4 mol B气体在2 L体积不变的密闭容器中混合并发生反应: 。若经2 min后测得C的浓度为0.6 mol·L
。若经2 min后测得C的浓度为0.6 mol·L ,则:
,则:
(4)用物质A表示的反应速率为______ 。
(5)2 min时物质B的浓度为______ 。B的转化率为______ 。
(6)当下列哪些项表明上述反应已达到平衡状态______ 。
A.单位时间内消耗1 mol B同时生成1.5 mol C
B.生成物D的浓度不再发生变化
C.正反应速率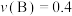 mol⋅L
mol⋅L ⋅min
⋅min ,逆反应速率
,逆反应速率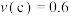 mol⋅L
mol⋅L ⋅min
⋅min
D.混合气体的总物质的量不再发生变化
E.用A、B、C表示的速率比为1∶2∶3
(7)下列说法正确的是______。
 的能量变化如图所示:
的能量变化如图所示:
(2)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为
(3)若要使Fe与稀硫酸的反应速率加快,下列措施可行的是______。
| A.改铁片为铁粉 | B.改稀硫酸为98%的硫酸 |
| C.增大压强 | D.滴加几滴 溶液 溶液 |
Ⅱ.在一定温度下将2 mol A气体和4 mol B气体在2 L体积不变的密闭容器中混合并发生反应:
 。若经2 min后测得C的浓度为0.6 mol·L
。若经2 min后测得C的浓度为0.6 mol·L ,则:
,则:(4)用物质A表示的反应速率为
(5)2 min时物质B的浓度为
(6)当下列哪些项表明上述反应已达到平衡状态
A.单位时间内消耗1 mol B同时生成1.5 mol C
B.生成物D的浓度不再发生变化
C.正反应速率
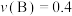 mol⋅L
mol⋅L ⋅min
⋅min ,逆反应速率
,逆反应速率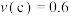 mol⋅L
mol⋅L ⋅min
⋅min
D.混合气体的总物质的量不再发生变化
E.用A、B、C表示的速率比为1∶2∶3
(7)下列说法正确的是______。
| A.当一个化学反应在一定条件下达到限度时,反应即停止 |
| B.化学反应的限度与时间长短无关 |
| C.增大B的浓度,正反应速率加快,逆反应速率减慢 |
| D.化学反应的限度是不可能改变的 |
您最近半年使用:0次
10 . 下列反应中属于放热反应的是
| A.盐酸与碳酸氢钠的反应 | B.灼热的碳与二氧化碳的反应 |
| C.氢氧化钠溶液与盐酸的反应 | D. 晶体与 晶体与 晶体的反应 晶体的反应 |
您最近半年使用:0次



