名校
1 . 反应2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g);△H<0可实现CO2的资源化,下列说法正确的是
CH3OCH3(g)+3H2O(g);△H<0可实现CO2的资源化,下列说法正确的是
 CH3OCH3(g)+3H2O(g);△H<0可实现CO2的资源化,下列说法正确的是
CH3OCH3(g)+3H2O(g);△H<0可实现CO2的资源化,下列说法正确的是| A.上述反应在任何温度下均可自发进行 |
| B.上述反应反应物的总能量大于生成物的总能量 |
C.上述反应平衡常数K=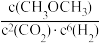 |
| D.上述反应达到平衡后,加入催化剂,平衡正向移动 |
您最近半年使用:0次
2 . 将 还原转化为有用的化学产品是目前研究的热点之一、回答下列问题:
还原转化为有用的化学产品是目前研究的热点之一、回答下列问题:
Ⅰ.用铜铝催化剂可将 加氢合成甲醇,已知过程中发生的反应如下:
加氢合成甲醇,已知过程中发生的反应如下:
ⅰ.


ⅱ.


ⅲ.


(1)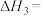
_____ (用含 、
、 的代数式表示),
的代数式表示),
_____ (用含 、
、 的代数式表示)。
的代数式表示)。
(2)查阅资料可知, ,则
,则_____ (填“低温"“商温”或“任意温度”)条件下有利于反应ⅲ自发进行。
Ⅱ. 和
和 以1:3的物质的量之比通入某密闭容器中,仅发生反应
以1:3的物质的量之比通入某密闭容器中,仅发生反应 ,
, 的平衡转化率与温度、气体的总压强的关系如图所示:
的平衡转化率与温度、气体的总压强的关系如图所示: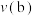
______ (填“>”“<”或“=”)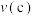 。
。
(4)平衡常数: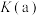
____ (填“>”“<”或“=”)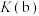 。
。
(5)压强:
______ (填“>”“<”或“=”) 。
。
(6)b点时,该反应的平衡常数
______ (分压=总压×物质的量分数,用含x、 的代数式表示)。
的代数式表示)。
Ⅲ.常温下,CH4和CO2都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图所示: 和
和 的体积比为
的体积比为______ 。
 还原转化为有用的化学产品是目前研究的热点之一、回答下列问题:
还原转化为有用的化学产品是目前研究的热点之一、回答下列问题:Ⅰ.用铜铝催化剂可将
 加氢合成甲醇,已知过程中发生的反应如下:
加氢合成甲醇,已知过程中发生的反应如下:ⅰ.



ⅱ.



ⅲ.



(1)
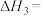
 、
、 的代数式表示),
的代数式表示),
 、
、 的代数式表示)。
的代数式表示)。(2)查阅资料可知,
 ,则
,则Ⅱ.
 和
和 以1:3的物质的量之比通入某密闭容器中,仅发生反应
以1:3的物质的量之比通入某密闭容器中,仅发生反应 ,
, 的平衡转化率与温度、气体的总压强的关系如图所示:
的平衡转化率与温度、气体的总压强的关系如图所示:
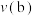
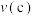 。
。(4)平衡常数:
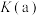
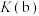 。
。(5)压强:

 。
。(6)b点时,该反应的平衡常数

 的代数式表示)。
的代数式表示)。Ⅲ.常温下,CH4和CO2都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图所示:
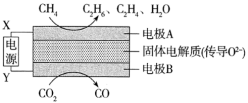
 和
和 的体积比为
的体积比为
您最近半年使用:0次
名校
解题方法
3 . 一定条件下,在密闭容器中利用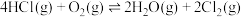 制备
制备 ,下列有关说法正确的是
,下列有关说法正确的是
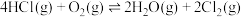 制备
制备 ,下列有关说法正确的是
,下列有关说法正确的是A.若断开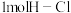 键的同时有 键的同时有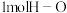 键断开,则表明该反应达到平衡状态 键断开,则表明该反应达到平衡状态 |
B.提高 ,该反应的平衡常数增大 ,该反应的平衡常数增大 |
C.使用催化剂,可以提高 的平衡转化率 的平衡转化率 |
D.该反应在一定条件下可自发进行,则该反应 |
您最近半年使用:0次
名校
解题方法
4 . 已知, 生产甲醇过程主要发生以下反应:
生产甲醇过程主要发生以下反应:
反应I.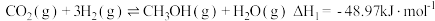
反应II.
反应III.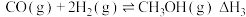
(1)反应III中, H=
H=_____________  ,该反应在
,该反应在_______ 条件下能自发进行。
A.在低温条件下自发进行 B.在高温条件下自发进行
C.在任何条件下都能自发进行 D.在任何条件下都不能自发进行
(2)反应III中, 的平衡转化率与温度的关系如图所示:
的平衡转化率与温度的关系如图所示: 两点压强大小关系是pA
两点压强大小关系是pA_____________ pB(填“ 、
、 、
、 ”)。
”)。
② 三点平衡常数
三点平衡常数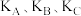 的大小关系为
的大小关系为_____________ 。 时,由D点到A点过程中正、逆反应速率之间的关系:v正
时,由D点到A点过程中正、逆反应速率之间的关系:v正_____________ v逆。(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。
(3)完成下列问题。
①向某恒温恒压密闭容器中充入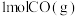 和
和 ,下列能说明反应III达到平衡的是
,下列能说明反应III达到平衡的是_______ 。
A.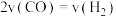
B.两种反应物转化率的比值不再改变
C.容器内混合气体的平均相对分子质量不再改变
D.容器内混合气体的密度不再改变
②在 恒容密闭容器中充入
恒容密闭容器中充入 和
和 ,在
,在 和
和 条件下经
条件下经 达到平衡状态。在该条件下,v(H2)=
达到平衡状态。在该条件下,v(H2)=_______ 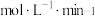 。
。
(4)已知: 的选择性
的选择性 ,不考虑催化剂活性温度,为同时提高
,不考虑催化剂活性温度,为同时提高 的平衡转化率和甲醇的选择性,应选择的反应条件是
的平衡转化率和甲醇的选择性,应选择的反应条件是_______ ,说明其原因_____________________ 。
A.低温低压 B.低温高压 C.高温高压 D.高温低压
 生产甲醇过程主要发生以下反应:
生产甲醇过程主要发生以下反应:反应I.
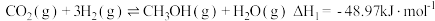
反应II.

反应III.
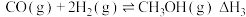
(1)反应III中,
 H=
H= ,该反应在
,该反应在A.在低温条件下自发进行 B.在高温条件下自发进行
C.在任何条件下都能自发进行 D.在任何条件下都不能自发进行
(2)反应III中,
 的平衡转化率与温度的关系如图所示:
的平衡转化率与温度的关系如图所示: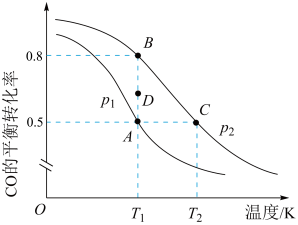
 两点压强大小关系是pA
两点压强大小关系是pA 、
、 、
、 ”)。
”)。②
 三点平衡常数
三点平衡常数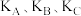 的大小关系为
的大小关系为 时,由D点到A点过程中正、逆反应速率之间的关系:v正
时,由D点到A点过程中正、逆反应速率之间的关系:v正 ”、“
”、“ ”或“
”或“ ”)。
”)。(3)完成下列问题。
①向某恒温恒压密闭容器中充入
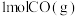 和
和 ,下列能说明反应III达到平衡的是
,下列能说明反应III达到平衡的是A.
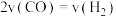
B.两种反应物转化率的比值不再改变
C.容器内混合气体的平均相对分子质量不再改变
D.容器内混合气体的密度不再改变
②在
 恒容密闭容器中充入
恒容密闭容器中充入 和
和 ,在
,在 和
和 条件下经
条件下经 达到平衡状态。在该条件下,v(H2)=
达到平衡状态。在该条件下,v(H2)=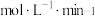 。
。(4)已知:
 的选择性
的选择性 ,不考虑催化剂活性温度,为同时提高
,不考虑催化剂活性温度,为同时提高 的平衡转化率和甲醇的选择性,应选择的反应条件是
的平衡转化率和甲醇的选择性,应选择的反应条件是A.低温低压 B.低温高压 C.高温高压 D.高温低压
您最近半年使用:0次
5 . “碳中和”目标如期实现的关键技术之一是CO2的再资源化利用。
(1)将二氧化碳转化为甲醇是目前研究的热点之一,在催化剂作用下主要发生以下反应:
Ⅰ.
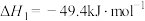
Ⅱ.
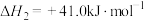
Ⅲ.

反应Ⅲ自发进行的条件及判断依据是__________ 。
(2)保持压强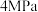 ,将起始
,将起始 的混合气体匀速通过装有催化剂的反应管,只发生上述反应Ⅰ和反应Ⅱ,测得出口处CO2的转化率和甲醇的选择性[
的混合气体匀速通过装有催化剂的反应管,只发生上述反应Ⅰ和反应Ⅱ,测得出口处CO2的转化率和甲醇的选择性[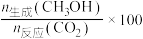 %]与温度的关系如图1、图2所示。
%]与温度的关系如图1、图2所示。 %,计算340℃时三种催化剂的催化效率之比
%,计算340℃时三种催化剂的催化效率之比
__________ 。
②随着温度的升高,CO2转化率增大,但甲醇选择性降低的原因是__________ 。
(3)甲醇再应用:在催化剂作用下,工业用甲醇空气氧化法制甲醛。
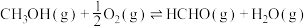
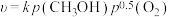
该反应为下面两个基元反应的合并:
反应Ⅰ: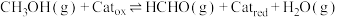

反应Ⅱ: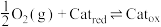

k、k1、k2为速率方程常数,分压p等于其物质的量分数乘以总压,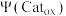 为氧化态催化剂的物质的量分数;
为氧化态催化剂的物质的量分数;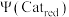 为还原态催化剂的物质的量分数;反应Ⅰ为决速步。
为还原态催化剂的物质的量分数;反应Ⅰ为决速步。
下列说法不正确 的是__________。
(4)处理CO2吸收液:用惰性电极电解吸收液(成分为饱和NaHCO3溶液),阴极区通入CO2共同电解,阴极产物为常见有机物,阳极气体产物吸收后再应用。
现用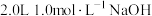 溶液吸收阳极逸出的气体,不考虑气体溶解残留,当电路中转移
溶液吸收阳极逸出的气体,不考虑气体溶解残留,当电路中转移 时,所得溶液中
时,所得溶液中
__________  。
。
(已知 的电离常数
的电离常数 ,
, )
)
(1)将二氧化碳转化为甲醇是目前研究的热点之一,在催化剂作用下主要发生以下反应:
Ⅰ.

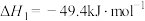
Ⅱ.

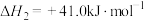
Ⅲ.


反应Ⅲ自发进行的条件及判断依据是
(2)保持压强
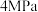 ,将起始
,将起始 的混合气体匀速通过装有催化剂的反应管,只发生上述反应Ⅰ和反应Ⅱ,测得出口处CO2的转化率和甲醇的选择性[
的混合气体匀速通过装有催化剂的反应管,只发生上述反应Ⅰ和反应Ⅱ,测得出口处CO2的转化率和甲醇的选择性[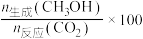 %]与温度的关系如图1、图2所示。
%]与温度的关系如图1、图2所示。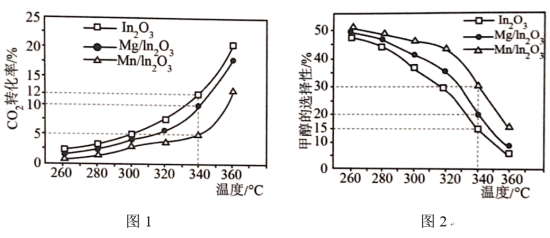
 %,计算340℃时三种催化剂的催化效率之比
%,计算340℃时三种催化剂的催化效率之比
②随着温度的升高,CO2转化率增大,但甲醇选择性降低的原因是
(3)甲醇再应用:在催化剂作用下,工业用甲醇空气氧化法制甲醛。
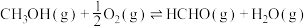
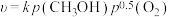
该反应为下面两个基元反应的合并:
反应Ⅰ:
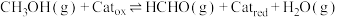

反应Ⅱ:
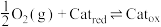

k、k1、k2为速率方程常数,分压p等于其物质的量分数乘以总压,
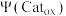 为氧化态催化剂的物质的量分数;
为氧化态催化剂的物质的量分数;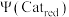 为还原态催化剂的物质的量分数;反应Ⅰ为决速步。
为还原态催化剂的物质的量分数;反应Ⅰ为决速步。下列说法
| A.改用更高效的催化剂可提高反应Ⅰ的平衡转化率 |
B.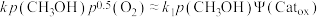 |
| C.Catred在体系中含量很低,升高温度会适当增加Catred在体系中的含量 |
D.若 和 和 的分压增大相同倍数, 的分压增大相同倍数, 比 比 对总反应速率的影响大 对总反应速率的影响大 |
现用
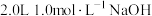 溶液吸收阳极逸出的气体,不考虑气体溶解残留,当电路中转移
溶液吸收阳极逸出的气体,不考虑气体溶解残留,当电路中转移 时,所得溶液中
时,所得溶液中
 。
。(已知
 的电离常数
的电离常数 ,
, )
)
您最近半年使用:0次
6 . 碲(Te)是半导体、红外探测等领域的重要战略元素。从阳极泥或冶炼烟尘中提取的粗二氧化碲中含有 、PbO、CuO等杂质。一种由粗二氧化碲提取纯碲的工艺流程如图所示。
、PbO、CuO等杂质。一种由粗二氧化碲提取纯碲的工艺流程如图所示。
(1)“浸出”步骤中,碲和硒两种元素分别转化为 和
和 。浸出温度控制在65℃左右,当温度超过80℃时,碲的浸出率会小幅降低。降低的主要原因是
。浸出温度控制在65℃左右,当温度超过80℃时,碲的浸出率会小幅降低。降低的主要原因是___________ 。
(2) 的沸点(387℃)高于
的沸点(387℃)高于 的沸点(191.4℃),原因是
的沸点(191.4℃),原因是___________ 。
(3)“净化”步骤中产生的滤渣主要含___________ (写化学式)和少量硒单质。
(4)化学反应的吉布斯自由能变 。
。 还原
还原 和
和 的
的 随温度T的变化曲线如图所示。则“还原除杂”步骤的温度不宜超过
随温度T的变化曲线如图所示。则“还原除杂”步骤的温度不宜超过___________ K,该步骤控制在此温度以下的原因是___________ 。___________ 。
(6)“还原”后的酸性还原尾液中含有少量未被还原的碲,加入还原剂R进行“尾还原”,可以产生粗碲,提高碲的回收率。综合还原效率、工艺成本和环保因素,最合适的还原剂是___________ (填标号)。
A.铁粉 B.氢气 C.硫化钠
 、PbO、CuO等杂质。一种由粗二氧化碲提取纯碲的工艺流程如图所示。
、PbO、CuO等杂质。一种由粗二氧化碲提取纯碲的工艺流程如图所示。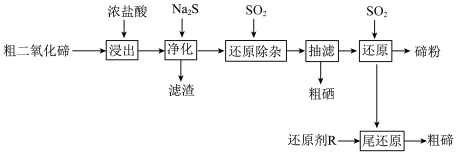
(1)“浸出”步骤中,碲和硒两种元素分别转化为
 和
和 。浸出温度控制在65℃左右,当温度超过80℃时,碲的浸出率会小幅降低。降低的主要原因是
。浸出温度控制在65℃左右,当温度超过80℃时,碲的浸出率会小幅降低。降低的主要原因是(2)
 的沸点(387℃)高于
的沸点(387℃)高于 的沸点(191.4℃),原因是
的沸点(191.4℃),原因是(3)“净化”步骤中产生的滤渣主要含
(4)化学反应的吉布斯自由能变
 。
。 还原
还原 和
和 的
的 随温度T的变化曲线如图所示。则“还原除杂”步骤的温度不宜超过
随温度T的变化曲线如图所示。则“还原除杂”步骤的温度不宜超过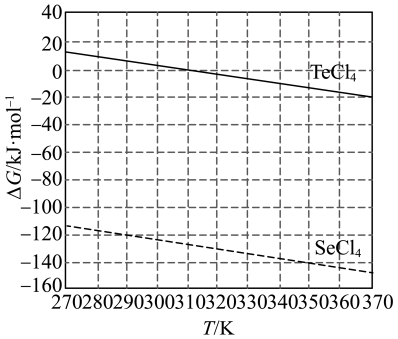
(6)“还原”后的酸性还原尾液中含有少量未被还原的碲,加入还原剂R进行“尾还原”,可以产生粗碲,提高碲的回收率。综合还原效率、工艺成本和环保因素,最合适的还原剂是
A.铁粉 B.氢气 C.硫化钠
您最近半年使用:0次
7日内更新
|
186次组卷
|
2卷引用:河南省周口市2024届高三二模理综-化学试题
解题方法
7 . 甲醇是重要的化工原料,工业上可利用 生产甲醇,同时可降低温室气体二氧化碳的排放。
生产甲醇,同时可降低温室气体二氧化碳的排放。
已知:①
②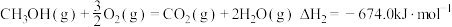
③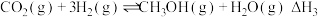
(1)
___________  ,反应③在
,反应③在___________ (填“高温”、“低温”或“任何温度”)下能自发进行。
(2)下列措施中,能提高 平衡转化率的是___________(填标号)。
平衡转化率的是___________(填标号)。
(3)在一密闭容器中加入 和
和 ,在一定条件下进行反应③,测得CO2(g)的平衡转化率与温度、压强的关系如图所示。
,在一定条件下进行反应③,测得CO2(g)的平衡转化率与温度、压强的关系如图所示。
___________ (填“>”“=”或“<”,下同) ,理由是
,理由是___________ 。
②当压强为 时,B点
时,B点
___________  。
。
③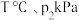 下,
下, 的平衡体积分数为
的平衡体积分数为___________ %,该条件下反应③的压强平衡常数
___________  (以分压表示,分压=总压×物质的量分数)。
(以分压表示,分压=总压×物质的量分数)。
 生产甲醇,同时可降低温室气体二氧化碳的排放。
生产甲醇,同时可降低温室气体二氧化碳的排放。已知:①

②
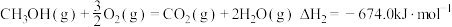
③
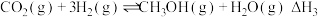
(1)

 ,反应③在
,反应③在(2)下列措施中,能提高
 平衡转化率的是___________(填标号)。
平衡转化率的是___________(填标号)。| A.压缩容器体积 | B.将 液化分离出来 液化分离出来 | C.恒容下充入 | D.使用高效催化剂 |
(3)在一密闭容器中加入
 和
和 ,在一定条件下进行反应③,测得CO2(g)的平衡转化率与温度、压强的关系如图所示。
,在一定条件下进行反应③,测得CO2(g)的平衡转化率与温度、压强的关系如图所示。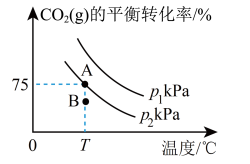

 ,理由是
,理由是②当压强为
 时,B点
时,B点
 。
。③
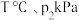 下,
下, 的平衡体积分数为
的平衡体积分数为
 (以分压表示,分压=总压×物质的量分数)。
(以分压表示,分压=总压×物质的量分数)。
您最近半年使用:0次
名校
解题方法
8 . 汽车尾气中含有CO、NO2等有毒气体,对汽车家装尾气净化装置,可使有毒气体相互反应转化为无毒气体。
已知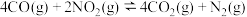
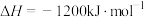
(1)该反应在___________ (填“高温、低温或任何温度”)下能自发进行。
(2)对于该反应,改变某一反应条件(温度 ),下列图象正确的是___________(填标号)。
),下列图象正确的是___________(填标号)。
(3)某实验小组模拟上述净化过程,一定温度下,在 的恒容密闭容器中,起始时按照甲、乙两种方式进行投料。甲:
的恒容密闭容器中,起始时按照甲、乙两种方式进行投料。甲: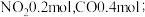 乙:
乙: ,经过一段时间后达到平衡状态。
,经过一段时间后达到平衡状态。
① 的平衡体积分数:甲
的平衡体积分数:甲___________ 乙(填“>、=、<或不确定”,下同)。
② 的平衡浓度:甲
的平衡浓度:甲___________ 乙。
③甲中 的转化率为
的转化率为 ,该反应的平衡常数为
,该反应的平衡常数为___________ 。
已知
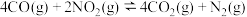
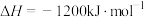
(1)该反应在
(2)对于该反应,改变某一反应条件(温度
 ),下列图象正确的是___________(填标号)。
),下列图象正确的是___________(填标号)。A.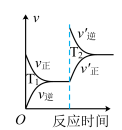 | B.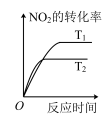 | C.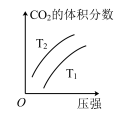 | D.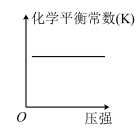 |
(3)某实验小组模拟上述净化过程,一定温度下,在
 的恒容密闭容器中,起始时按照甲、乙两种方式进行投料。甲:
的恒容密闭容器中,起始时按照甲、乙两种方式进行投料。甲: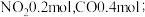 乙:
乙: ,经过一段时间后达到平衡状态。
,经过一段时间后达到平衡状态。①
 的平衡体积分数:甲
的平衡体积分数:甲②
 的平衡浓度:甲
的平衡浓度:甲③甲中
 的转化率为
的转化率为 ,该反应的平衡常数为
,该反应的平衡常数为
您最近半年使用:0次
解题方法
9 . Ⅰ、化学实验中,通常需要使用到硫酸
(1)向Na2S2O3溶液滴加稀硫酸,产生淡黄色沉淀,写出反应的离子方程式___________ 。
(2)向硫酸酸化的KMnO4溶液中滴加草酸溶液,紫红色褪去。写出反应的离子方程式___________ 。
Ⅱ、氢气作为一种清洁能源,一直是能源研究的热点,工业上制取氢气有多种方法:
①C(s)+H2O(g)=CO(g)+H2(g) △H1=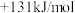
②CH4(g)+CO2(g)=2CO(g)+2H2(g) △H2=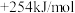
③CH4(g)+H2O(g)=CO(g)+3H2(g) △H3=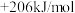
④CH3OH(1)=CO(g)+2H2(g) △H4=
(3)根据以上数据,请写出CH4(g)分解生成C(s)和H2(g)的热化学方程式___________ 。反应②需要在___________ (高温、低温)下才能自发进行
(4)几种化学键的键能如下表所示:
根据以上有关反应的△H,计算x=___________ 。
(5)我国科学家通过计算机模拟,研究了在某催化剂表面上发生反应④的反应历程(吸附在催化剂表面的物质,用"*"标注)。甲醇(CH3OH)脱氢反应的第一步历程,有两种可能方式:
方式Ⅰ: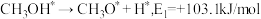
方式Ⅱ:
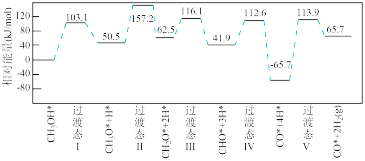
活化能E值推测,甲醇脱氢过程中主要历程的方式为___________ (填"Ⅰ"或"Ⅱ")。计算机模拟的各步反应的能量变化示意图如下。___________ 。
(1)向Na2S2O3溶液滴加稀硫酸,产生淡黄色沉淀,写出反应的离子方程式
(2)向硫酸酸化的KMnO4溶液中滴加草酸溶液,紫红色褪去。写出反应的离子方程式
Ⅱ、氢气作为一种清洁能源,一直是能源研究的热点,工业上制取氢气有多种方法:
①C(s)+H2O(g)=CO(g)+H2(g) △H1=
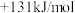
②CH4(g)+CO2(g)=2CO(g)+2H2(g) △H2=
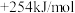
③CH4(g)+H2O(g)=CO(g)+3H2(g) △H3=
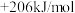
④CH3OH(1)=CO(g)+2H2(g) △H4=

(3)根据以上数据,请写出CH4(g)分解生成C(s)和H2(g)的热化学方程式
(4)几种化学键的键能如下表所示:
| 化学键 | C=O | H—H | 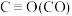 | C—H | O—H |
| 键能/kJ·mol-1 | 803 | 436 | x | 414 | 463 |
(5)我国科学家通过计算机模拟,研究了在某催化剂表面上发生反应④的反应历程(吸附在催化剂表面的物质,用"*"标注)。甲醇(CH3OH)脱氢反应的第一步历程,有两种可能方式:
方式Ⅰ:
方式Ⅱ:

活化能E值推测,甲醇脱氢过程中主要历程的方式为
您最近半年使用:0次
名校
10 . 哈伯法合成氨技术是德国诺贝尔化学奖获得者哈伯发明的。其合成原理为:N2(g)+3H2(g) 2NH3(g)
2NH3(g)  H<0,
H<0, S<0。下列有关工业合成氨的说法正确的是
S<0。下列有关工业合成氨的说法正确的是
 2NH3(g)
2NH3(g)  H<0,
H<0, S<0。下列有关工业合成氨的说法正确的是
S<0。下列有关工业合成氨的说法正确的是A.因为 H<0,所以该反应一定能自发进行 H<0,所以该反应一定能自发进行 |
B.因为 S<0,所以该反应一定不能自发进行 S<0,所以该反应一定不能自发进行 |
| C.在低温下进行是为了提高反应物的转化率 |
| D.使用催化剂加快反应速率是因为催化剂降低了反应的活化能 |
您最近半年使用:0次



