Ⅰ、化学实验中,通常需要使用到硫酸
(1)向Na2S2O3溶液滴加稀硫酸,产生淡黄色沉淀,写出反应的离子方程式___________ 。
(2)向硫酸酸化的KMnO4溶液中滴加草酸溶液,紫红色褪去。写出反应的离子方程式___________ 。
Ⅱ、氢气作为一种清洁能源,一直是能源研究的热点,工业上制取氢气有多种方法:
①C(s)+H2O(g)=CO(g)+H2(g) △H1=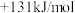
②CH4(g)+CO2(g)=2CO(g)+2H2(g) △H2=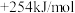
③CH4(g)+H2O(g)=CO(g)+3H2(g) △H3=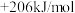
④CH3OH(1)=CO(g)+2H2(g) △H4=
(3)根据以上数据,请写出CH4(g)分解生成C(s)和H2(g)的热化学方程式___________ 。反应②需要在___________ (高温、低温)下才能自发进行
(4)几种化学键的键能如下表所示:
根据以上有关反应的△H,计算x=___________ 。
(5)我国科学家通过计算机模拟,研究了在某催化剂表面上发生反应④的反应历程(吸附在催化剂表面的物质,用"*"标注)。甲醇(CH3OH)脱氢反应的第一步历程,有两种可能方式:
方式Ⅰ: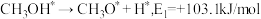
方式Ⅱ:
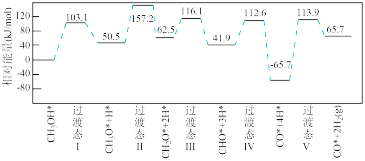
活化能E值推测,甲醇脱氢过程中主要历程的方式为___________ (填"Ⅰ"或"Ⅱ")。计算机模拟的各步反应的能量变化示意图如下。___________ 。
(1)向Na2S2O3溶液滴加稀硫酸,产生淡黄色沉淀,写出反应的离子方程式
(2)向硫酸酸化的KMnO4溶液中滴加草酸溶液,紫红色褪去。写出反应的离子方程式
Ⅱ、氢气作为一种清洁能源,一直是能源研究的热点,工业上制取氢气有多种方法:
①C(s)+H2O(g)=CO(g)+H2(g) △H1=
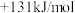
②CH4(g)+CO2(g)=2CO(g)+2H2(g) △H2=
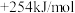
③CH4(g)+H2O(g)=CO(g)+3H2(g) △H3=
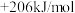
④CH3OH(1)=CO(g)+2H2(g) △H4=

(3)根据以上数据,请写出CH4(g)分解生成C(s)和H2(g)的热化学方程式
(4)几种化学键的键能如下表所示:
| 化学键 | C=O | H—H | 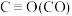 | C—H | O—H |
| 键能/kJ·mol-1 | 803 | 436 | x | 414 | 463 |
(5)我国科学家通过计算机模拟,研究了在某催化剂表面上发生反应④的反应历程(吸附在催化剂表面的物质,用"*"标注)。甲醇(CH3OH)脱氢反应的第一步历程,有两种可能方式:
方式Ⅰ:
方式Ⅱ:

活化能E值推测,甲醇脱氢过程中主要历程的方式为
更新时间:2024-04-23 22:02:13
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】元素铬(Cr)在自然界主要以+3价和+6价存在。
(1)工业上利用铬铁矿(FeO·Cr2O3)冶炼铬的工艺流程如图所示:
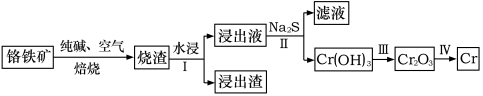
①为加快焙烧速率和提高原料的利用率,可采取的措施之一是___ 。
②“水浸Ⅰ”要获得“浸出液”的操作是____ 。已知“浸出液”的主要成分为Na2CrO4,则Cr2O3在高温焙烧时反应的化学方程式为___ 。
③若向“滤液”中加入盐酸酸化的氯化钡溶液有白色沉淀生成,则操作Ⅱ发生反应的离子方程式为___ 。
(2)含有Cr2O 的废水毒性较大,某工厂为了使废水的排放达标,进行如下处理:
的废水毒性较大,某工厂为了使废水的排放达标,进行如下处理:
Cr2O
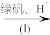 Cr3+、Fe3+
Cr3+、Fe3+ Cr(OH)3、Fe(OH)3
Cr(OH)3、Fe(OH)3
①该废水中加入绿矾(FeSO4·7H2O)和H+,发生反应的离子方程式为___ 。
②若处理后的废水中残留的c(Fe3+)=2.0×10-13mol·L-1,则残留的Cr3+的浓度为____ 。(已知:Ksp[Fe(OH)3]=4.0×10-38,Ksp[Cr(OH)3]=6.0×10-31)
(1)工业上利用铬铁矿(FeO·Cr2O3)冶炼铬的工艺流程如图所示:

①为加快焙烧速率和提高原料的利用率,可采取的措施之一是
②“水浸Ⅰ”要获得“浸出液”的操作是
③若向“滤液”中加入盐酸酸化的氯化钡溶液有白色沉淀生成,则操作Ⅱ发生反应的离子方程式为
(2)含有Cr2O
 的废水毒性较大,某工厂为了使废水的排放达标,进行如下处理:
的废水毒性较大,某工厂为了使废水的排放达标,进行如下处理:Cr2O

 Cr3+、Fe3+
Cr3+、Fe3+ Cr(OH)3、Fe(OH)3
Cr(OH)3、Fe(OH)3①该废水中加入绿矾(FeSO4·7H2O)和H+,发生反应的离子方程式为
②若处理后的废水中残留的c(Fe3+)=2.0×10-13mol·L-1,则残留的Cr3+的浓度为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】高铁酸钾是一种高效多功能的新型非氯绿色消毒剂,主要用于饮水处理。实验小组制备高铁酸钾(K2FeO4)并探究其性质。
资料:K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
(1)制备K2FeO4(夹持装置略)
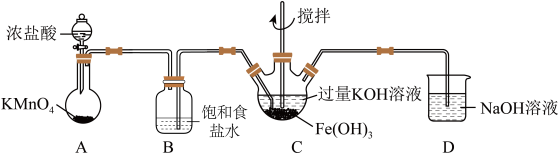
①如图所示,A为氯气发生装置。装置A、B、C、D中存在错误的是______________ (填序号)。
②C中得到紫色固体和溶液。C中通入氯气发生反应,生成高铁酸钾(K2FeO4)的化学方程式为_______ ,此外Cl2还可能与过量的KOH反应。
(2)探究K2FeO4的性质
①取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2。为证明是否K2FeO4,氧化了Cl-而产生Cl2,设计以下方案:
i.由方案I中溶液变红可知溶液a中含有__________ 离子,但该离子的存在不能判断一定是K2FeO4,氧化了Cl2,因为K2FeO4,在酸性溶液中不稳定,请写出K2FeO4在酸性溶液中发生反应的离子方程式___________________________________ 。
ii.方案Ⅱ可证明K2FeO4,氧化了Cl-.用KOH溶液洗涤的目的是_______________ 。
②根据K2FeO4的制备实验得出:氧化性Cl2_____ FeO42- (填“>”或“<”),而方案Ⅱ实验表明,Cl2和FeO42-的氧化性强弱关系恰好相反,原因是_______________ 。
(3)若在制备装置C中加入Fe(OH)3的质量为14.0g,充分反应后经过滤、洗涤、干燥得K2FeO4固体19.3g,则K2FeO4的产率为______________ 。
资料:K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
(1)制备K2FeO4(夹持装置略)

①如图所示,A为氯气发生装置。装置A、B、C、D中存在错误的是
②C中得到紫色固体和溶液。C中通入氯气发生反应,生成高铁酸钾(K2FeO4)的化学方程式为
(2)探究K2FeO4的性质
①取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2。为证明是否K2FeO4,氧化了Cl-而产生Cl2,设计以下方案:
| 方案I | 取少量溶液a,滴加KSCN溶液至过量,溶液呈红色。 |
| 方案II | 用KOH溶液充分洗涤C中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液b。取少量b,滴加盐酸,有Cl2产生。 |
i.由方案I中溶液变红可知溶液a中含有
ii.方案Ⅱ可证明K2FeO4,氧化了Cl-.用KOH溶液洗涤的目的是
②根据K2FeO4的制备实验得出:氧化性Cl2
(3)若在制备装置C中加入Fe(OH)3的质量为14.0g,充分反应后经过滤、洗涤、干燥得K2FeO4固体19.3g,则K2FeO4的产率为
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】硼镁泥是一种工业废料,主要成分是MgO(占40%,质量分数),还有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等杂质,以此为原料制取的硫酸镁,可用于印染、造纸、医药等工业。从硼镁泥中提取MgSO4∙7H2O的工艺流程如图:
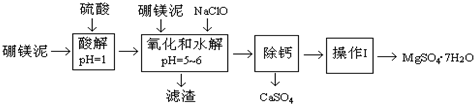
(1)实验中需要1 mol/L的硫酸800 mL,若用 98% 的浓硫酸(ρ= 1.84 g/mL)来配制,浓硫酸的浓度为_______ mol·L-1 ,量取浓硫酸需要使用量筒的规格为_______ (填写选项字母)
A.10 mL B.20 mL C.50 mL D.100 mL
(2)加入的NaClO可与Mn2+ 反应:Mn2+ + ClO‾ + H2O = MnO2↓+ 2H+ + Cl‾,在该步骤中还有一种离子也会被NaClO氧化,该反应的离子方程式为_______ 。
(3)滤渣的主要成分除含有Fe(OH)3、Al(OH)3外,还含有_______ 。
(4)在“除钙”前,需检验滤液中Fe3+ 是否被除尽,简述检验方法_______ 。(写出操作、现象和结论)
(5)已知MgSO4、CaSO4 的溶解度(单位为 g/100 g 水)如表:
“除钙”是将MgSO4和CaSO4混合溶液中的CaSO4除去,根据表中数据,简要说明操作步骤_______ 、_______ 。

(1)实验中需要1 mol/L的硫酸800 mL,若用 98% 的浓硫酸(ρ= 1.84 g/mL)来配制,浓硫酸的浓度为
A.10 mL B.20 mL C.50 mL D.100 mL
(2)加入的NaClO可与Mn2+ 反应:Mn2+ + ClO‾ + H2O = MnO2↓+ 2H+ + Cl‾,在该步骤中还有一种离子也会被NaClO氧化,该反应的离子方程式为
(3)滤渣的主要成分除含有Fe(OH)3、Al(OH)3外,还含有
(4)在“除钙”前,需检验滤液中Fe3+ 是否被除尽,简述检验方法
(5)已知MgSO4、CaSO4 的溶解度(单位为 g/100 g 水)如表:
| 温度(℃) | 40 | 50 | 60 | 70 |
| MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
| CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
“除钙”是将MgSO4和CaSO4混合溶液中的CaSO4除去,根据表中数据,简要说明操作步骤
您最近半年使用:0次
【推荐1】环境问题越来越受到人们的重视,“绿水青山就是金山银山”的理念已被人们认同。运用化学反应原理研究碳、氮、硫的单质及其化合物的反应对缓解环境污染具有重要意义。回答下列问题:
(1)亚硝酰氯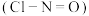 气体是有机合成中的重要试剂,它可由
气体是有机合成中的重要试剂,它可由 和
和 在通常条件下反应制得,该反应的热化学方程式为
在通常条件下反应制得,该反应的热化学方程式为___________ 。
相关化学键的键能如下表所示:
(2)为研究汽车尾气转化为无毒无害的物质的有关反应,在某恒容密闭容器中充入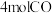 和
和 ,发生反应
,发生反应 ,平衡时
,平衡时 的体积分数与温度
的体积分数与温度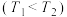 、压强的关系如图所示:
、压强的关系如图所示:

①该可逆反应达到平衡后,在提高反应速率的同时提高 的转化率,可采取的措施有
的转化率,可采取的措施有___________ (填字母序号)。
a.按体积比为 再充入
再充入 和
和 b.改用高效催化剂
b.改用高效催化剂
c.升高温度 d.增加 的浓度
的浓度
②由图可知,压强为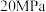 、温度为
、温度为 下的平衡常数Kp=
下的平衡常数Kp=________ MPa-1(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,保留2位有效数字)。
③若在 点将反应容器降低温度至
点将反应容器降低温度至 的同时缩小体积至体系压强增大,达到新的平衡状态时,可能是图中
的同时缩小体积至体系压强增大,达到新的平衡状态时,可能是图中 点中的
点中的___________ 点(填字母序号)。
(3)有人设想采用下列方法减少 对环境的污染:用
对环境的污染:用 还原
还原 ,从产物中分离出一种含硫质量分数约为
,从产物中分离出一种含硫质量分数约为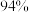 的化合物,并用这种化合物来还原
的化合物,并用这种化合物来还原 。这种含硫化合物和
。这种含硫化合物和 反应的化学方程式为
反应的化学方程式为___________ 。
(4)用 溶液吸收
溶液吸收 也是减少大气污染的一种有效方法。25℃时,将一定量的
也是减少大气污染的一种有效方法。25℃时,将一定量的 通入到
通入到 溶液中,两者完全反应,若溶液中
溶液中,两者完全反应,若溶液中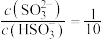 ,则该混合溶液的
,则该混合溶液的
___________ (25℃时, 的电离平衡常数
的电离平衡常数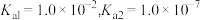 )。
)。
(5)科学家提出一种间接电化学法对大气污染物 进行无害化处理,其原理示意如图(质子膜允许
进行无害化处理,其原理示意如图(质子膜允许 和
和 通过)。
通过)。

电解池发生的反应为___________ 。
(1)亚硝酰氯
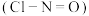 气体是有机合成中的重要试剂,它可由
气体是有机合成中的重要试剂,它可由 和
和 在通常条件下反应制得,该反应的热化学方程式为
在通常条件下反应制得,该反应的热化学方程式为相关化学键的键能如下表所示:
| 化学键 |  |  |  |  |
键能 | 243 | 630 | 200 | 607 |
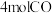 和
和 ,发生反应
,发生反应 ,平衡时
,平衡时 的体积分数与温度
的体积分数与温度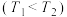 、压强的关系如图所示:
、压强的关系如图所示:
①该可逆反应达到平衡后,在提高反应速率的同时提高
 的转化率,可采取的措施有
的转化率,可采取的措施有a.按体积比为
 再充入
再充入 和
和 b.改用高效催化剂
b.改用高效催化剂c.升高温度 d.增加
 的浓度
的浓度②由图可知,压强为
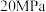 、温度为
、温度为 下的平衡常数Kp=
下的平衡常数Kp=③若在
 点将反应容器降低温度至
点将反应容器降低温度至 的同时缩小体积至体系压强增大,达到新的平衡状态时,可能是图中
的同时缩小体积至体系压强增大,达到新的平衡状态时,可能是图中 点中的
点中的(3)有人设想采用下列方法减少
 对环境的污染:用
对环境的污染:用 还原
还原 ,从产物中分离出一种含硫质量分数约为
,从产物中分离出一种含硫质量分数约为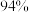 的化合物,并用这种化合物来还原
的化合物,并用这种化合物来还原 。这种含硫化合物和
。这种含硫化合物和 反应的化学方程式为
反应的化学方程式为(4)用
 溶液吸收
溶液吸收 也是减少大气污染的一种有效方法。25℃时,将一定量的
也是减少大气污染的一种有效方法。25℃时,将一定量的 通入到
通入到 溶液中,两者完全反应,若溶液中
溶液中,两者完全反应,若溶液中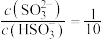 ,则该混合溶液的
,则该混合溶液的
 的电离平衡常数
的电离平衡常数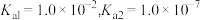 )。
)。(5)科学家提出一种间接电化学法对大气污染物
 进行无害化处理,其原理示意如图(质子膜允许
进行无害化处理,其原理示意如图(质子膜允许 和
和 通过)。
通过)。
电解池发生的反应为
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】请利用化学反应中的热效应原理,回答下列问题。
(1)已知: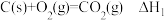
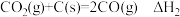
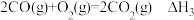
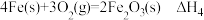
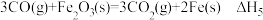
下列关于,上述反应焓变的判断不正确的是_______(填字母)。
(2)“嫦娥二号”卫星使用液态四氧化二氮和液态偏二甲肼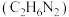 作推进剂。
作推进剂。 与偏二甲肼燃烧产物只有
与偏二甲肼燃烧产物只有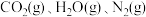 ,并放出大量热,已知
,并放出大量热,已知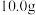 液态偏二甲肼与液态四氧化二氮完全燃烧可放出
液态偏二甲肼与液态四氧化二氮完全燃烧可放出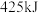 热量,该反应的热化学方程式为
热量,该反应的热化学方程式为_______ 。
(3)能源短缺是全球面临的问题,用 来生产燃料甲醇的反应原理为
来生产燃料甲醇的反应原理为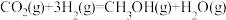 。已知某些化学键的键能数据如表所示。
。已知某些化学键的键能数据如表所示。
则该反应的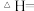
_______ 。
(4)氮氧化物是造成光化学烟雾和臭氧层损耗的主要气体。已知:
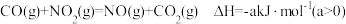
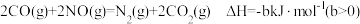
若用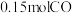 还原
还原 至
至 (
( 完全反应)的整个过程中转移电子的物质的量为
完全反应)的整个过程中转移电子的物质的量为_______  ,放出的热量为
,放出的热量为_______  (用含有a和b的代数式表示)。
(用含有a和b的代数式表示)。
(1)已知:
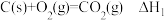
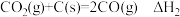
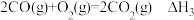
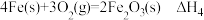
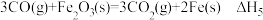
下列关于,上述反应焓变的判断不正确的是_______(填字母)。
A.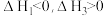 | B.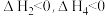 |
C.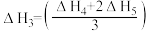 | D.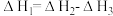 |
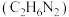 作推进剂。
作推进剂。 与偏二甲肼燃烧产物只有
与偏二甲肼燃烧产物只有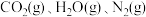 ,并放出大量热,已知
,并放出大量热,已知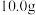 液态偏二甲肼与液态四氧化二氮完全燃烧可放出
液态偏二甲肼与液态四氧化二氮完全燃烧可放出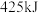 热量,该反应的热化学方程式为
热量,该反应的热化学方程式为(3)能源短缺是全球面临的问题,用
 来生产燃料甲醇的反应原理为
来生产燃料甲醇的反应原理为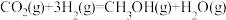 。已知某些化学键的键能数据如表所示。
。已知某些化学键的键能数据如表所示。| 化学键 |  |  | 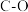 |  |  |
键能/ | 413.4 | 436.0 | 351.0 | 745.0 | 462.8 |
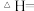
(4)氮氧化物是造成光化学烟雾和臭氧层损耗的主要气体。已知:
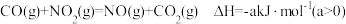
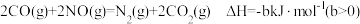
若用
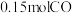 还原
还原 至
至 (
( 完全反应)的整个过程中转移电子的物质的量为
完全反应)的整个过程中转移电子的物质的量为 ,放出的热量为
,放出的热量为 (用含有a和b的代数式表示)。
(用含有a和b的代数式表示)。
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】请完成下列填空:
(1)还原剂肼( )与氧化剂
)与氧化剂 混合极易发生反应,生成气态水和氮气。已知:①使
混合极易发生反应,生成气态水和氮气。已知:①使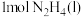 和
和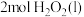 转化为
转化为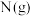 、
、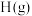 、
、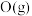 需要吸收
需要吸收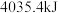 热量,破坏
热量,破坏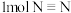 键需吸收
键需吸收 热量;②
热量;②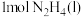 与
与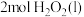 完全反应生成气态水和氮气的能量变化如图所示:
完全反应生成气态水和氮气的能量变化如图所示:

①该反应的热化学方程式为___________ 。
②断开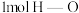 键吸收的热量为
键吸收的热量为___________  。
。
(2)25℃时,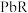 (
( 为
为 或
或 )的沉淀溶解平衡关系如图所示。
)的沉淀溶解平衡关系如图所示。
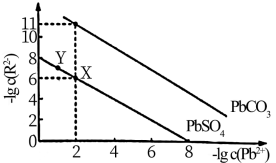
①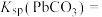
___________ 。
②向X点对应的饱和溶液中加入少量 固体,
固体,___________ (填“能”或“不能”)转化为Y点对应的溶液。
③当 和
和 沉淀共存时,溶液中
沉淀共存时,溶液中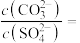
___________ 。
(1)还原剂肼(
 )与氧化剂
)与氧化剂 混合极易发生反应,生成气态水和氮气。已知:①使
混合极易发生反应,生成气态水和氮气。已知:①使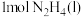 和
和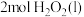 转化为
转化为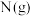 、
、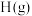 、
、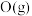 需要吸收
需要吸收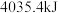 热量,破坏
热量,破坏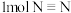 键需吸收
键需吸收 热量;②
热量;②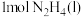 与
与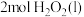 完全反应生成气态水和氮气的能量变化如图所示:
完全反应生成气态水和氮气的能量变化如图所示:
①该反应的热化学方程式为
②断开
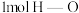 键吸收的热量为
键吸收的热量为 。
。(2)25℃时,
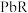 (
( 为
为 或
或 )的沉淀溶解平衡关系如图所示。
)的沉淀溶解平衡关系如图所示。
①
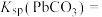
②向X点对应的饱和溶液中加入少量
 固体,
固体,③当
 和
和 沉淀共存时,溶液中
沉淀共存时,溶液中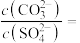
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】含硫化合物在生产、生活中有较广泛的应用。请按要求回答下列问题。
I.“保险粉”(Na2S2O4)易溶于水、难溶于乙醇,具有极强的还原性,在空气中易被氧化,在碱性介质中稳定。它的制备工艺流程如下图所示,请按要求回答下列问题。
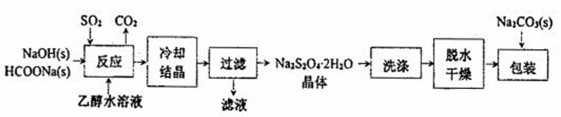
(1)“反应”在70℃条件下进行,写出发生反应的离子方程式:__________ 。
(2)在包装保存“保险粉”时加入少量的Na2CO3固体,目的是__________ 。
(3)现将10mL 0.050mol/L Na2S2O4溶液在空气中放置,其溶液的pH与时间(t)的关系如右图所示:(忽略溶液体积的变化)。
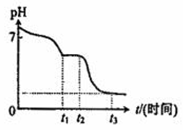
① t1~t2段溶液中S元素的化合价为____________ 。
② t3时刻后溶液的pH为__________ 。
Ⅱ.由工业制硫酸反应之一:2SO2(g)+O2(g) 2SO3(g),推测此反应的△S(填“>”或“<”)
2SO3(g),推测此反应的△S(填“>”或“<”) ______ 0,△H(填“>”或“<”)______ 0。
(l)若在绝热恒容密闭容器中,通入一定量的SO2和O2,一定条件下反应,请在如下坐标中画出从开始经一段时间正反应速率[v(正)] 随时间(t)的变化曲线图:
______
(2)若在相同条件下,分别投2molSO2(g)和1molO2(g) 于如下三容器中:
则三容器中反应分别平衡时K的大小关系是_____________ ;
SO2的平衡转化率的大小关系是____________________ 。
I.“保险粉”(Na2S2O4)易溶于水、难溶于乙醇,具有极强的还原性,在空气中易被氧化,在碱性介质中稳定。它的制备工艺流程如下图所示,请按要求回答下列问题。

(1)“反应”在70℃条件下进行,写出发生反应的离子方程式:
(2)在包装保存“保险粉”时加入少量的Na2CO3固体,目的是
(3)现将10mL 0.050mol/L Na2S2O4溶液在空气中放置,其溶液的pH与时间(t)的关系如右图所示:(忽略溶液体积的变化)。

① t1~t2段溶液中S元素的化合价为
② t3时刻后溶液的pH为
Ⅱ.由工业制硫酸反应之一:2SO2(g)+O2(g)
 2SO3(g),推测此反应的△S(填“>”或“<”)
2SO3(g),推测此反应的△S(填“>”或“<”) (l)若在绝热恒容密闭容器中,通入一定量的SO2和O2,一定条件下反应,请在如下坐标中画出从开始经一段时间正反应速率[v(正)] 随时间(t)的变化曲线图:

(2)若在相同条件下,分别投2molSO2(g)和1molO2(g) 于如下三容器中:
| 绝热恒容(2L ) 密闭容器A | 恒温(T℃)恒容(2L) 密闭容器B | 恒温(T℃)恒压 密闭容器C | |
| 平衡常数K | KA | KB | KC |
| SO2的平衡转化率 | αA | αB | αC |
则三容器中反应分别平衡时K的大小关系是
SO2的平衡转化率的大小关系是
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】I、2021 年 1 月 7 日,我国首个探明储量超千亿方的深层页岩气田——中国石化西南石油局威荣页岩气田一期项目全面建成,对促进成渝地区双城经济圈建设具有重要意义。回答下列问题:
(1)页岩气的主要成分是甲烷。已知 25℃,101kPa 时甲烷的燃烧热为 890.3 kJ·mol-1。请写出表示甲烷燃烧热的热化学方程式:_______ 。
(2)用甲烷可以合成乙烯:2CH4(g)⇌C2H4(g) + 2H2(g) ΔH=+202 kJ·mol-1,该反应在_______ 下自发进行(填“高温”、“低温”或“任何温度”)。
II、在催化剂作用下 CO2 和 H2 可直接合成乙烯:2CO2(g) + 6H2(g)⇌C2H4(g) + 4H2O(g)。
(3)关于该反应,下列叙述正确的是_______(填字母序号) 。
(4)在体积为 2 L 的恒容密闭容器中,加入 2 mol CO2 和 6 mol H2,在催化剂作用下发生乙烯直接合成反应,测得温度对 CO2 的平衡转化率影响如图所示。
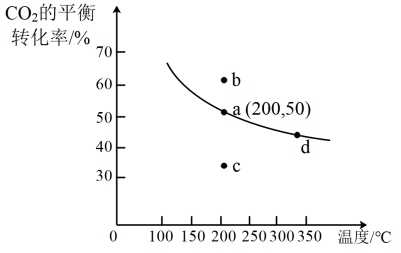
①已知在 200℃下,10 min 时反应达到平衡状态。则0~10min 内用 CO2 表示的平均反应速率为_______ 。
②该反应的 ΔH_______ 0(填 “<”、“>” 或 “=”),请结合平衡移动原理简述_______ 。
③若不使用催化剂,则 200℃ 时 CO2 的平衡转化率位于图中的_______ 点(填“a”、“b”、“c”或“d”)。
(1)页岩气的主要成分是甲烷。已知 25℃,101kPa 时甲烷的燃烧热为 890.3 kJ·mol-1。请写出表示甲烷燃烧热的热化学方程式:
(2)用甲烷可以合成乙烯:2CH4(g)⇌C2H4(g) + 2H2(g) ΔH=+202 kJ·mol-1,该反应在
II、在催化剂作用下 CO2 和 H2 可直接合成乙烯:2CO2(g) + 6H2(g)⇌C2H4(g) + 4H2O(g)。
(3)关于该反应,下列叙述正确的是_______(填字母序号) 。
| A.恒容下达平衡状态时,再充入少量氦气,正逆反应速率不变 |
| B.当混合气体的平均摩尔质量不再发生变化时,反应达平衡状态 |
| C.当反应达平衡状态时,3v正(H2) = 2v逆(H2O) |
| D.恒温下缩小容器体积,反应物转化率减小 |

①已知在 200℃下,10 min 时反应达到平衡状态。则0~10min 内用 CO2 表示的平均反应速率为
②该反应的 ΔH
③若不使用催化剂,则 200℃ 时 CO2 的平衡转化率位于图中的
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】“绿水青山就是金山银山”,研究并消除氮氧化物污染对建设美丽家乡,打造宜居环境有重要意义。
Ⅰ.已知:2NO(g)+O2(g)=2NO2(g) ΔH1=-114 kJ∙mol−1
C(s)+O2(g)=CO2(g) ΔH2=-393.5 kJ∙mol−1
N2(g)+O2(g)=2NO(g) ΔH3=+181 kJ∙mol−1
(1)若某反应的平衡常数表达式为K= ,请写出此反应的热化学方程式
,请写出此反应的热化学方程式 _________ ,该反应自发进行的条件是_________ 。(填“高温”或“低温”或“任何温度”)
Ⅱ.为避免汽车尾气中的有害气体对大气的污染,需给汽车安装尾气净化装置。在净化装置中发生反应2NO(g)+2CO(g) 2CO2(g)+N2(g) ΔH1=-746.8 kJ∙mol−1
2CO2(g)+N2(g) ΔH1=-746.8 kJ∙mol−1
(2)T℃时,将体积比为1:1的CO和NO的混合气体充入刚性容器中发生上述反应,每隔一定时间测得容器内的压强如下表所示:
①反应开始10 min内,以CO的压强变化表示该反应的平均反应速率为_________ kPa/min,该反应的平衡常数Kp=_________ kPa-1 (用分数表示,Kp为用各气体分压表示的平衡常数。)
②反应达到平衡后,若再向容器中加入2 mol CO2(g)和1 mol N2,再次达到平衡时NO的百分含量将_________ (填“增大””减小”或”不变”)。
(3)实验测得,v正=k正c2(NO)·c2(CO),v逆=k逆c(N2)·c2(CO2),k正、k逆为速率常数,只与温度有关)。
①达到平衡后,仅升高温度,k正增大的倍数_________ (填“>”“<”或“ ” ) k逆增大的倍数。
” ) k逆增大的倍数。
②若在1 L的密闭容器中充入1 mol CO和1 mol NO,在一定温度下达到平衡时,CO的转化率为40%,则
_________ 。
Ⅰ.已知:2NO(g)+O2(g)=2NO2(g) ΔH1=-114 kJ∙mol−1
C(s)+O2(g)=CO2(g) ΔH2=-393.5 kJ∙mol−1
N2(g)+O2(g)=2NO(g) ΔH3=+181 kJ∙mol−1
(1)若某反应的平衡常数表达式为K=
 ,请写出此反应的热化学方程式
,请写出此反应的热化学方程式 Ⅱ.为避免汽车尾气中的有害气体对大气的污染,需给汽车安装尾气净化装置。在净化装置中发生反应2NO(g)+2CO(g)
 2CO2(g)+N2(g) ΔH1=-746.8 kJ∙mol−1
2CO2(g)+N2(g) ΔH1=-746.8 kJ∙mol−1(2)T℃时,将体积比为1:1的CO和NO的混合气体充入刚性容器中发生上述反应,每隔一定时间测得容器内的压强如下表所示:
| 时间/min |  | 10 | 20 | 30 | 40 | 50 | 60 |
| kPa | 1.08 | 1.02 | 0.97 | 0.93 | 0.90 | 0.90 | 0.90 |
②反应达到平衡后,若再向容器中加入2 mol CO2(g)和1 mol N2,再次达到平衡时NO的百分含量将
(3)实验测得,v正=k正c2(NO)·c2(CO),v逆=k逆c(N2)·c2(CO2),k正、k逆为速率常数,只与温度有关)。
①达到平衡后,仅升高温度,k正增大的倍数
 ” ) k逆增大的倍数。
” ) k逆增大的倍数。②若在1 L的密闭容器中充入1 mol CO和1 mol NO,在一定温度下达到平衡时,CO的转化率为40%,则

您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】请完成下列问题:
Ⅰ.现代社会中,人类的一切活动都离不开能量,化学反应中,不仅有新物质的生成,而且伴随着能量的变化,同时,化学电池也成为人类生产和生活的重要能量来源之一。
(1)已知:键能是在标准状况下,将1mol气态分子AB(g)解离为气态原子A(g),B(g)所需的能量。从断键和成键的角度分析下述反应中能量的变化。部分化学键的键能如表所示:
反应2H2(g)+O2(g)=2H2O(g)生成2 mol H2O(g)可以放出热量是_______ kJ。
(2)如下图所示,是原电池的装置图。请回答下列问题:
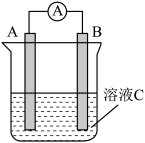
①若需将反应Cu+2Fe3+=Cu2++2Fe2+设计成如图所示的原电池装置,已知A电极为负极,则B电极反应式为_______ 。
②若用上图装置探究金属铝、镁与稀氢氧化钠(溶液C)形成的原电池反应,实验过程中电流计指针发生偏转,B极上有气泡生成,则A极发生的电极反应式是_______ 。
Ⅱ.物质的类别和核心元素的化合价是研究物质性质的两个重要角度。下图所示是硫及其部分化合物的“价类二维图”,根据图示回答下列问题:
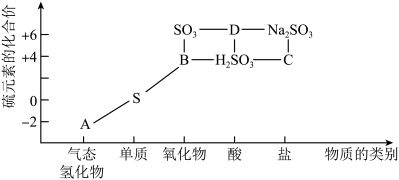
(3)足量B通入品红溶液中,溶液褪色,体现了B的_______ 性。足量B通入溴水中,溶液褪色,体现了B的_______ 性。气体A和B,不能用D的浓溶液干燥的气体是_______ (填A或B化学式)。
(4)欲制备Na2S2O3,从氧化还原角度分析,下列选项中合理的是_______(填序号)。
(5)已知:2FeSO4 Fe2O3+B↑+SO3↑,某小组为探究FeSO4的热分解反应产物,按下图装置进行实验。
Fe2O3+B↑+SO3↑,某小组为探究FeSO4的热分解反应产物,按下图装置进行实验。
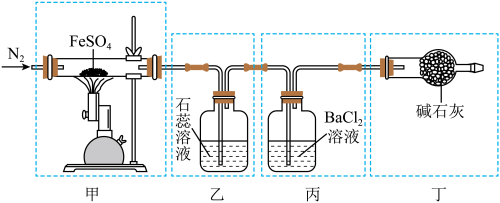
请回答下列问题:
①装置乙中的实验现象为_______ 。
②装置丙中产生白色沉淀,该白色沉淀的成分是_______ (填化学式);结合装置乙、丙的现象,能否判断分解产物中存在SO3?_______ (填“是”或“否”)。
Ⅰ.现代社会中,人类的一切活动都离不开能量,化学反应中,不仅有新物质的生成,而且伴随着能量的变化,同时,化学电池也成为人类生产和生活的重要能量来源之一。
(1)已知:键能是在标准状况下,将1mol气态分子AB(g)解离为气态原子A(g),B(g)所需的能量。从断键和成键的角度分析下述反应中能量的变化。部分化学键的键能如表所示:
| 化学键 | H—H | O=O | H—O |
| 键能(kJ/mol) | 436 | 496 | 463 |
(2)如下图所示,是原电池的装置图。请回答下列问题:

①若需将反应Cu+2Fe3+=Cu2++2Fe2+设计成如图所示的原电池装置,已知A电极为负极,则B电极反应式为
②若用上图装置探究金属铝、镁与稀氢氧化钠(溶液C)形成的原电池反应,实验过程中电流计指针发生偏转,B极上有气泡生成,则A极发生的电极反应式是
Ⅱ.物质的类别和核心元素的化合价是研究物质性质的两个重要角度。下图所示是硫及其部分化合物的“价类二维图”,根据图示回答下列问题:

(3)足量B通入品红溶液中,溶液褪色,体现了B的
(4)欲制备Na2S2O3,从氧化还原角度分析,下列选项中合理的是_______(填序号)。
| A.Na2S+S | B.Na2SO3+S |
| C.Na2SO3+Na2SO4 | D.SO2+Na2SO4 |
 Fe2O3+B↑+SO3↑,某小组为探究FeSO4的热分解反应产物,按下图装置进行实验。
Fe2O3+B↑+SO3↑,某小组为探究FeSO4的热分解反应产物,按下图装置进行实验。
请回答下列问题:
①装置乙中的实验现象为
②装置丙中产生白色沉淀,该白色沉淀的成分是
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】实验方案设计及实施
| 预期转化 | 选取试剂 | 实验现象 | 结论及化学方程式 |
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】硫代硫酸钠 (Na2S2O3)可用作分析试剂及还原剂,遇酸易分解。
Ⅰ.某化工厂生产硫代硫酸钠的流程如下:
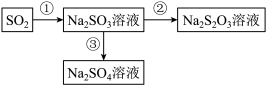
(1)为实现反应②,从氧化还原的角度分析,下列转化关系中正确的是_______(填序号)。
(2)反应①制备的 溶液易发生反应③而变质,证明
溶液易发生反应③而变质,证明 已变质的试剂为
已变质的试剂为_______ (填名称)。
Ⅱ.某学习小组利用绿矾 ( )分解生成的
)分解生成的 气体制备硫代硫酸钠,装置如图所示。
气体制备硫代硫酸钠,装置如图所示。
已知:①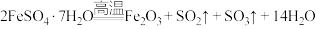
② 的沸点为
的沸点为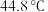 、熔点为
、熔点为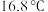 ,
, 的沸点为
的沸点为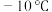 。
。
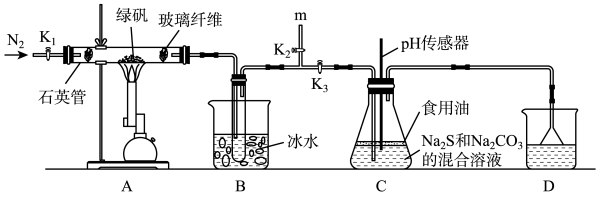
检查装置气密性后加入药品,依次进行如下操作:
①打开活塞 、
、 ,关闭活塞
,关闭活塞 ,通入一段时间
,通入一段时间 ;
;
②关闭活塞 、
、 ,打开活塞
,打开活塞 ,加热绿矾;
,加热绿矾;
③装置C中的混合溶液 约为8时停止加热;
约为8时停止加热;
④在m处连接盛有 溶液的容器,关闭活塞
溶液的容器,关闭活塞 ,_______;
,_______;
⑤从锥形瓶中得到 晶体。
晶体。
回答下列问题:
(3)补充完善步骤④_______ 。
(4)装置B中使用冰水浴的目的是_______ 。
(5)装置D中盛放的溶液可以是_______ (填序号)。
A. 溶液 B.稀氨水 C.稀
溶液 B.稀氨水 C.稀
(6)写出装置C中制备 的化学方程式
的化学方程式_______ 。
Ⅰ.某化工厂生产硫代硫酸钠的流程如下:

(1)为实现反应②,从氧化还原的角度分析,下列转化关系中正确的是_______(填序号)。
A. | B. |
C.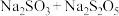 | D. |
 溶液易发生反应③而变质,证明
溶液易发生反应③而变质,证明 已变质的试剂为
已变质的试剂为Ⅱ.某学习小组利用绿矾 (
 )分解生成的
)分解生成的 气体制备硫代硫酸钠,装置如图所示。
气体制备硫代硫酸钠,装置如图所示。已知:①
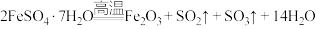
②
 的沸点为
的沸点为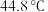 、熔点为
、熔点为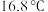 ,
, 的沸点为
的沸点为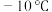 。
。
检查装置气密性后加入药品,依次进行如下操作:
①打开活塞
 、
、 ,关闭活塞
,关闭活塞 ,通入一段时间
,通入一段时间 ;
;②关闭活塞
 、
、 ,打开活塞
,打开活塞 ,加热绿矾;
,加热绿矾;③装置C中的混合溶液
 约为8时停止加热;
约为8时停止加热;④在m处连接盛有
 溶液的容器,关闭活塞
溶液的容器,关闭活塞 ,_______;
,_______;⑤从锥形瓶中得到
 晶体。
晶体。回答下列问题:
(3)补充完善步骤④
(4)装置B中使用冰水浴的目的是
(5)装置D中盛放的溶液可以是
A.
 溶液 B.稀氨水 C.稀
溶液 B.稀氨水 C.稀
(6)写出装置C中制备
 的化学方程式
的化学方程式
您最近半年使用:0次



