解题方法
1 . 依据下列热化学方程式得出的结论中,正确的是
A.已知 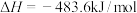 ,则氢气的燃烧热 ,则氢气的燃烧热 为 为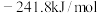 |
B.已知C(石墨,s)= C(金刚石,s)  ,则金刚石比石墨稳定 ,则金刚石比石墨稳定 |
C.已知 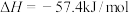 ,则含 ,则含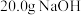 的稀溶液与稀盐酸完全中和,放出 的稀溶液与稀盐酸完全中和,放出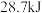 的热量 的热量 |
D.已知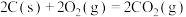  ; ;  ,则 ,则 |
您最近半年使用:0次
解题方法
2 . 一定条件下,1-苯基丙炔(Ph-C=C-CH3)可与HCl发生催化加成,反应如下:不正确 的是
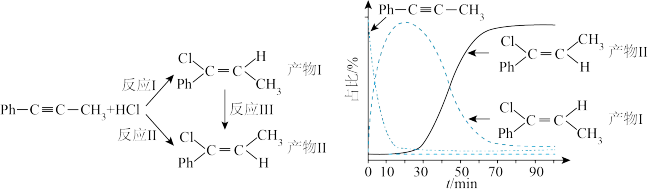
| A.反应活化能:反应I<反应Ⅱ |
| B.反应焓变:反应I<反应Ⅱ |
| C.增加HCl浓度不会改变平衡时产物Ⅱ和产物I的比例 |
| D.选择相对较短的反应时间,及时分离可获得高产率的产物Ⅰ |
您最近半年使用:0次
3 . 下列各组化学反应中,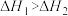 的是
的是
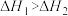 的是
的是A.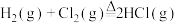  ; ;  |
B.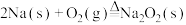  ; ;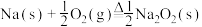  |
C.  ; ;  |
D.  ; ;  |
您最近半年使用:0次
4 . 请根据学过的知识回答下列问题:
(1)
 完全燃烧生成液态水时放出341.7kJ热量,则表示
完全燃烧生成液态水时放出341.7kJ热量,则表示 燃烧热的热化学方程
燃烧热的热化学方程___________ 。
(2)已知: 键的键能是
键的键能是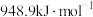 ,
, 键的键能是
键的键能是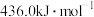 ,
, 键的键能是
键的键能是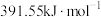 ,则
,则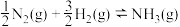

___________ 。
(3)已知:①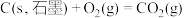

②

③

则298K时反应 的焓变:
的焓变:
___________ 。
(4)已知常温时红磷比白磷稳定,比较下列反应中 的大小:
的大小:
___________  。
。
①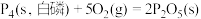

②

(5)现将一定量的稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别和
 的稀盐酸恰好完全反应,其反应热分别为
的稀盐酸恰好完全反应,其反应热分别为 、
、 、
、 ,则
,则 、
、 、
、 的大小关系为
的大小关系为___________ 。
(6)如图所示,某反应在不同条件下的反应历程分别为a、b。
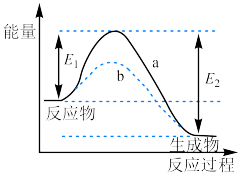
据图可判断出反应物的总键能___________ (填“>”“<”或“=”,下同)生成物的总键能,反应历程a、b的反应热___________ (填“相同”或“不相同”)。
(1)

 完全燃烧生成液态水时放出341.7kJ热量,则表示
完全燃烧生成液态水时放出341.7kJ热量,则表示 燃烧热的热化学方程
燃烧热的热化学方程(2)已知:
 键的键能是
键的键能是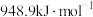 ,
, 键的键能是
键的键能是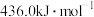 ,
, 键的键能是
键的键能是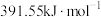 ,则
,则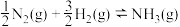

(3)已知:①
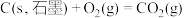

②


③


则298K时反应
 的焓变:
的焓变:
(4)已知常温时红磷比白磷稳定,比较下列反应中
 的大小:
的大小:
 。
。①
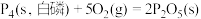

②


(5)现将一定量的稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别和

 的稀盐酸恰好完全反应,其反应热分别为
的稀盐酸恰好完全反应,其反应热分别为 、
、 、
、 ,则
,则 、
、 、
、 的大小关系为
的大小关系为(6)如图所示,某反应在不同条件下的反应历程分别为a、b。

据图可判断出反应物的总键能
您最近半年使用:0次
5 . 已知强酸的稀溶液与强碱的稀溶液发生中和反应,生成1mol水时的热效应ΔH= -57.3KJ/mol。向1L0.5mol/L NaOH溶液中分别加入:①稀醋酸 ②浓硫酸 ③稀硝酸,恰好完全反应时的热效应分别是ΔH1、ΔH2、ΔH3,其关系正确的是
| A.ΔH1>ΔH3>ΔH2 | B.ΔH1=ΔH2=ΔH3 |
| C.ΔH1<ΔH3<ΔH2 | D.ΔH1=ΔH3<ΔH2 |
您最近半年使用:0次
6 . MgCO3和CaCO3的能量关系如下图所示(M=Ca、Mg)
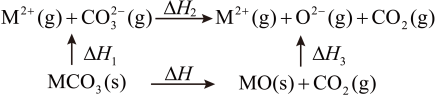
已知:离子电荷相同时,半径越小,离子键越强。下列说法正确的是
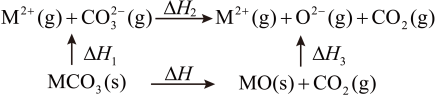
已知:离子电荷相同时,半径越小,离子键越强。下列说法正确的是
| A.△H2(CaCO3) =△H2(MgCO3) | B.△H1(MgCO3)=△H1(CaCO3) |
| C.△H=△H1+△H2+△H3 | D.△H3(CaCO3)>△H3(MgCO3)>0 |
您最近半年使用:0次
名校
解题方法
7 . 关于如下三个化学反应叙述错误的是(已知:a<0):
(1)A(g) + B(g)
B(g) C(g) ΔH1=a kJ·mol-1
C(g) ΔH1=a kJ·mol-1
(2)A(g) + B(g)
B(g)  C(l) ΔH2=b kJ·mol-1
C(l) ΔH2=b kJ·mol-1
(3)2A(g) + B(g) 2C(l) ΔH3=c kJ·mol-1
2C(l) ΔH3=c kJ·mol-1
(1)A(g) +
 B(g)
B(g) C(g) ΔH1=a kJ·mol-1
C(g) ΔH1=a kJ·mol-1 (2)A(g) +
 B(g)
B(g)  C(l) ΔH2=b kJ·mol-1
C(l) ΔH2=b kJ·mol-1 (3)2A(g) + B(g)
 2C(l) ΔH3=c kJ·mol-1
2C(l) ΔH3=c kJ·mol-1| A.c=2b | B.平衡常数K(3) =2K(2) |
| C.b<0 | D.当(1)反应放出akJ能量时,参加反应的A一定是1mol |
您最近半年使用:0次
8 . 随着能源结构的改变,甲醇将成为21世纪具有竞争力的清洁能源,工业上常利用CO或 来生产甲醇。回答下列问题:
来生产甲醇。回答下列问题:
(1)二氧化碳加氢制甲醇时,一般认为可通过如下步骤来实现:
第一步:

第二步:

① 与
与 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为___________ 。
②若第一步为慢反应,下列示意图中能体现上述反应能量变化的是___________ (填标号)。
A.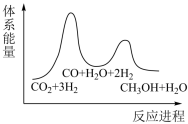 B.
B.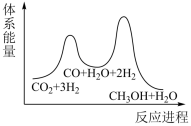 C.
C.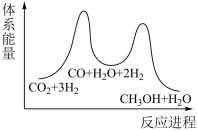 D.
D.
(2)气态甲醇用作燃料时,可发生如下两个反应:

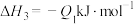

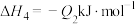
则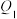
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(3)某同学设计了如下电化学装置,利用 制取甲醇。
制取甲醇。
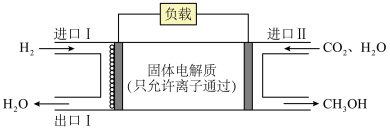
①固体电解质采用___________ (填“氧离子导体”或“质子导体”)。
②正极的电极反应式为___________ 。
(4)利用可再生能源电还原 制取甲醇的装置如下图所示,高浓度的
制取甲醇的装置如下图所示,高浓度的 用于抑制酸性电解液中的析氢反应来提高甲醇的生成率,Cu电极上发生的电极反应为
用于抑制酸性电解液中的析氢反应来提高甲醇的生成率,Cu电极上发生的电极反应为___________ ,当制得 时,标准状况下理论上阳极产生的气体体积为
时,标准状况下理论上阳极产生的气体体积为___________ 。

 来生产甲醇。回答下列问题:
来生产甲醇。回答下列问题:(1)二氧化碳加氢制甲醇时,一般认为可通过如下步骤来实现:
第一步:


第二步:


①
 与
与 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为②若第一步为慢反应,下列示意图中能体现上述反应能量变化的是
A.
 B.
B. C.
C. D.
D.
(2)气态甲醇用作燃料时,可发生如下两个反应:

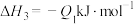

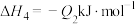
则
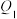
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(3)某同学设计了如下电化学装置,利用
 制取甲醇。
制取甲醇。
①固体电解质采用
②正极的电极反应式为
(4)利用可再生能源电还原
 制取甲醇的装置如下图所示,高浓度的
制取甲醇的装置如下图所示,高浓度的 用于抑制酸性电解液中的析氢反应来提高甲醇的生成率,Cu电极上发生的电极反应为
用于抑制酸性电解液中的析氢反应来提高甲醇的生成率,Cu电极上发生的电极反应为 时,标准状况下理论上阳极产生的气体体积为
时,标准状况下理论上阳极产生的气体体积为
您最近半年使用:0次
2024-02-14更新
|
77次组卷
|
2卷引用:山东省泰安第一中学2023-2024学年高二上学期12月月考化学试题
9 . 下列有关热化学方程式的叙述正确的是
A.已知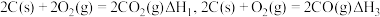 ,则 ,则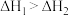 |
B. ,则 ,则 的燃烧热 的燃烧热 |
C.已知正丁烷(g)→异丁烷(g) ,则异丁烷比正丁烷稳定 ,则异丁烷比正丁烷稳定 |
D. 和 和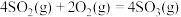 的 的 相等 相等 |
您最近半年使用:0次
10 . 下列图像分别表示有关反应的反应过程与能量变化的关系:

据此判断下列说法正确的是

据此判断下列说法正确的是
| A.石墨转变为金刚石是吸热反应 |
| B.白磷比红磷稳定 |
| C.CO(g)+H2O(g)=CO2(g)+H2(g)ΔH>0 |
| D.S(g)+O2(g)=SO2(g)ΔH1;S(s)+O2(g)=SO2(g)ΔH2,则ΔH1>ΔH2 |
您最近半年使用:0次



