名校
1 . 钛酸钡( )具有高介电常数和低介电损耗,是电子陶瓷中使用最广泛的材料之一,被誉为“电子陶瓷工业的支柱”。一种超细微
)具有高介电常数和低介电损耗,是电子陶瓷中使用最广泛的材料之一,被誉为“电子陶瓷工业的支柱”。一种超细微 粉末的制备方法如下。
粉末的制备方法如下。
 )具有高介电常数和低介电损耗,是电子陶瓷中使用最广泛的材料之一,被誉为“电子陶瓷工业的支柱”。一种超细微
)具有高介电常数和低介电损耗,是电子陶瓷中使用最广泛的材料之一,被誉为“电子陶瓷工业的支柱”。一种超细微 粉末的制备方法如下。
粉末的制备方法如下。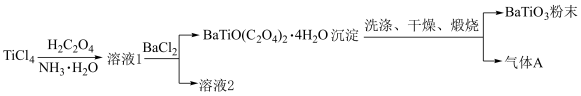
A.可用硝酸酸化的 溶液检验洗涤是否完全 溶液检验洗涤是否完全 |
| B.用溶液2提取的一种副产物可作肥料 |
| C.流程中的三步反应均为非氧化还原反应 |
D.向 中先加入 中先加入 后加入 后加入 的目的是防止 的目的是防止 水解 水解 |
您最近半年使用:0次
2 . Ⅰ.按要求回答下列问题:
(1)下列变化中属于吸热反应的是___________ 。
①铝片与稀盐酸的反应 ②将胆矾加热变为白色粉末 ③干冰汽化
④氯酸钾分解制氧气 ⑤甲烷在氧气中的燃烧反应 ⑥ 与盐酸的反应
与盐酸的反应
(2)反应 在一个容积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
在一个容积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是___________ 。
①增加 的量
的量
②将容器的体积缩小一半
③保持体积不变,充入 使体系压强增大
使体系压强增大
④保持压强不变,充入 使容器体积变大
使容器体积变大
Ⅱ.在体积为 的密闭容器中,充入
的密闭容器中,充入 和
和 ,一定条件下反应:
,一定条件下反应: ,测得
,测得 和
和 的浓度随时间变化如图:
的浓度随时间变化如图:
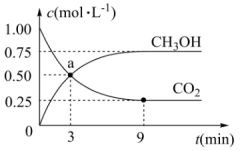
(3)从3min到9min,v(CO2)=___________ (结果保留两位有效数字);a点时v(正)___________ v(逆)(填>、<或=);
Ⅲ.某研究小组在实验室用硫化碱法制备 ,实验装置如图:
,实验装置如图:
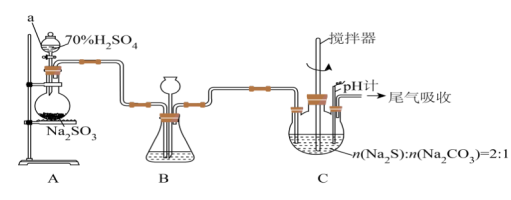
(4)装置 的作用是
的作用是___________ 。
(5)配制 溶液时,常加入少量
溶液时,常加入少量___________ 以防止出现浑浊和 的逸出。
的逸出。
(6)为了提高 的吸收效率,在不改变装置
的吸收效率,在不改变装置 中的溶液浓度、体积的条件下,还可采取的合理措施是
中的溶液浓度、体积的条件下,还可采取的合理措施是___________ (填序号)。
a.适当加快搅拌速率 b.加快 的流速 c.增大
的流速 c.增大 的接触面积
的接触面积
(1)下列变化中属于吸热反应的是
①铝片与稀盐酸的反应 ②将胆矾加热变为白色粉末 ③干冰汽化
④氯酸钾分解制氧气 ⑤甲烷在氧气中的燃烧反应 ⑥
 与盐酸的反应
与盐酸的反应(2)反应
 在一个容积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
在一个容积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是①增加
 的量
的量②将容器的体积缩小一半
③保持体积不变,充入
 使体系压强增大
使体系压强增大④保持压强不变,充入
 使容器体积变大
使容器体积变大Ⅱ.在体积为
 的密闭容器中,充入
的密闭容器中,充入 和
和 ,一定条件下反应:
,一定条件下反应: ,测得
,测得 和
和 的浓度随时间变化如图:
的浓度随时间变化如图:
(3)从3min到9min,v(CO2)=
Ⅲ.某研究小组在实验室用硫化碱法制备
 ,实验装置如图:
,实验装置如图:
(4)装置
 的作用是
的作用是(5)配制
 溶液时,常加入少量
溶液时,常加入少量 的逸出。
的逸出。(6)为了提高
 的吸收效率,在不改变装置
的吸收效率,在不改变装置 中的溶液浓度、体积的条件下,还可采取的合理措施是
中的溶液浓度、体积的条件下,还可采取的合理措施是a.适当加快搅拌速率 b.加快
 的流速 c.增大
的流速 c.增大 的接触面积
的接触面积
您最近半年使用:0次
解题方法
3 . 二氧化锗常用作有机反应的催化剂以及制备半导体的原料。某大型化工厂提纯二氧化锗废料(主要含GeO2、AS2O3)的工艺如图,下列有关说法正确的是
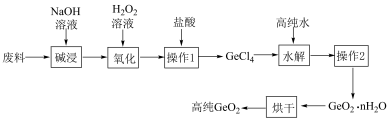
已知:①GeO2与碱反应生成Na2GeO3;AS2O3与碱反应生成NaASO2;
②GeCl4的熔点−49.5℃,沸点为85℃,极易发生水解

已知:①GeO2与碱反应生成Na2GeO3;AS2O3与碱反应生成NaASO2;
②GeCl4的熔点−49.5℃,沸点为85℃,极易发生水解
| A.Ge在周期表中位于第四周期第ⅥA族 |
B.“氧化”时,离子反应为ASO +H2O2+2OH-=ASO +H2O2+2OH-=ASO +2H2O +2H2O |
| C.“操作1”是蒸馏,“操作2”所用仪器主要为玻璃棒、漏斗、烧杯 |
| D.“操作1”加入的盐酸为7mol/L,若改成1mol/L可节省原料同时不影响产率 |
您最近半年使用:0次
4 . Ⅰ.
(1) 的水溶液呈
的水溶液呈_____ (填“酸”、“中”、“碱”)性,常温时的
_____ 7(填“>”“=”、“<”),实验室在配制 的溶液时,常将
的溶液时,常将 固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的浓度,以
固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的浓度,以_____ (填“促进”、“抑制”)其水解。
Ⅱ.常温下有浓度均为 的四种溶液:①
的四种溶液:① 、②
、② 、③HCl、④
、③HCl、④ 。
。
(2)有人称溶液①是油污的“清道夫”,原因是_____ (用离子方程式解释)。
(3)溶液②中,
_____  。
。
(4)将10mL溶液③加水稀释至100mL,则此时溶液中由水电离出的
_____ 。
(5)取④的溶液 ,向其中加入含
,向其中加入含 的溶液后呈中性,则
的溶液后呈中性,则 电离平衡常数
电离平衡常数
_____ 。
(1)
 的水溶液呈
的水溶液呈
 的溶液时,常将
的溶液时,常将 固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的浓度,以
固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的浓度,以Ⅱ.常温下有浓度均为
 的四种溶液:①
的四种溶液:① 、②
、② 、③HCl、④
、③HCl、④ 。
。(2)有人称溶液①是油污的“清道夫”,原因是
(3)溶液②中,

 。
。(4)将10mL溶液③加水稀释至100mL,则此时溶液中由水电离出的

(5)取④的溶液
 ,向其中加入含
,向其中加入含 的溶液后呈中性,则
的溶液后呈中性,则 电离平衡常数
电离平衡常数
您最近半年使用:0次
5 . 下列试题中,溶液温度均为常温,请回答:
(1)0.1mol/L的醋酸钠溶液pH=10的原因是
(2)0.1mol/L的NaCN溶液中各离子浓度由大到小的顺序是
(3)浓度均为0.1mol·L-1的V1LHCl溶液和V2LNaOH溶液混合后,混合溶液的pH=12,则V1:V2=
(4)CH3COONa和CH3COOH的混合溶液中c(Na+)=c(CH3COO-),则该溶液呈
(5)在日常生活中经常用硫酸铝和碳酸氢钠混合溶液作灭火剂,请用离子方程式表示其灭火原理:
(6)物质的量浓度均为0.1mol·L-1的4种溶液:①NH3·H2O、②NH4HSO4、③CH3COONH4、④NH4Cl,按要求从大到小按序号排序,c(
 ):
):
您最近半年使用:0次
6 . 某研究小组设计了如下流程以废铁屑(含有少量碳和 杂质)为原料制备无水
杂质)为原料制备无水 。已知:氯化亚砜(
。已知:氯化亚砜( )熔点
)熔点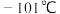 ,沸点
,沸点 ,易水解。
,易水解。
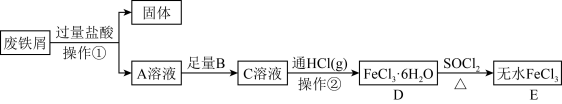
(1)为避免引入新的杂质,试剂 可以选用_________________(填编号)。
可以选用_________________(填编号)。
(2)操作②是蒸发结晶,加热的同时通入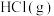 的目的是
的目的是_________________ 。
(3)取少量 晶体,溶于水并滴加
晶体,溶于水并滴加 溶液,现象是
溶液,现象是_________________ 。
(4)反应 的化学方程式为
的化学方程式为_________________ 。
(5)由 转化成
转化成 的过程中可能产生少量亚铁盐,写出一种可能的还原剂
的过程中可能产生少量亚铁盐,写出一种可能的还原剂_________________ ,并设计实验验证是该还原剂将 还原
还原_________________ 。
 杂质)为原料制备无水
杂质)为原料制备无水 。已知:氯化亚砜(
。已知:氯化亚砜( )熔点
)熔点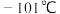 ,沸点
,沸点 ,易水解。
,易水解。
(1)为避免引入新的杂质,试剂
 可以选用_________________(填编号)。
可以选用_________________(填编号)。A. 溶液 溶液 | B.氯水 | C.溴水 | D. 溶液 溶液 |
(2)操作②是蒸发结晶,加热的同时通入
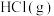 的目的是
的目的是(3)取少量
 晶体,溶于水并滴加
晶体,溶于水并滴加 溶液,现象是
溶液,现象是(4)反应
 的化学方程式为
的化学方程式为(5)由
 转化成
转化成 的过程中可能产生少量亚铁盐,写出一种可能的还原剂
的过程中可能产生少量亚铁盐,写出一种可能的还原剂 还原
还原
您最近半年使用:0次
7 . 向三份0.1mol/L  溶液中分别加入少量
溶液中分别加入少量 、
、 、
、 固体(忽略溶液体积变化),则
固体(忽略溶液体积变化),则 浓度的变化依次为
浓度的变化依次为
 溶液中分别加入少量
溶液中分别加入少量 、
、 、
、 固体(忽略溶液体积变化),则
固体(忽略溶液体积变化),则 浓度的变化依次为
浓度的变化依次为| A.减小、增大、减小 | B.增大、减小、减小 |
| C.减小、增大、增大 | D.增大、减小、增大 |
您最近半年使用:0次
名校
8 . 无水氯化铁,在空气中极易潮解,加热易升华,常应用于金属蚀刻和污水处理。某化学兴趣小组设计如下实验制备无水氯化铁,并进行其性质探究。回答下列问题:
I.无水氯化铁的制备
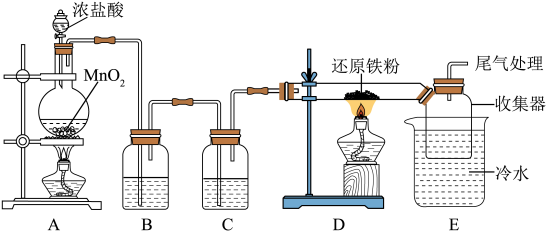
(1)盛装浓盐酸的仪器名称是_______ ,装置B中盛装的药品是_______ ,装置C的作用是_______ 。
(2)装置D中发生反应的化学方程式为_______ 。
(3)装置D、E之间用大口径玻璃管连接的原因是_______ 。
Ⅱ.氯化铁性质探究
(4)取收集器中固体配制成 溶液。所需的玻璃仪器主要有量筒、玻璃棒、烧杯、胶头滴管和
溶液。所需的玻璃仪器主要有量筒、玻璃棒、烧杯、胶头滴管和_______ 配制溶液时,应先将氯化铁固体溶于较浓的盐酸中,盐酸的作用是_______ 。
(5)向甲、乙两支试管中分别加入 溶液,向甲试管中滴加
溶液,向甲试管中滴加 溶液,试管中溶液由黄色变为红褐色,并有沉淀生成,振荡后沉淀消失,继续滴加
溶液,试管中溶液由黄色变为红褐色,并有沉淀生成,振荡后沉淀消失,继续滴加 溶液,溶液颜色加深,放置一小时后溶液变为绿色。向乙试管中滴加
溶液,溶液颜色加深,放置一小时后溶液变为绿色。向乙试管中滴加 溶液,试管中溶液由黄色变为红褐色,没有沉淀生成,继续滴加
溶液,试管中溶液由黄色变为红褐色,没有沉淀生成,继续滴加 溶液,溶液颜色加深,放置一小时后溶液变为绿色。
溶液,溶液颜色加深,放置一小时后溶液变为绿色。
①甲试管中产生沉淀的化学式为_______ ,利用平衡移动原理解释产生该沉淀的原因:_______ 。
②甲、乙两支试管中最终溶液都变为绿色,发生反应的离子方程式为_______ 。
I.无水氯化铁的制备

(1)盛装浓盐酸的仪器名称是
(2)装置D中发生反应的化学方程式为
(3)装置D、E之间用大口径玻璃管连接的原因是
Ⅱ.氯化铁性质探究
(4)取收集器中固体配制成
 溶液。所需的玻璃仪器主要有量筒、玻璃棒、烧杯、胶头滴管和
溶液。所需的玻璃仪器主要有量筒、玻璃棒、烧杯、胶头滴管和(5)向甲、乙两支试管中分别加入
 溶液,向甲试管中滴加
溶液,向甲试管中滴加 溶液,试管中溶液由黄色变为红褐色,并有沉淀生成,振荡后沉淀消失,继续滴加
溶液,试管中溶液由黄色变为红褐色,并有沉淀生成,振荡后沉淀消失,继续滴加 溶液,溶液颜色加深,放置一小时后溶液变为绿色。向乙试管中滴加
溶液,溶液颜色加深,放置一小时后溶液变为绿色。向乙试管中滴加 溶液,试管中溶液由黄色变为红褐色,没有沉淀生成,继续滴加
溶液,试管中溶液由黄色变为红褐色,没有沉淀生成,继续滴加 溶液,溶液颜色加深,放置一小时后溶液变为绿色。
溶液,溶液颜色加深,放置一小时后溶液变为绿色。①甲试管中产生沉淀的化学式为
②甲、乙两支试管中最终溶液都变为绿色,发生反应的离子方程式为
您最近半年使用:0次
2024-03-02更新
|
97次组卷
|
2卷引用:湖北省恩施州高中教育联盟2023-2024学年高二上学期期末考试化学试题
名校
解题方法
9 . 已知 、
、 、
、 、
、 、
、 分别表示弱酸的电离平衡常数、弱碱的电离平衡常数,水的离子积常数、盐的水解平衡常数、难溶电解质的溶度积常数。通过查阅资料获得温度为
分别表示弱酸的电离平衡常数、弱碱的电离平衡常数,水的离子积常数、盐的水解平衡常数、难溶电解质的溶度积常数。通过查阅资料获得温度为 时以下数据:
时以下数据: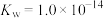 ,
, ,
,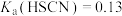 ,
, ,
,
(1)有关上述常数的说法正确的是___________ 。
a.它们都能反映一定条件下对应变化进行的程度
b.所有弱电解质的电离常数和难溶电解质的 都随温度的升高而增大
都随温度的升高而增大
c.常温下, 在水中的
在水中的 大于在饱和
大于在饱和 溶液中的
溶液中的
d.一定温度下,在 溶液中,
溶液中,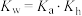
(2) 时,将浓度相等的
时,将浓度相等的 与
与 溶液等体积混合,判断溶液呈
溶液等体积混合,判断溶液呈___________ (填“酸”、“碱”或“中”)性。
(3)已知 溶液为中性,又知
溶液为中性,又知 溶液加到
溶液加到 溶液中有气体放出,现有
溶液中有气体放出,现有 时等浓度的四种溶液:A.
时等浓度的四种溶液:A.  ,B.
,B. ,C.
,C. ,D.
,D. 。
。
回答下列问题:
①试推断 溶液的
溶液的
___________ 7(填“>”、“<”或“=”)
②将四种溶液按 浓度由大到小的顺序排列是:
浓度由大到小的顺序排列是:___________ (用字母排序)。
(4)为探究 在酸中的溶解性,利用以上数据可以计算出反应:
在酸中的溶解性,利用以上数据可以计算出反应: 在
在 时的平衡常数
时的平衡常数
___________ ,并据此推断 是否能溶解于醋酸,并简要说明原因。(已知
是否能溶解于醋酸,并简要说明原因。(已知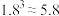 )
)___________ 。
 、
、 、
、 、
、 、
、 分别表示弱酸的电离平衡常数、弱碱的电离平衡常数,水的离子积常数、盐的水解平衡常数、难溶电解质的溶度积常数。通过查阅资料获得温度为
分别表示弱酸的电离平衡常数、弱碱的电离平衡常数,水的离子积常数、盐的水解平衡常数、难溶电解质的溶度积常数。通过查阅资料获得温度为 时以下数据:
时以下数据: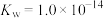 ,
, ,
,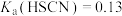 ,
, ,
,
(1)有关上述常数的说法正确的是
a.它们都能反映一定条件下对应变化进行的程度
b.所有弱电解质的电离常数和难溶电解质的
 都随温度的升高而增大
都随温度的升高而增大c.常温下,
 在水中的
在水中的 大于在饱和
大于在饱和 溶液中的
溶液中的
d.一定温度下,在
 溶液中,
溶液中,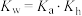
(2)
 时,将浓度相等的
时,将浓度相等的 与
与 溶液等体积混合,判断溶液呈
溶液等体积混合,判断溶液呈(3)已知
 溶液为中性,又知
溶液为中性,又知 溶液加到
溶液加到 溶液中有气体放出,现有
溶液中有气体放出,现有 时等浓度的四种溶液:A.
时等浓度的四种溶液:A.  ,B.
,B. ,C.
,C. ,D.
,D. 。
。回答下列问题:
①试推断
 溶液的
溶液的
②将四种溶液按
 浓度由大到小的顺序排列是:
浓度由大到小的顺序排列是:(4)为探究
 在酸中的溶解性,利用以上数据可以计算出反应:
在酸中的溶解性,利用以上数据可以计算出反应: 在
在 时的平衡常数
时的平衡常数
 是否能溶解于醋酸,并简要说明原因。(已知
是否能溶解于醋酸,并简要说明原因。(已知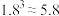 )
)
您最近半年使用:0次
名校
10 . 关于下列常温下的水溶液的说法正确的是
A.向水中加入 溶液仍显中性,水的电离平衡不移动 溶液仍显中性,水的电离平衡不移动 |
B.加水稀释亚硫酸( )溶液, )溶液, 始终不变 始终不变 |
| C.将pH=3的醋酸与pH=11的NaOH溶液等体积混合后溶液呈中性 |
D.相同 的溶质的物质的量浓度: 的溶质的物质的量浓度: |
您最近半年使用:0次
2024-02-01更新
|
194次组卷
|
3卷引用:山东省德州市2023-2024学年高二上学期期末考试化学试题



