名校
解题方法
1 . 人们常常利用化学反应中的能量变化为人类服务。
(1)氢能是一种具有发展前景的理想清洁能源,氢气燃烧时放出大量的热。氢气燃烧生成水蒸气的能量变化如下图所示: 完全燃烧生成1 mol
完全燃烧生成1 mol 时,释放的能量是
时,释放的能量是______ kJ。
(2)下列化学反应在理论上可以设计成原电池的是______。
(3)下图是某兴趣小组设计的原电池示意图:_____________ 。
②将稀 换成
换成 溶液,电极质量增加的是
溶液,电极质量增加的是______ (填“锌极”或“铜极”,下同),溶液中 移向
移向______ 。
(1)氢能是一种具有发展前景的理想清洁能源,氢气燃烧时放出大量的热。氢气燃烧生成水蒸气的能量变化如下图所示:
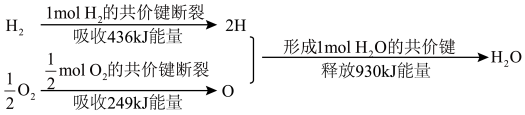
 完全燃烧生成1 mol
完全燃烧生成1 mol 时,释放的能量是
时,释放的能量是(2)下列化学反应在理论上可以设计成原电池的是______。
A.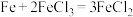 | B. |
C.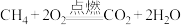 | D.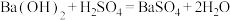 |
(3)下图是某兴趣小组设计的原电池示意图:
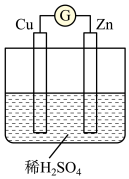
②将稀
 换成
换成 溶液,电极质量增加的是
溶液,电极质量增加的是 移向
移向
您最近半年使用:0次
名校
解题方法
2 . 过二硫酸钾( )具有强氧化性,常用于水池及封闭循环处理水中有害物质的氧化降解。请回答下列问题:
)具有强氧化性,常用于水池及封闭循环处理水中有害物质的氧化降解。请回答下列问题:
Ⅰ. 中含有过氧键,与过氧化氢相似,可以和
中含有过氧键,与过氧化氢相似,可以和 发生氧化还原反应,由此构成原电池装置(质子交换膜只允许
发生氧化还原反应,由此构成原电池装置(质子交换膜只允许 通过),如图。
通过),如图。______ (填“a”或“b”)极,b极的电极反应式为______________________ 。
(2)下列关于a,b极的电极材料合理的是________ (填标号)。
Ⅱ.制备过二硫酸钾( )。
)。
往 溶液中加入硫酸及硫酸钾粉末,搅拌,常温下反应半小时,然后在搅拌下使物料冷却至14℃,
溶液中加入硫酸及硫酸钾粉末,搅拌,常温下反应半小时,然后在搅拌下使物料冷却至14℃, 以结晶析出,溶液中含有硫酸氢盐。
以结晶析出,溶液中含有硫酸氢盐。
(3)制备 的化学方程式为
的化学方程式为_____________________ 。
Ⅲ.产品提纯。
在450mL 0.5 KOH水溶液中,边搅拌边加入
KOH水溶液中,边搅拌边加入 粗产品,缓慢加热到70℃,待结晶完全溶解后,冷却到14℃,使
粗产品,缓慢加热到70℃,待结晶完全溶解后,冷却到14℃,使 重新结晶,再在90~95℃下气流干燥,即得成品。
重新结晶,再在90~95℃下气流干燥,即得成品。
(4)现用KOH固体配制上述KOH水溶液,需称量_________ g KOH固体,所需仪器如图所示,其中不需要的仪器是________________ (填标号),还缺少的仪器为_______________________ (写仪器名称)。 (
( )含量测定。
)含量测定。
取a g样品全部溶解在烧杯中,加入20.00mL 0.1
 溶液,恰好完全反应。
溶液,恰好完全反应。
(5)反应生成 写出该反应的离子方程式:
写出该反应的离子方程式:________________ 。
(6)此样品中 的质量分数为
的质量分数为________________ 。
 )具有强氧化性,常用于水池及封闭循环处理水中有害物质的氧化降解。请回答下列问题:
)具有强氧化性,常用于水池及封闭循环处理水中有害物质的氧化降解。请回答下列问题:Ⅰ.
 中含有过氧键,与过氧化氢相似,可以和
中含有过氧键,与过氧化氢相似,可以和 发生氧化还原反应,由此构成原电池装置(质子交换膜只允许
发生氧化还原反应,由此构成原电池装置(质子交换膜只允许 通过),如图。
通过),如图。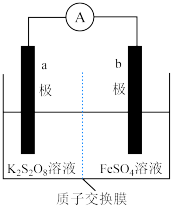
(2)下列关于a,b极的电极材料合理的是
选项 | a极 | b极 |
A | Pt | Pt |
B | 石墨 | 石墨 |
C | 石墨 | Zn |
D | Al | Cu |
Ⅱ.制备过二硫酸钾(
 )。
)。往
 溶液中加入硫酸及硫酸钾粉末,搅拌,常温下反应半小时,然后在搅拌下使物料冷却至14℃,
溶液中加入硫酸及硫酸钾粉末,搅拌,常温下反应半小时,然后在搅拌下使物料冷却至14℃, 以结晶析出,溶液中含有硫酸氢盐。
以结晶析出,溶液中含有硫酸氢盐。(3)制备
 的化学方程式为
的化学方程式为Ⅲ.产品提纯。
在450mL 0.5
 KOH水溶液中,边搅拌边加入
KOH水溶液中,边搅拌边加入 粗产品,缓慢加热到70℃,待结晶完全溶解后,冷却到14℃,使
粗产品,缓慢加热到70℃,待结晶完全溶解后,冷却到14℃,使 重新结晶,再在90~95℃下气流干燥,即得成品。
重新结晶,再在90~95℃下气流干燥,即得成品。(4)现用KOH固体配制上述KOH水溶液,需称量

 (
( )含量测定。
)含量测定。取a g样品全部溶解在烧杯中,加入20.00mL 0.1

 溶液,恰好完全反应。
溶液,恰好完全反应。(5)反应生成
 写出该反应的离子方程式:
写出该反应的离子方程式:(6)此样品中
 的质量分数为
的质量分数为
您最近半年使用:0次
名校
解题方法
3 . 钠基—海水电池因其具有环境友好、能量密度高和海水储量丰富且易得等优势,有望成为新一代储能器件,其工作原理如图所示。下列说法正确的是
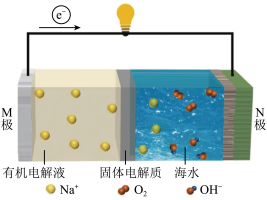
| A.M极为正极,发生还原反应 | B.放电时, 由左室移至海水中 由左室移至海水中 |
C.N极发生的电极反应为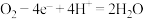 | D.可以将有机电解液换为低成本的钠盐水溶液 |
您最近半年使用:0次
4 . 设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.常温常压下,18g  中含有的电子数为9 中含有的电子数为9 |
B.将2.24L  通入足量水中,得到的 通入足量水中,得到的 分子数为0.1 分子数为0.1 |
C.1mol  与足量 与足量 在一定条件下反应,生成的 在一定条件下反应,生成的 分子数为NA 分子数为NA |
D.以稀硫酸为电解液的锌铜原电池中,每转移0.2 个电子,负极质量减少6.4g 个电子,负极质量减少6.4g |
您最近半年使用:0次
名校
5 . 13g锌粒与足量2 稀硫酸反应生成
稀硫酸反应生成 ,下列措施可以加快反应速率,但减少
,下列措施可以加快反应速率,但减少 的最终生成量的是
的最终生成量的是
 稀硫酸反应生成
稀硫酸反应生成 ,下列措施可以加快反应速率,但减少
,下列措施可以加快反应速率,但减少 的最终生成量的是
的最终生成量的是| A.将锌粒换成等质量的锌粉 | B.向稀硫酸中加入少量 固体 固体 |
C.向稀硫酸中加入少量 溶液 溶液 | D.将该稀硫酸换成足量0.5 稀硫酸 稀硫酸 |
您最近半年使用:0次
名校
解题方法
6 . 下列反应在理论上可以设计为原电池的是
A. | B.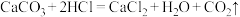 |
C. | D.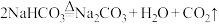 |
您最近半年使用:0次
解题方法
7 . 海泥细菌通过消耗海底沉积层中的有机物获得营养,同时产生电子。科学家利用这一原理设计了海泥细菌电池,该技术可在海底加速石油污染物降解速率,其中海泥代谢产物显酸性,电池工作原理如图所示。下列说法错误的是

| A.电子从B电极流向A电极 |
B.工作时B电极附近溶液 减小 减小 |
C.负极的电极反应式为: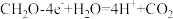 |
D.A电极消耗标况下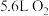 ,有 ,有 质子从海底沉积层进入海水层 质子从海底沉积层进入海水层 |
您最近半年使用:0次
名校
8 . CO2/HCOOH循环在氢能的贮存/释放、燃料电池等方面具有重要应用。
(1)CO2催化加氢。在密闭容器中,向含有催化剂的KHCO3溶液(CO2与KOH溶液反应制得)中通入H2生成HCOO−,其离子方程式为_______ ;其他条件不变, 转化为HCOO−的转化率随温度的变化如图所示。反应温度在40℃~80℃范围内,
转化为HCOO−的转化率随温度的变化如图所示。反应温度在40℃~80℃范围内, 催化加氢的转化率迅速上升,其主要原因是
催化加氢的转化率迅速上升,其主要原因是_______ 。_______ ;放电过程中需补充的物质A为_______ (填化学式)。
②图中所示的HCOOH燃料电池放电的本质是通过HCOOH与O2的反应,将化学能转化为电能,其反应的离子方程式为_______ 。
(3)HCOOH催化释氢。在催化剂作用下,HCOOH分解生成CO2和H2可能的反应机理如图所示。_______ (填化学式)。
②研究发现:其他条件不变时,以HCOOK溶液代替HCOOH催化释氢的效果更佳,其具体优点是提高释放氢气的速率,提高释放出氢气的纯度,请分析原因_______ 。
(1)CO2催化加氢。在密闭容器中,向含有催化剂的KHCO3溶液(CO2与KOH溶液反应制得)中通入H2生成HCOO−,其离子方程式为
 转化为HCOO−的转化率随温度的变化如图所示。反应温度在40℃~80℃范围内,
转化为HCOO−的转化率随温度的变化如图所示。反应温度在40℃~80℃范围内, 催化加氢的转化率迅速上升,其主要原因是
催化加氢的转化率迅速上升,其主要原因是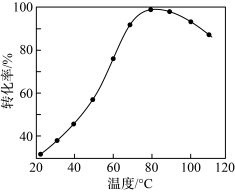
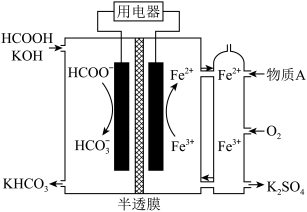
②图中所示的HCOOH燃料电池放电的本质是通过HCOOH与O2的反应,将化学能转化为电能,其反应的离子方程式为
(3)HCOOH催化释氢。在催化剂作用下,HCOOH分解生成CO2和H2可能的反应机理如图所示。
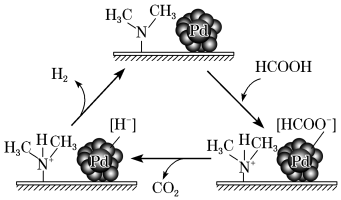
②研究发现:其他条件不变时,以HCOOK溶液代替HCOOH催化释氢的效果更佳,其具体优点是提高释放氢气的速率,提高释放出氢气的纯度,请分析原因
您最近半年使用:0次
名校
解题方法
9 . 下列各组材料组成如图装置,能形成原电池且M做正极的是
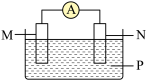
| 选项 | M | N | P |
| A | Zn | Cu | 稀硫酸 |
| B | Ag | Zn | 蔗糖溶液 |
| C | Ag | Fe |  溶液 溶液 |
| D | Al | Mg | NaOH溶液 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
10 . 热电厂尾气经处理得到较纯的 ,可用于原电池法生产硫酸,其工作原理如图所示。电池工作时,下列说法不正确的是
,可用于原电池法生产硫酸,其工作原理如图所示。电池工作时,下列说法不正确的是
 ,可用于原电池法生产硫酸,其工作原理如图所示。电池工作时,下列说法不正确的是
,可用于原电池法生产硫酸,其工作原理如图所示。电池工作时,下列说法不正确的是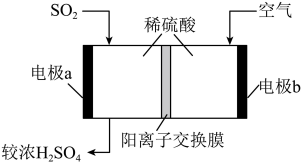
A.电极 为正极 为正极 |
B. 极消耗 极消耗 与 与 极消耗 极消耗 两者物质的量相等 两者物质的量相等 |
C.溶液中 极区向 极区向 极区迁移 极区迁移 |
D.电极 的电极反应式: 的电极反应式: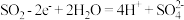 |
您最近半年使用:0次



