1 . 短周期元素A、B、C、D的原子序数依次增大,基态A原子核外电子占据3个轨道,基态B原子核外电子占据3个能级且每个能级上电子数相等,C的双原子单质分子中σ键和π键数目之比为1∶2,D的最高化合价和最低化合价代数和等于4。
(1)基态B原子的价电子排布图 为______________ ;基态D原子核外电子占据最高能级的电子云轮廓图为_____________ 形。
(2)氯元素与A、B、C元素组成的共价分子ACl3、BCl4、CCl3中,中心原子采用sp2杂化、空间结构为平面三角形的是_________ (填分子式,下同),属于极性分子的是_________ ,键角由大到小的顺序为_____________ 。
(3)(DC)4为热色性固体,且有色温效应,其颜色在低于-30℃时为淡黄色,室温下为橙黄色,高于100℃时为深红色。(DC)4属于_______ 晶体,在淡黄色→橙黄色→深红色的转化中,破坏的作用力是___________ ;在常压下,(DC)4高于130℃分解为相应的单质,这一变化中破坏的作用力是_________ 。
(4)A、C形成立方晶体,晶体结构类似于金刚石,如图所示(白色球代表A原子,黑色球代表C原子)。已知:该晶体边长为a nm,NA代表阿伏加德罗常数的值。_______________ ,晶体性脆的原因是_______________ 。
②该晶体的密度为_____________ g·cm-3(不必化简)。
(1)基态B原子的
(2)氯元素与A、B、C元素组成的共价分子ACl3、BCl4、CCl3中,中心原子采用sp2杂化、空间结构为平面三角形的是
(3)(DC)4为热色性固体,且有色温效应,其颜色在低于-30℃时为淡黄色,室温下为橙黄色,高于100℃时为深红色。(DC)4属于
(4)A、C形成立方晶体,晶体结构类似于金刚石,如图所示(白色球代表A原子,黑色球代表C原子)。已知:该晶体边长为a nm,NA代表阿伏加德罗常数的值。

②该晶体的密度为
您最近半年使用:0次
2 . 下列说法正确的是
| A.1 mol N2分子中的π键与1 mol CO2分子中的π键的数目之比为2∶1 |
| B.键能:甲烷(C-C)<乙烯(C=C) |
| C.强度:氢键>化学键>范德华力 |
D.沸点: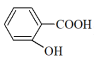 > >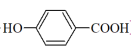 |
您最近半年使用:0次
3 . 下列说法正确的是
| A.H2O是含有极性键的非极性分子 |
B.SO3与SO 均为平面三角形 均为平面三角形 |
C.SO 中S原子为sp3杂化 中S原子为sp3杂化 |
| D.H2S稳定性小于H2O,是因为其分子间不存在氢键 |
您最近半年使用:0次
4 . 下列现象不能用“相似相溶”规律解释的是
| A.甲烷难溶于水 | B.氯气易溶于NaOH溶液 |
| C.溴易溶于CCl4 | D.酒精易溶于水 |
您最近半年使用:0次
5 . 下列有关化学用语正确的是
| A.HF的电子式:H:F |
B.铍原子最外层电子的原子轨道电子云图: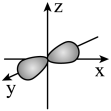 |
C.p—pπ键电子云模型: |
D.氧原子核外电子轨道表示式: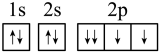 |
您最近半年使用:0次
名校
解题方法
6 . 下列说法错误的是
| A.碘易溶于四氯化碳、甲烷难溶于水,二者都可用相似相溶原理解释 |
B.乳酸分子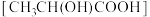 中含有一个手性碳原子 中含有一个手性碳原子 |
| C.氟的电负性大于氯的电负性,导致三氟乙酸的酸性大于三氯乙酸的酸性 |
| D.水很稳定是因为水中含有大量氢键 |
您最近半年使用:0次
名校
7 .  为一种治疗真菌感染的药物,合成路线如下:
为一种治疗真菌感染的药物,合成路线如下: 不稳定。
不稳定。
回答下列问题:
(1) 的反应类型为
的反应类型为_______ 。
(2)化合物 中所含
中所含 原子的杂化方式为
原子的杂化方式为_______ 。
(3) 的反应中生成的
的反应中生成的 分子不含有手性碳原子,
分子不含有手性碳原子, 在
在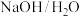 加热条件下生成稳定产物的官能团名称为
加热条件下生成稳定产物的官能团名称为_______ 。该反应除B分子外,还有副产物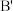 ,
,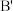 的结构简式为
的结构简式为_______ 。
(4)F的水解产物为I,I的同分异构体中满足以下条件的结构简式为_______ (写出其中一种)
①能发生银镜反应;②核磁共振氢谱显示为5组峰,且峰面积比为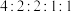
(5)写出以 和
和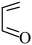 为原料制备
为原料制备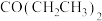 的合成路线流程图
的合成路线流程图_______ (无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)
 为一种治疗真菌感染的药物,合成路线如下:
为一种治疗真菌感染的药物,合成路线如下: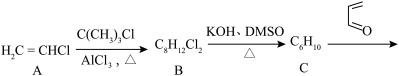
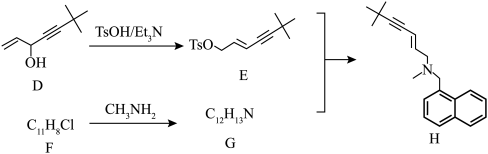
 不稳定。
不稳定。回答下列问题:
(1)
 的反应类型为
的反应类型为(2)化合物
 中所含
中所含 原子的杂化方式为
原子的杂化方式为(3)
 的反应中生成的
的反应中生成的 分子不含有手性碳原子,
分子不含有手性碳原子, 在
在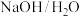 加热条件下生成稳定产物的官能团名称为
加热条件下生成稳定产物的官能团名称为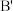 ,
,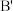 的结构简式为
的结构简式为(4)F的水解产物为I,I的同分异构体中满足以下条件的结构简式为
①能发生银镜反应;②核磁共振氢谱显示为5组峰,且峰面积比为
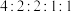
(5)写出以
 和
和 为原料制备
为原料制备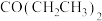 的合成路线流程图
的合成路线流程图
您最近半年使用:0次
名校
解题方法
8 . 尿素作为主要的化肥种类之一,也是一种重要的化工原料。合成尿素的反应为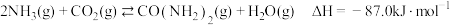 。
。
(1) 时,将一定量
时,将一定量 与
与 在恒温恒容密闭容器中发生上述反应,下列不能说明该反应达到平衡状态的是
在恒温恒容密闭容器中发生上述反应,下列不能说明该反应达到平衡状态的是___________ (填标号)。
A.反应体系中气体分子的平均摩尔质量保持不变
B.反应体系中气体的密度保持不变
C.反应消耗 同时生成
同时生成
D.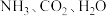 三种气体的物质的量之比为
三种气体的物质的量之比为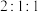
E. 的质量保持不变
的质量保持不变
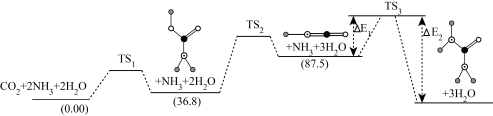
(2)如图是上述反应合成尿素的机理及能量变化(单位: ),
), 表示过渡态。
表示过渡态。
①尿素分子中C原子的杂化方式为___________ 。
②该反应历程中,起决速步骤的方程式为___________ 。
若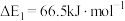 ,则
,则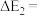
___________  。
。 ,在液相中,
,在液相中, 的平衡转化率与温度,初始氨碳比[用L表示,
的平衡转化率与温度,初始氨碳比[用L表示, ]、初始水碳比[用W表示,
]、初始水碳比[用W表示, ]关系如图所示。
]关系如图所示。 中,
中,___________ (填“A”或“B”)的W较小,判断依据是___________ 。
②对于液相反应,常用某组分M达到平衡时的物质的量分数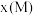 代替平衡浓度来计算平衡常数(记作
代替平衡浓度来计算平衡常数(记作 )。
)。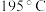 时,
时,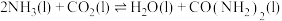 的
的 的值为
的值为___________ 。
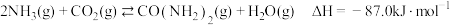 。
。(1)
 时,将一定量
时,将一定量 与
与 在恒温恒容密闭容器中发生上述反应,下列不能说明该反应达到平衡状态的是
在恒温恒容密闭容器中发生上述反应,下列不能说明该反应达到平衡状态的是A.反应体系中气体分子的平均摩尔质量保持不变
B.反应体系中气体的密度保持不变
C.反应消耗
 同时生成
同时生成
D.
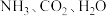 三种气体的物质的量之比为
三种气体的物质的量之比为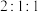
E.
 的质量保持不变
的质量保持不变(2)如图是上述反应合成尿素的机理及能量变化(单位:
 ),
), 表示过渡态。
表示过渡态。①尿素分子中C原子的杂化方式为
②该反应历程中,起决速步骤的方程式为
若
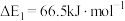 ,则
,则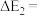
 。
。
 ,在液相中,
,在液相中, 的平衡转化率与温度,初始氨碳比[用L表示,
的平衡转化率与温度,初始氨碳比[用L表示, ]、初始水碳比[用W表示,
]、初始水碳比[用W表示, ]关系如图所示。
]关系如图所示。
 中,
中,②对于液相反应,常用某组分M达到平衡时的物质的量分数
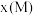 代替平衡浓度来计算平衡常数(记作
代替平衡浓度来计算平衡常数(记作 )。
)。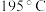 时,
时,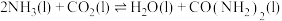 的
的 的值为
的值为
您最近半年使用:0次
名校
9 . A、B、C、D、E、F、G是元素周期表前四周期常见元素,且原子序数依次增大,其相关信息如表所示,请用化学用语回答下列问题。
(1)写出元素符号A:_______ ,B:_______ ,E_______ ,G:_______ 。
(2)C、D、E三种元素的原子半径由大到小的顺序为_______ (用元素符号表示)。
(3)由A、B、C三种元素分别与氢元素形成的简单气态氢化物,其空间构型分别为:_______ ,_______ ,_______ 。
(4)已知元素A、B形成的 分子中所有原子都满足8电子稳定结构,则
分子中所有原子都满足8电子稳定结构,则 中σ键与π键之比为
中σ键与π键之比为_______ 。
(5)G元素可形成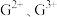 ,其中较稳定的是
,其中较稳定的是 ,试从核外电子排布的角度解释其原因:
,试从核外电子排布的角度解释其原因:_______ 。
(6)短周期元素M与D同族,已知元素M、F的电负性分别为1.5和3.0,预测它们形成的化合物是_______ 化合物(填“离子”或“共价”)。根据“对角线规则”,元素周期表中某些处于对角的元素,它们的化合物性质具有相似性,则M的最高价氧化物对应的水化物与NaOH溶液反应的离子方程式为_______ 。
| A | 原子核外有6种不同运动状态的电子 |
| C | 基态原子中s电子总数与p电子总数相等 |
| D | 电离能数据(单位: ):738、1451、7733、10540、13630…… ):738、1451、7733、10540、13630…… |
| E | 基态原子最外层电子排布式为: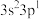 |
| F | 基态原子的最外层p轨道上2个电子的自旋状态与其他电子的自旋状态相反 |
| G | 其中一种氧化物是有磁性的黑色固体 |
(2)C、D、E三种元素的原子半径由大到小的顺序为
(3)由A、B、C三种元素分别与氢元素形成的简单气态氢化物,其空间构型分别为:
(4)已知元素A、B形成的
 分子中所有原子都满足8电子稳定结构,则
分子中所有原子都满足8电子稳定结构,则 中σ键与π键之比为
中σ键与π键之比为(5)G元素可形成
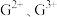 ,其中较稳定的是
,其中较稳定的是 ,试从核外电子排布的角度解释其原因:
,试从核外电子排布的角度解释其原因:(6)短周期元素M与D同族,已知元素M、F的电负性分别为1.5和3.0,预测它们形成的化合物是
您最近半年使用:0次
名校
10 . 请回答下列问题:
(1)由磷原子核形成的三种微粒:① 、②
、② 、③
、③ ,半径由大到小的顺序为
,半径由大到小的顺序为_______ (填标号,下同);再失去一个电子所需最低能量由大到小的顺序为_______ 。
(2)比较H-O-H键角大小;H3O+_______ H2O(填“>”、“<”或“=”)。
(3)胍(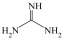 )分子中所有原子共平面,胍中N杂化方式为
)分子中所有原子共平面,胍中N杂化方式为_______ 。
(4)干冰晶体中,每个CO2周围等距离且紧邻的CO2有_______ 个;在冰晶体结构中,每个水分子最多与相邻的_______ 个水分子相连接。同为分子晶体,但干冰中CO2的配位数大于冰中水分子的配位数,其原因是_______ 。
(1)由磷原子核形成的三种微粒:①
 、②
、② 、③
、③ ,半径由大到小的顺序为
,半径由大到小的顺序为(2)比较H-O-H键角大小;H3O+
(3)胍(
 )分子中所有原子共平面,胍中N杂化方式为
)分子中所有原子共平面,胍中N杂化方式为(4)干冰晶体中,每个CO2周围等距离且紧邻的CO2有
您最近半年使用:0次



