名校
1 . 乙烯的产量是衡量一个国家石油化工发展水平的重要标志。一定条件下 和
和 合成乙烯的反应为
合成乙烯的反应为 。向1L恒容密闭容器中充入1mol
。向1L恒容密闭容器中充入1mol  和3mol
和3mol  ,测得不同温度下
,测得不同温度下 的平衡转化率及催化剂的催化效率如题图所示。下列说法正确的是
的平衡转化率及催化剂的催化效率如题图所示。下列说法正确的是
 和
和 合成乙烯的反应为
合成乙烯的反应为 。向1L恒容密闭容器中充入1mol
。向1L恒容密闭容器中充入1mol  和3mol
和3mol  ,测得不同温度下
,测得不同温度下 的平衡转化率及催化剂的催化效率如题图所示。下列说法正确的是
的平衡转化率及催化剂的催化效率如题图所示。下列说法正确的是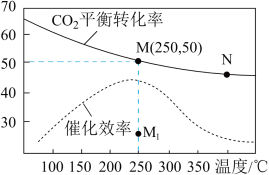
| A.升高温度,平衡向逆反应方向移动,催化剂的催化效率降低 |
| B.图中M点乙烯的体积分数约为7.7% |
C.250℃时,当 的转化率位于 的转化率位于 点时,保持其他条件不变,仅延长反应时间不可能使转化率达到50% 点时,保持其他条件不变,仅延长反应时间不可能使转化率达到50% |
D.向N点的平衡体系中充入1mol  和3mol 和3mol  ,其他条件不变,再次达到平衡时, ,其他条件不变,再次达到平衡时, 增大 增大 |
您最近半年使用:0次
2 . 向绝热恒容密闭容器中通入一定量SO2与NO2的混合气体,在一定条件下发生反应:SO2(g)+NO2(g) SO3(g)+NO(g)。其正反应速率
SO3(g)+NO(g)。其正反应速率 正随时间t变化的曲线如下,不考虑副反应的影响,下列说法正确的是
正随时间t变化的曲线如下,不考虑副反应的影响,下列说法正确的是
 SO3(g)+NO(g)。其正反应速率
SO3(g)+NO(g)。其正反应速率 正随时间t变化的曲线如下,不考虑副反应的影响,下列说法正确的是
正随时间t变化的曲线如下,不考虑副反应的影响,下列说法正确的是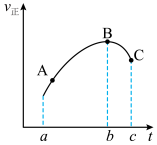
A. 逆随t变化的曲线在a~c时间段内与 逆随t变化的曲线在a~c时间段内与 正的趋势相同 正的趋势相同 |
| B.从A点到C点,NO的分压一直增大 |
| C.其他条件不变时,若在恒温条件下发生此反应,则SO2的平衡转化率减小 |
| D.A、B、C三点的Q值:QA>QB>Qc |
您最近半年使用:0次
名校
解题方法
3 . 一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇: ,分别在300℃和500℃下生成甲醇的量如图所示。根据图像,计算在500℃时,从反应开始到平衡的氢气的平均反应速率为
,分别在300℃和500℃下生成甲醇的量如图所示。根据图像,计算在500℃时,从反应开始到平衡的氢气的平均反应速率为
 ,分别在300℃和500℃下生成甲醇的量如图所示。根据图像,计算在500℃时,从反应开始到平衡的氢气的平均反应速率为
,分别在300℃和500℃下生成甲醇的量如图所示。根据图像,计算在500℃时,从反应开始到平衡的氢气的平均反应速率为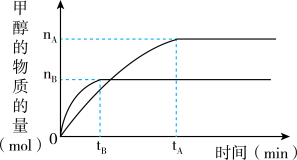
A.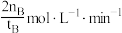 | B. | C. | D.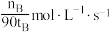 |
您最近半年使用:0次
名校
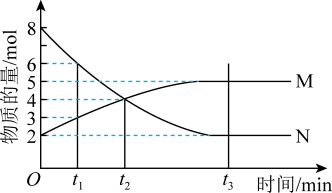
4 . Ⅰ.在一定温度下,4L密闭容器内某一反应中气体M、气体N的物质的量随时间变化的曲线如图: 时刻,正逆反应速率大小
时刻,正逆反应速率大小
___________  。(填“>”“=”或“<”)
。(填“>”“=”或“<”)
(2)若 min,计算反应开始至
min,计算反应开始至 时刻用M的浓度变化表示的平均反应速率
时刻用M的浓度变化表示的平均反应速率___________ 。
(3) 时刻化学反应达到平衡,反应物的转化率为
时刻化学反应达到平衡,反应物的转化率为___________ 。
(4)写出反应的化学方程式___________ 。
(5)如果升高温度,则
___________ (填“增大”“减小”或“不变”)。
Ⅱ.某同学设计如下实验方案探究影响锌与稀硫酸反应速率的因素,有关数据如下表所示:
(6)①本实验待测数据可以是___________ ,实验Ⅰ和实验Ⅱ可以探究___________ ,对锌与稀硫酸反应速率的影响。
②实验Ⅲ和实验Ⅳ的目的是___________ 。
(7)为探究反应物浓度对化学反应速率的影响,设计的实验方案如下表:
表中
___________ 。
 时刻,正逆反应速率大小
时刻,正逆反应速率大小
 。(填“>”“=”或“<”)
。(填“>”“=”或“<”)(2)若
 min,计算反应开始至
min,计算反应开始至 时刻用M的浓度变化表示的平均反应速率
时刻用M的浓度变化表示的平均反应速率(3)
 时刻化学反应达到平衡,反应物的转化率为
时刻化学反应达到平衡,反应物的转化率为(4)写出反应的化学方程式
(5)如果升高温度,则

Ⅱ.某同学设计如下实验方案探究影响锌与稀硫酸反应速率的因素,有关数据如下表所示:
| 序号 | 纯锌粉/g | 2.0 硫酸溶液/mL 硫酸溶液/mL | 温度/℃ | 硫酸铜固体/g | 加入蒸馏水/mL |
| Ⅰ | 2.0 | 50.0 | 25 | 0 | 0 |
| Ⅱ | 2.0 | 40.0 | 25 | 0 | 10.0 |
| Ⅲ | 2.0 | 50.0 | 25 | 0.2 | 0 |
| Ⅳ | 2.0 | 50.0 | 25 | 4.0 | 0 |
(6)①本实验待测数据可以是
②实验Ⅲ和实验Ⅳ的目的是
(7)为探究反应物浓度对化学反应速率的影响,设计的实验方案如下表:
| 实验序号 | 体积V/mL | ||||
 溶液 溶液 | 水 | KI溶液 |  溶液 溶液 | 淀粉溶液 | |
| ① | 10.0 | 0.0 | 4.0 | 4.0 | 2.0 |
| ② | 9.0 | 1.0 | 4.0 | 4.0 | 2.0 |
| ③ | 8.0 |  | 4.0 | 4.0 | 2.0 |
您最近半年使用:0次
5 . 一定条件下, 在恒容密闭容器中发生分解反应:
在恒容密闭容器中发生分解反应: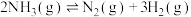
 ,
, 随时间的变化如图所示。已知
随时间的变化如图所示。已知 时反应达到平衡,
时反应达到平衡, 时改变某单一条件(浓度、温度或催化剂等),下列说法不正确的是
时改变某单一条件(浓度、温度或催化剂等),下列说法不正确的是
 在恒容密闭容器中发生分解反应:
在恒容密闭容器中发生分解反应: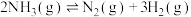
 ,
, 随时间的变化如图所示。已知
随时间的变化如图所示。已知 时反应达到平衡,
时反应达到平衡, 时改变某单一条件(浓度、温度或催化剂等),下列说法不正确的是
时改变某单一条件(浓度、温度或催化剂等),下列说法不正确的是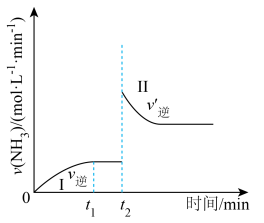
A.由0到 , , 的浓度不断增大 的浓度不断增大 |
B.由 到 到 , ,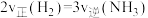 |
C. 时,可能向容器中通入了 时,可能向容器中通入了 |
D.平衡常数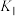 可能小于 可能小于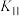 |
您最近半年使用:0次
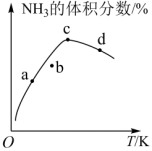
6 . 为了降低大气中NO的排放量,可在NH3的作用下,通过催化剂将NO转化为无毒无害的 。向2L的恒容密闭容器中加入一定量的NH3、NO、NO2,测得NH3、N2、H2O的浓度随时间的变化情况如图所示。下列说法正确的是
。向2L的恒容密闭容器中加入一定量的NH3、NO、NO2,测得NH3、N2、H2O的浓度随时间的变化情况如图所示。下列说法正确的是
 。向2L的恒容密闭容器中加入一定量的NH3、NO、NO2,测得NH3、N2、H2O的浓度随时间的变化情况如图所示。下列说法正确的是
。向2L的恒容密闭容器中加入一定量的NH3、NO、NO2,测得NH3、N2、H2O的浓度随时间的变化情况如图所示。下列说法正确的是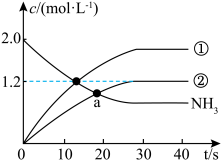
| A.曲线①表示N2的浓度随时间的变化情况 |
B.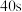 时, 时,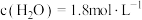 |
C.a点时,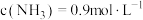 |
D.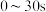 内,用NO表示的平均反应速率为 内,用NO表示的平均反应速率为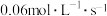 |
您最近半年使用:0次
7 . 一种芳香族化合物 结构如图。
结构如图。 萃取稀土离子
萃取稀土离子 的原理为
的原理为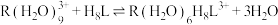 。分配比
。分配比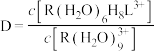 ,水相初始浓度
,水相初始浓度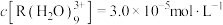 ,萃取平衡时
,萃取平衡时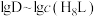 关系如图。下列说法正确的是
关系如图。下列说法正确的是

 结构如图。
结构如图。 萃取稀土离子
萃取稀土离子 的原理为
的原理为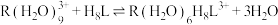 。分配比
。分配比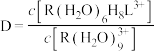 ,水相初始浓度
,水相初始浓度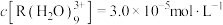 ,萃取平衡时
,萃取平衡时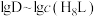 关系如图。下列说法正确的是
关系如图。下列说法正确的是
A.该条件下, 对图中三种阳离子的萃取平衡常数数量级相同 对图中三种阳离子的萃取平衡常数数量级相同 |
B.达平衡时水相中 |
C. 对 对 的萃取效果最好 的萃取效果最好 |
D.萃取平衡时,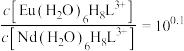 |
您最近半年使用:0次
解题方法
8 . 低碳烷烃选择氧化及脱氢反应的研究既是解决能源问题的有效途径之一,也是碳基能源催化研究的热门课题。乙烷的选择氧化生成乙醛有如下三种反应机理:
机理Ⅰ:C2H6→CH3CHO
机理Ⅱ:C2H6→CH3CH2OH→CH3CHO
机理Ⅲ:C2H6→C2H4→CH3CHO
已知下图是乙烷选择氧化生成乙醛的一种反应历程的过渡态、中间体和产物的稳定几何构型。
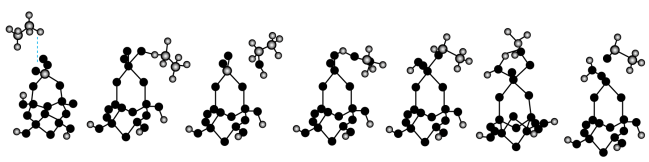
请回答下列问题:
(1)根据图中的几何构型示意图,推测该反应历程是乙烷选择氧化生成乙醛的机理___________ (填“Ⅰ”或“Ⅱ”或“Ⅲ”)
(2)一定条件下,几种化学键的键能如表所示
①反应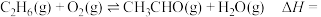
___________  。升高温度活化分子百分数将
。升高温度活化分子百分数将___________ (填“增大”或“不变”或“减小”)。
②温度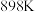 下,在
下,在 的刚性密闭容器中按一定比例
的刚性密闭容器中按一定比例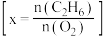 加入
加入 和
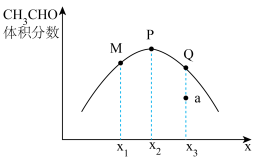
和 发生反应,平衡时
发生反应,平衡时 的体积分数与
的体积分数与 的关系如图所示。图中P点的横坐标
的关系如图所示。图中P点的横坐标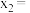
___________ ;乙烷转化率最大的是___________ 点(填“M”或“P”或“Q”);若要缩短a点至Q点所用的时间,可采取的措施有___________ (答出一条即可)。
(3)反应速率与浓度之间存在如下关系: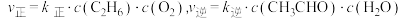 ,k正、k逆为速率常数,只受温度影响。
,k正、k逆为速率常数,只受温度影响。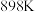 时在
时在 的刚性密闭容器中,通入
的刚性密闭容器中,通入 和
和 发生反应,保持温度不变,平衡时
发生反应,保持温度不变,平衡时 的体积分数为
的体积分数为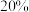 ,则此温度下
,则此温度下 的转化率为
的转化率为___________ ;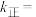
___________ (用k逆表示);当温度升高时,k正增大b倍,k逆增大d倍,则b___________ d(填“>”或“=”或“<”)。
机理Ⅰ:C2H6→CH3CHO
机理Ⅱ:C2H6→CH3CH2OH→CH3CHO
机理Ⅲ:C2H6→C2H4→CH3CHO
已知下图是乙烷选择氧化生成乙醛的一种反应历程的过渡态、中间体和产物的稳定几何构型。

请回答下列问题:
(1)根据图中的几何构型示意图,推测该反应历程是乙烷选择氧化生成乙醛的机理
(2)一定条件下,几种化学键的键能如表所示
| 化学键 | C-H | O-H | O=O | C=O | C-C |
| 键能kJ·mol-l | 413.4 | 426.8 | 497.3 | 750 | 347.7 |
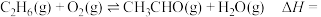
 。升高温度活化分子百分数将
。升高温度活化分子百分数将②温度
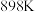 下,在
下,在 的刚性密闭容器中按一定比例
的刚性密闭容器中按一定比例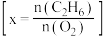 加入
加入 和
和 发生反应,平衡时
发生反应,平衡时 的体积分数与
的体积分数与 的关系如图所示。图中P点的横坐标
的关系如图所示。图中P点的横坐标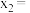

(3)反应速率与浓度之间存在如下关系:
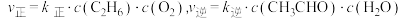 ,k正、k逆为速率常数,只受温度影响。
,k正、k逆为速率常数,只受温度影响。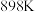 时在
时在 的刚性密闭容器中,通入
的刚性密闭容器中,通入 和
和 发生反应,保持温度不变,平衡时
发生反应,保持温度不变,平衡时 的体积分数为
的体积分数为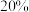 ,则此温度下
,则此温度下 的转化率为
的转化率为
您最近半年使用:0次
解题方法
9 . 已知反应
 ,将
,将 和
和 按一定比例通入恒温恒压的密闭容器中,反应相同时间后,
按一定比例通入恒温恒压的密闭容器中,反应相同时间后, 的体积分数随温度的变化关系如图所示。下列说法正确的是
的体积分数随温度的变化关系如图所示。下列说法正确的是
A.b点 | B.逆反应速率: |
C.平衡常数值: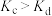 | D.反应在a、c、d点均达到平衡状态 |
您最近半年使用:0次
名校
10 . 络合平衡是广泛存在于自然界中的平衡之一, 、
、 、
、 之间存在络合平衡:
之间存在络合平衡:
① ,平衡常数为
,平衡常数为 ;
;
② ,平衡常数为
,平衡常数为 ,且
,且 大于
大于 。
。

 、
、 、
、 之间存在络合平衡:
之间存在络合平衡:①
 ,平衡常数为
,平衡常数为 ;
;②
 ,平衡常数为
,平衡常数为 ,且
,且 大于
大于 。
。298K时,在水溶液中,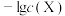 ,
,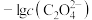 之间关系如图所示,其中,X代表
之间关系如图所示,其中,X代表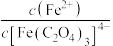 、
、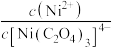 下列叙述正确的是
下列叙述正确的是

A.由图可知 的数量级为 的数量级为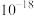 |
B. 直线代表 直线代表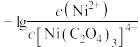 与 与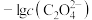 关系 关系 |
C.c点条件下,能生成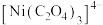 ,不能生成 ,不能生成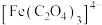 |
D.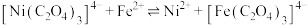 的平衡常数K为 的平衡常数K为 |
您最近半年使用:0次



