16. (1)在容积为1.00 L的容器中,通入一定量的N
2O
4(g),发生反应,随温度升高,混合气体的颜色变深。回答下列问题:
①写出反应的化学方程式:
___________________________________。
②100 ℃时,体系中各物质浓度随时间变化如图所示。
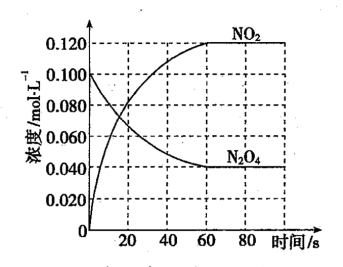
在0~60 s时段,反应速率
v(N
2O
4)为
_______ mol·L
-1·s
-1。
(2)可逆反应N
2+3H
2
2NH
3是工业上合成氨的重要反应,反应过程中的能量变化如图所示:
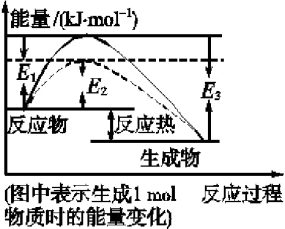
①根据题图,请写出合成氨的热化学方程式(热量值用
E1、
E2或
E3表示)
____________________。
②图中虚线部分是通过
________来改变化学反应速率。
③下列各关系中能说明反应已达到平衡状态的是
____。
A.3
v正(N
2)=
v正(H
2) B.
v正(N
2)=
v逆(NH
3)
C.
v正(N
2)=3
v逆(H
2) D.2
v正(H
2)=3
v逆(NH
3)