21. 为了缓解温空效应,科学家提出了多种回收和利用CO
2的方案。
(1)方案1: 利用FeO吸收CO
2获得H
2ⅰ.6FeO(s)+CO
2(g)=2Fe
3O
4(s)+C(s) ΔH
1=-76.0kJ/mol
ⅱ.C(s)+2H
2O(g)=CO
2(g)+2H
2(g) ΔH
2 =+113. 4kJ/mol
请写出由FeO制备H
2的热化学方程式
_________________。
方案2: 利用CO
2制备CH
4300℃时,向2L恒容密闭容器中充入2molCO
2和8molH
2发生反应: CO
2(g)+4H
2(g)

CH
4(g)+ 2H
2O(g) ΔH
4,混合气体中CH
4的浓度与反应时间的关系如图所示。
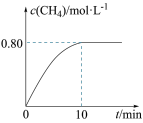
(2)① 从反应开始到恰好达到平衡时,H
2的平均反应速率v(H
2)=
_________________。
② 300℃时,反应的平衡常数K=
_______________。
③ 300℃时,如果该容器中有1.6molCO
2、2.0molH
2、5.6molCH
4、4.0molH
2O(g)。则v
正____________v
逆(填“>”“<”或“=" )
(3)下列有关说法正确的是(填序号)
_______________。
A.容器内密度不变,说明反应达到平衡状态
B.容器内压强不变,说明反应达到平衡状态
C.300℃时,向平衡后的容器中再充入2molCO
2和8molH
2,重新达到平衡时CH
4的浓度等于1.6mo/L
D.每断开2molC=O键的同时断开4molC-H键,说明反应达到平衡状态
E.达到平衡后,分离出水蒸气,既能加快反应速率又能使平衡正方向移动
(4)已知200℃时,该反应的平衡常数K=64.8(L
/mol)
2。则ΔH
4________0(填“>”“<”或“=”)。
方案3:利用“Na-CO
2”电池将CO
2变废为宝。我国科研人员研制出的可充电“Na-CO
2”电池钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应为4Na+3CO
2
2Na
2CO
3+C。放电时该电池“吸入”CO
2,其工作原理如图所示:(假设开始时两极的质量相等)

(5)①放电时,正极的电极反应式为
_______________。
②若生成的Na
2CO
3和C全部沉积在电极表面,当转移0.2mole
-时,两极的质量差为
_____g。