22. (1)随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO
2的含量及有效地开发利用CO
2,引起了各国的普遍关注, 目前工业上有一种方法是用CO
2来生产燃料甲醇。为探究反应原理,现进行如下实验:在体积为1 L的密闭容器中,充入1mol CO
2和3mol H
2,一定条件下发生反应:CO
2(g)+3H
2(g)

CH
3OH(g)+H
2O(g) △H=-49.0kJ/mol
测得CO
2和CH
3OH(g)的浓度随时间变化如图所示。
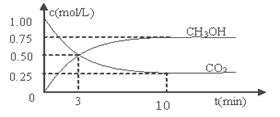
平衡时H
2的转化率为
________________。
反应进行到3 min时,同种物质的v
正 与v
逆的关系: v
正________v
逆(填>,=,<)
③ 上述反应平衡常数的表达式为
___________________,经计算该温度下此反应平衡常数的数值为
_______________。
(2)如图装置,A、B中电极为多孔的惰性电极;C、D为夹在湿的Na
2SO
4滤纸条上的铂夹;电源有a、b两极。若在A、B中充满KOH溶液后倒立于KOH溶液的水槽中,切断K
1,闭合K
2、K
3,通直流电,一段时间后试管中产生气体,如图所示,据此分析:
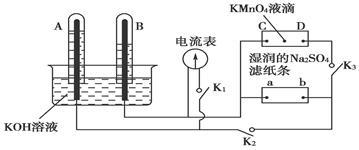
B试管中的气体是
_____(填名称或分子式);a为电源
________(正或负)极。
写出电解时A极的电极反应式:
__________________。
③若电解一段时间,A、B中均有气体包围电极。此时切断K
2、K
3,闭合K
1。电流表的指针偏转,则此时B极电极反应式为
_________________。
(3)甲烷燃料电池可以提升能量利用率.如图所示是利用甲烷燃料电池电解50ml2mol/L的氯化铜溶液的装置示意图:
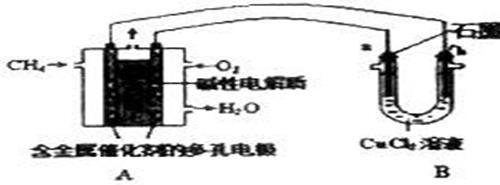
请回答:
甲烷燃料电池的负极反应式是:
_____________________.
当A中消耗0.05mol氧气时,B中
________极(填“a”或“b”)增重
________g.