19. S
2Cl
2是工业上常用的硫化剂,实验室制备S
2Cl
2的方法有2种:①CS
2+3Cl
2
CCl
4+S
2Cl
2;②2S+Cl
2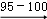
S
2Cl
2.已知S
2Cl
2中硫元素显+1价,电子式:
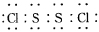
,它不稳定,在水中易发生岐化反应(一部分硫元素价态升高,一部分降低),反应涉及的几种物质的熔沸点如表:
| 物质 | S | CS2 | CCl4 | S2Cl2 |
| 沸点/℃ | 445 | 47 | 77 | 137 |
| 熔点/℃ | 113 | ﹣109 | ﹣23 | ﹣77 |
实验室利用下列装置制备S
2Cl
2(部分夹持仪器已略去)。回答下列问题:
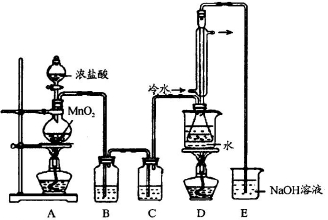
(1)写出A装置中发生反应的离子方程式
_________。
(2)实验中盐酸通常采用36.5%的浓溶液,不用稀盐酸的理由是
__________。
(3)D中冷凝管起到导气和冷凝回流双重作用.这种冷却装置可应用于下列高中化学中
_______实验。
A.石油分馏 B.制备乙烯
C.制取乙酸乙酯 D.制取溴苯
(4)B装置中盛放的是
_________,反应结束后从锥形瓶内混合物中分离出产品的方法是
_________,D中采用热水浴加热的原因是
__________。
(5)A装置仪器装配时,整套装置装配完毕后,应先进行
__________,再添加试剂.实验完毕,拆除装置时,应先将E中长导管移开液面,目的是
__________。
(6)实验过程中,若缺少C装置,则发现产品浑浊不清,出现该现象的原因可用化学方程式表示为
______________。实验完毕,当把剩余浓盐酸倒入E烧杯中与吸收了尾气的氢氧化钠溶液混合时,发现有少量黄绿色刺激性气体产生,产生该现象的原因是
_________________。(用离子方程式表示)