名校
1 . 在常温下,有关下列4种溶液的叙述中错误的是
| 编号 | ① | ② | ③ | ④ |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
| pH | 11 | 11 | 3 | 3 |
| A.在溶液①、②中分别加入适量的氯化铵晶体后,两种溶液的pH均减小 |
| B.分别取1mL稀释至10mL,四种溶液的pH:①>②>④>③ |
C.将溶液①、④等体积混合,所得溶液中: |
D.将aL溶液④与bL溶液②混合后,若所得溶液的pH=4,则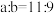 |
您最近半年使用:0次
名校
2 . 水溶液存在离子平衡,回答下列问题:
(1)水的电离平衡曲线如图所示。若以A点表示25°C时水在电离平衡时的离子浓度。当温度升到100°C时,水的电离平衡状态到B点,该温度时0.1mol/LNaOH溶液pH为___________ 。___________ (填“正”或“逆”)反应方向移动:水的电离程度将___________ (填“增大”、“减小”或“不变”)。
(3)常温下向20.00mL0.100mol/LHX(一元酸)溶液中滴加0.100mol/LNaOH的pH变化如图所示。___________ 。
②C点溶液中c(X-)___________ c(Na+)(填“>”、“<”或“=”)。
(1)水的电离平衡曲线如图所示。若以A点表示25°C时水在电离平衡时的离子浓度。当温度升到100°C时,水的电离平衡状态到B点,该温度时0.1mol/LNaOH溶液pH为
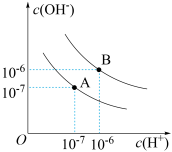
(3)常温下向20.00mL0.100mol/LHX(一元酸)溶液中滴加0.100mol/LNaOH的pH变化如图所示。

②C点溶液中c(X-)
您最近半年使用:0次
3 . 已知四种酸的电离平衡常数如下表,其中酸性最强的是
| 弱酸 | 次氯酸 | 醋酸 | 碳酸 | 硫化氢 |
| 电离平衡常数 | Ka=4.7×10-8 | Ka=1.7×10-5 | Ka1=4.2×10-7 Ka2=5.6×10-11 | Ka1=9.1×10-8 Ka2=1.1×10-12 |
| A.醋酸 | B.次氯酸 | C.碳酸 | D.硫化氢 |
您最近半年使用:0次
4 . 下列物质中属于强电解质的是
| A.NH3 | B.CO2 | C.BaSO4 | D.盐酸 |
您最近半年使用:0次
名校
5 . 类比pH,对于稀溶液pM=-lgc(M)(M:H2A、HA-、A2-),pKa=-lgKa,室温下,向某浓度H2A溶液加入NaOH(s),保持溶液体积和温度不变,测得pH与p(H2A)、p(HA-)、p(A2-)变化如图所示。下列说法不正确的是

| A.a点c(A2-)等于b点c(H2A) |
| B.常温下,pKa1=0.80 |
| C.b点时,c(H+)+c(Na+)=c(OH-)+c(HA-)+c(A2-) |
| D.pH=6.00时,c(A2-)>c(HA-)>c(H2A) |
您最近半年使用:0次
解题方法
6 . 硫、氮和磷是生物必须的营养元素,含硫、氮和磷的化合物在自然界中广泛存在。
(1)火山喷发产生H2S在大气中发生如下反应:
①
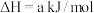
②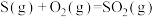
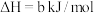
写出H2S(g)完全燃烧的热化学方程式_______ 。
(2)工业上可用NaClO碱性溶液吸收SO2.为了提高吸收效率,常用Ni2O3作为催化剂。反应过程中产生的四价镍和原子氧具有极强的氧化能力,可加快对SO2的吸收。该催化过程的示意图如下图所示。Ca(ClO)2也可用于脱硫,且脱硫效果比NaClO更好,原因是_______ 。_______ ;
②若无能量损失,相同条件下,SO2和NO的体积比为_______ 时,两种气体都能被完全处理。
(4)某含磷废水的主要成分是H3PO3.25℃时,向一定体积的亚磷酸(H3PO3,二元弱酸)溶液中滴加等物质的量浓度的NaOH溶液,混合液中含磷粒子的物质的量分数( )与溶液pH的关系如下图所示。
)与溶液pH的关系如下图所示。_______ 7(填“<”或“>”或“=”)。
②Na2HPO3其水解平衡常数
_______ (填数值)。
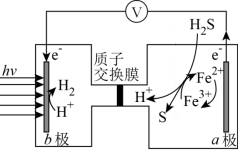
(5)太阳能光电催化——化学耦合分解H2S的装置如图所示。该太阳能光电催化——化学耦合分解H2S的过程可描述为_______ 。
(1)火山喷发产生H2S在大气中发生如下反应:
①

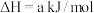
②
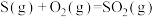
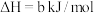
写出H2S(g)完全燃烧的热化学方程式
(2)工业上可用NaClO碱性溶液吸收SO2.为了提高吸收效率,常用Ni2O3作为催化剂。反应过程中产生的四价镍和原子氧具有极强的氧化能力,可加快对SO2的吸收。该催化过程的示意图如下图所示。Ca(ClO)2也可用于脱硫,且脱硫效果比NaClO更好,原因是


②若无能量损失,相同条件下,SO2和NO的体积比为
(4)某含磷废水的主要成分是H3PO3.25℃时,向一定体积的亚磷酸(H3PO3,二元弱酸)溶液中滴加等物质的量浓度的NaOH溶液,混合液中含磷粒子的物质的量分数(
 )与溶液pH的关系如下图所示。
)与溶液pH的关系如下图所示。
②Na2HPO3其水解平衡常数

(5)太阳能光电催化——化学耦合分解H2S的装置如图所示。该太阳能光电催化——化学耦合分解H2S的过程可描述为
您最近半年使用:0次
7 . 室温下,二元酸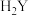 溶液中逐滴滴加NaOH溶液,混合溶液中粒子浓度与pH的关系如图所示。下列说法正确的是
溶液中逐滴滴加NaOH溶液,混合溶液中粒子浓度与pH的关系如图所示。下列说法正确的是
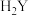 溶液中逐滴滴加NaOH溶液,混合溶液中粒子浓度与pH的关系如图所示。下列说法正确的是
溶液中逐滴滴加NaOH溶液,混合溶液中粒子浓度与pH的关系如图所示。下列说法正确的是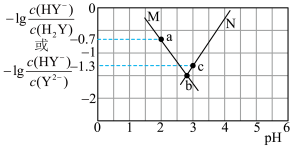
A.曲线M表示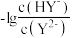 与pH的变化关系 与pH的变化关系 |
| B.a→c过程中,水的电离程度先增大后减小 |
C.b点溶液中: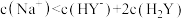 |
D.NaHY溶液中: |
您最近半年使用:0次
8 . 已知常温下水溶液中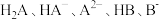 的分布分数
的分布分数 [如
[如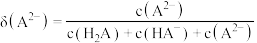 ]随
]随 变化曲线如图1所示;用
变化曲线如图1所示;用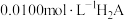 溶液滴定
溶液滴定 溶液,溶液中
溶液,溶液中 和
和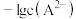 关系如图2所示。下列说法错误的是
关系如图2所示。下列说法错误的是
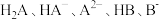 的分布分数
的分布分数 [如
[如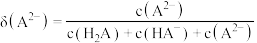 ]随
]随 变化曲线如图1所示;用
变化曲线如图1所示;用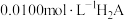 溶液滴定
溶液滴定 溶液,溶液中
溶液,溶液中 和
和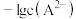 关系如图2所示。下列说法错误的是
关系如图2所示。下列说法错误的是
A.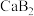 的水解平衡常数的数量级为 的水解平衡常数的数量级为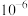 |
B.曲线e为 |
C. |
D.滴定过程中始终存在: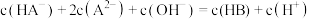 |
您最近半年使用:0次
名校
解题方法
9 . 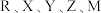 五种短周期主族元素,原子序数依次增大,R元素的原子最外层电子排布式为
五种短周期主族元素,原子序数依次增大,R元素的原子最外层电子排布式为 与M同主族,且M元素的原子序数为Y元素的2倍,Z是同周期元素中原子半径最大的元素,下列说法错误的是
与M同主族,且M元素的原子序数为Y元素的2倍,Z是同周期元素中原子半径最大的元素,下列说法错误的是
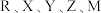 五种短周期主族元素,原子序数依次增大,R元素的原子最外层电子排布式为
五种短周期主族元素,原子序数依次增大,R元素的原子最外层电子排布式为 与M同主族,且M元素的原子序数为Y元素的2倍,Z是同周期元素中原子半径最大的元素,下列说法错误的是
与M同主族,且M元素的原子序数为Y元素的2倍,Z是同周期元素中原子半径最大的元素,下列说法错误的是A.电负性: | B.氢化物的沸点: |
| C.Z与Y形成的化合物中可能含有非极性共价键 | D.等物质的量浓度的 最高价氧化物对应的水化物水溶液酸性依次递增 最高价氧化物对应的水化物水溶液酸性依次递增 |
您最近半年使用:0次
名校
10 . 下列说法不正确的是
| A.Na、K、Rb的密度依次增大 |
| B.H2O、HF、NH3的沸点依次降低 |
| C.等质量的CH4、C2H4、C6H6完全燃烧的耗氧量依次减小 |
| D.等体积等pH的盐酸和醋酸分别与一定量锌反应生成等量氢气时,醋酸耗时短 |
您最近半年使用:0次



