1 . 常温下,等浓度的氨水和醋酸溶液互相滴定过程中,溶液中pH与pX[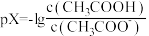 或
或 ]的关系如图所示。下列说法错误的是
]的关系如图所示。下列说法错误的是
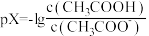 或
或 ]的关系如图所示。下列说法错误的是
]的关系如图所示。下列说法错误的是
A.常温下, |
B.水的电离程度: |
| C.曲线Ⅱ代表NH3•H2O溶液滴定CH3COOH溶液 |
D.g点 |
您最近半年使用:0次
7日内更新
|
330次组卷
|
3卷引用:甘肃省靖远县2024届高三下学期第三次联考化学试题
2 . 常温下,向某浓度的HA溶液中加入NaOH固体,保持溶液的体积和温度不变,测得pH与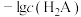 、
、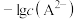 、
、 的变化关系如图所示。下列说法不正确的是
的变化关系如图所示。下列说法不正确的是
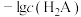 、
、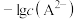 、
、 的变化关系如图所示。下列说法不正确的是
的变化关系如图所示。下列说法不正确的是
A.常温下, 的电离平衡常数 的电离平衡常数 为 为 |
B.a点时, |
| C.a点→b点过程中,水的电离程度增大 |
D.NaHA溶液中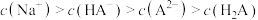 |
您最近半年使用:0次
3 . 向10mLHCOOH-NH4Cl混合溶液(浓度均为0.1mol·L−1)中滴加0.1mol·L−1NaOH溶液,并监测溶液pH变化,实验数据如图。由该实验可得到的结论是
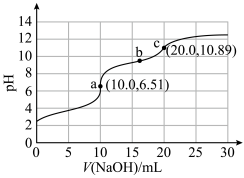
| A.HCOOH电离方程式为HCOOH=H++HCOO− |
| B.由a点数据可推出电离能力:HCOOH>NH3·H2O |
| C.b点溶液中的OH−主要来自HCOO−水解 |
| D.0.05mol·L−1氨水的pH<10.89 |
您最近半年使用:0次
名校
4 . 已知 时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
1.物质的量浓度均为 的下列四种溶液:
的下列四种溶液: 最大是___________。
最大是___________。
2.标准状况下将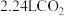 ,通入
,通入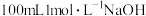 溶液中,用溶液中微粒的浓度符号完成下列等式:
溶液中,用溶液中微粒的浓度符号完成下列等式:
___________ 。
 时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:| 化学式 |  |  |  |
| 电离平衡常数 |  | 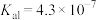  |  |
 的下列四种溶液:
的下列四种溶液: 最大是___________。
最大是___________。A. | B. | C. | D. |
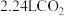 ,通入
,通入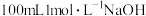 溶液中,用溶液中微粒的浓度符号完成下列等式:
溶液中,用溶液中微粒的浓度符号完成下列等式:
您最近半年使用:0次
名校
解题方法
5 . 常温下,下列关于电解质溶液的说法正确的是
| A.pH=12的氨水和氢氧化钠溶液按体积比1∶9混合后,pH值增大 |
B.等体积、等浓度的Na2CO3和NaHCO3溶液混合后,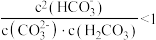 |
C.0.2mol/LCH3COOH溶液与0.1mol/LNaOH溶液等体积混合后存在: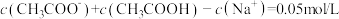 |
D.等浓度的氨水和硫酸按体积比3∶1混合后溶液显碱性,则混合溶液中存在: |
您最近半年使用:0次
7日内更新
|
127次组卷
|
2卷引用:四川省成都市石室中学2023-2024学年高二下学期4月月考化学试卷
解题方法
6 . 常温下,用NaOH溶液滴定磷酸的稀溶液,溶液的 与
与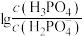 或
或 或
或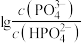 的关系如图所示,下列说法错误的是
的关系如图所示,下列说法错误的是
 与
与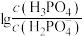 或
或 或
或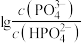 的关系如图所示,下列说法错误的是
的关系如图所示,下列说法错误的是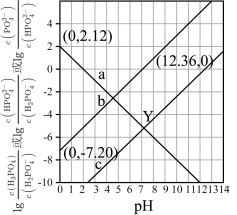
A.直线b表示 与 与 的关系 的关系 |
B.Y点溶液的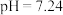 |
C.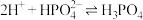 的平衡常数为 的平衡常数为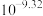 |
D.等浓度的 溶液与 溶液与 溶液按体积比 溶液按体积比 混合后, 混合后,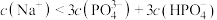 |
您最近半年使用:0次
7 . 常温下向 饱和溶液(始终有
饱和溶液(始终有 固体存在)中滴加HCl溶液或者NaOH溶液调节pH,测得溶液中
固体存在)中滴加HCl溶液或者NaOH溶液调节pH,测得溶液中 浓度的对数lg(Ca)与溶液的pH之间的关系如下图。已知
浓度的对数lg(Ca)与溶液的pH之间的关系如下图。已知 的电离常数的负对数:
的电离常数的负对数: ,
, ;下列说法正确的是
;下列说法正确的是
 饱和溶液(始终有
饱和溶液(始终有 固体存在)中滴加HCl溶液或者NaOH溶液调节pH,测得溶液中
固体存在)中滴加HCl溶液或者NaOH溶液调节pH,测得溶液中 浓度的对数lg(Ca)与溶液的pH之间的关系如下图。已知
浓度的对数lg(Ca)与溶液的pH之间的关系如下图。已知 的电离常数的负对数:
的电离常数的负对数: ,
, ;下列说法正确的是
;下列说法正确的是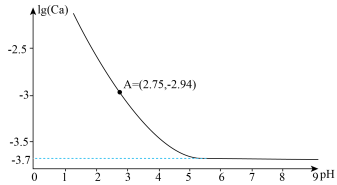
A.溶液中始终存在: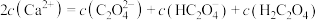 |
B.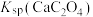 的数量级为 的数量级为 |
C.pH=7时,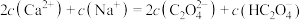 |
D.A点时,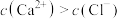 |
您最近半年使用:0次
解题方法
8 . 现有常温下甲、乙、丙、丁、戊五种溶液,其中,甲为0.1mol·L-1的NaOH溶液,乙为0.1mol·L-1的H2SO4溶液,丙为0.1mol·L-1的CH3COOH溶液,丁NH4Cl溶液,戊NaF溶液,试回答下列问题:
(1)甲溶液的pH=_______ 。
(2)丙溶液中存在的电离平衡为_______ 、_______ (用电离方程式表示)。
(3)常温下,用水稀释0.1mol·L-1的CH3COOH溶液时,下列各量随水量的增加而增大的是____ (填序号)。①n(H+) ②c(OH-) ③ ④c(H+)·c(OH-)
④c(H+)·c(OH-)
(4)甲、乙、丙三种溶液中由水电离出的c(OH-)的由大到小的顺序为_______ 。
(5)丁溶液显酸性原因(用离子方程式表示)_______ 。
(6)戊溶液显碱性的原因(用离子方程式表示)_______ 。
(1)甲溶液的pH=
(2)丙溶液中存在的电离平衡为
(3)常温下,用水稀释0.1mol·L-1的CH3COOH溶液时,下列各量随水量的增加而增大的是
 ④c(H+)·c(OH-)
④c(H+)·c(OH-)(4)甲、乙、丙三种溶液中由水电离出的c(OH-)的由大到小的顺序为
(5)丁溶液显酸性原因(用离子方程式表示)
(6)戊溶液显碱性的原因(用离子方程式表示)
您最近半年使用:0次
名校
9 . 已知室温时, 某一元酸HA在水中有0.1%发生电离,下列叙述错误的是
某一元酸HA在水中有0.1%发生电离,下列叙述错误的是
 某一元酸HA在水中有0.1%发生电离,下列叙述错误的是
某一元酸HA在水中有0.1%发生电离,下列叙述错误的是A.该溶液的 |
| B.升高温度,溶液的pH增大 |
C.此酸的电离常数约为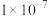 |
D.由HA电离出的 约为水电离出的 约为水电离出的 的 的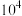 倍 倍 |
您最近半年使用:0次
名校
10 . 亚砷酸(H3AsO3)可用于治疗白血病,亚砷酸在溶液中存在多种微粒形态,向1L0.1mol/LH3AsO3溶液中逐滴加入0.1mol/LKOH溶液,各种微粒的物质的量分数与溶液pH的关系如图所示,下列说法错误的是
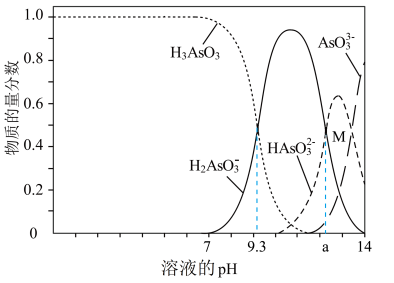
| A.人体血液的pH约为7.35-7.45,服用药物后血液中所含砷元素的主要微粒是H3AsO3 |
| B.该温度下,H3AsO3的电离平衡常数Ka的数量级为10-10 |
C. 时,溶液中: 时,溶液中: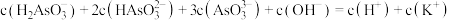 |
D.M点对应的溶液中: |
您最近半年使用:0次



