22-23高二上·山西·期末
名校
解题方法
1 . Ka、Kw、Kh、Ksp分别表示电离常数、水的离子积常数、水解常数、溶度积常数,下列判断不正确的是
A.室温下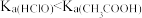 , , 的电离度一定比HClO的大 的电离度一定比HClO的大 |
B.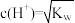 的溶液任何温度下均为中性 的溶液任何温度下均为中性 |
| C.已知25℃时,AgCl和砖红色沉淀Ag2CrO4的Ksp分别为1.8×10-10和2.0×10-12,则用AgNO3标准溶液滴定Cl-时,可采用K2CrO4为指示剂 |
| D.某温度下,一元弱酸HA的Ka越小,则NaA的Kh越大 |
您最近一年使用:0次
2023-12-25更新
|
486次组卷
|
8卷引用:水溶液中的离子反应与平衡——进阶学习
名校
解题方法
2 . 在常温下,有关下列4种溶液的叙述中错误的是
| 编号 | ① | ② | ③ | ④ |
| 溶液 | 氨水 | 氢氧化钠 | 醋酸 | 盐酸 |
| pH | 11 | 11 | 3 | 3 |
| A.在溶液①、②中分别加入适量的氯化铵晶体后,两种溶液的pH均减小 |
| B.分别加水稀释10倍,四种溶液的pH:①>②>④>③ |
C.将溶液①、④等体积混合,所得溶液中: |
D.将aL溶液④与bL溶液②混合后,若所得溶液的 ,则 ,则 |
您最近一年使用:0次
2023-11-22更新
|
143次组卷
|
10卷引用:人教2019版选择性必修一第三章 水溶液中的离子反应与平衡 复习与提高
人教2019版选择性必修一第三章 水溶液中的离子反应与平衡 复习与提高山东省临沂市平邑县、沂水县2020~2021学年高二上学期期中联考化学试题江西省丰城市第九中学2021-2022学年高二上学期第二次月考(日新班)化学试题湖北省天门外国语学校2022-2023学年高二上学期12月月考化学试题四川省成都外国语学校2022-2023学年高二上学期12月月考化学试题天津市南开大学附属中学2022-2023学年高二上学期期末考试化学试卷吉林省长春市东北师范大学附属中学2022-2023学年高三上学期12月期中考试化学试题江西省南昌市第十中学2023-2024学年高二上学期期中考试化学试卷湖南省衡阳市八中2023-2024学年高二上学期第四次月考化学试题湖北省武汉市新洲区第一中学2024届高二上学期11月阶段测试化学试题
3 . 25 ℃时部分弱酸的电离平衡常数如下表:
(1)在温度相同时,各弱酸的Ka值与酸性的相对强弱的关系为________________ 。
(2)室温下①0.1 mol·L-1 HCOONa,②0.1 mol·L-1 NaClO,③0.1 mol·L-1 Na2CO3,④0.1 mol·L-1 NaHCO3,溶液的pH由大到小的关系为________________ 。
(3)浓度均为0.1 mol·L-1的Na2SO3和Na2CO3的混合溶液中,SO 、CO
、CO 、HSO
、HSO 、HCO
、HCO 浓度由大到小的顺序为
浓度由大到小的顺序为____________________ 。
(4)下列离子方程式书写正确的是__________ (填字母)。
a.2ClO-+H2O+CO2=2HClO+CO
b.2HCOOH+CO =2HCOO-+H2O+CO2↑
=2HCOO-+H2O+CO2↑
c.H2SO3+2HCOO-=2HCOOH+SO
d.Cl2+H2O+2CO =2HCO
=2HCO +Cl-+ClO-
+Cl-+ClO-
(5)常温下,pH=3的HCOOH溶液与pH=11的NaOH溶液等体积混合后,溶液中离子浓度由大到小的顺序为________________________ 。
弱酸 | HCOOH | HClO | H2CO3 | H2SO3 |
电离平衡 常数/(mol·L-1) | Ka=1.8×10-4 | Ka=4.7×10-8 | Ka1=4.2×10-7 Ka2=5.6×10-11 | Ka1=1.54×10-2 Ka2=1.02×10-7 |
(2)室温下①0.1 mol·L-1 HCOONa,②0.1 mol·L-1 NaClO,③0.1 mol·L-1 Na2CO3,④0.1 mol·L-1 NaHCO3,溶液的pH由大到小的关系为
(3)浓度均为0.1 mol·L-1的Na2SO3和Na2CO3的混合溶液中,SO
 、CO
、CO 、HSO
、HSO 、HCO
、HCO 浓度由大到小的顺序为
浓度由大到小的顺序为(4)下列离子方程式书写正确的是
a.2ClO-+H2O+CO2=2HClO+CO

b.2HCOOH+CO
 =2HCOO-+H2O+CO2↑
=2HCOO-+H2O+CO2↑c.H2SO3+2HCOO-=2HCOOH+SO

d.Cl2+H2O+2CO
 =2HCO
=2HCO +Cl-+ClO-
+Cl-+ClO-(5)常温下,pH=3的HCOOH溶液与pH=11的NaOH溶液等体积混合后,溶液中离子浓度由大到小的顺序为
您最近一年使用:0次
4 . 25 ℃时,用浓度为0.100 0 mol·L-1的NaOH溶液滴定20.00 mL浓度均为0.100 0 mol·L-1的三种酸HX、HY、HZ的溶液,滴定曲线如图所示。
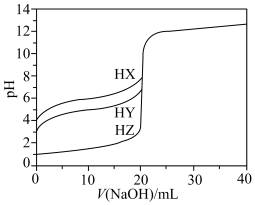
(1)在相同温度下,相同浓度的三种酸溶液的导电能力由强到弱的顺序是____________ 。
(2)V(NaOH)=20.00 mL时,溶液中c(HY)__________ (填“<”“>”或“=”,下同)c(Y-)。若使最终溶液的pH=7,则滴定HZ溶液和滴定HX溶液所需NaOH溶液的体积的关系是HX溶液________ HZ溶液。
(3)将上述HX溶液、HY溶液等体积混合后,用NaOH溶液滴定至HX恰好完全反应时,溶液中各离子浓度的大小关系为_____________ 。
(4)根据滴定曲线,可得Ka(HY)≈________ 。

(1)在相同温度下,相同浓度的三种酸溶液的导电能力由强到弱的顺序是
(2)V(NaOH)=20.00 mL时,溶液中c(HY)
(3)将上述HX溶液、HY溶液等体积混合后,用NaOH溶液滴定至HX恰好完全反应时,溶液中各离子浓度的大小关系为
(4)根据滴定曲线,可得Ka(HY)≈
您最近一年使用:0次
5 . 已知在25 ℃时,氨水中NH3·H2O的电离常数Kb=1.8×10-5 mol·L-1,回答下列问题:
(1)氨水中NH3·H2O的电离常数表达式Kb=___________ 。
(2)当向该氨水中加入一定量的NaOH溶液时,Kb值是否会发生变化?___________ (填“会”或“不会”)。
(3)若该氨水的起始浓度为0.01 mol·L-1,则达到电离平衡时溶液中OH-的物质的量浓度为___________ 。
(1)氨水中NH3·H2O的电离常数表达式Kb=
(2)当向该氨水中加入一定量的NaOH溶液时,Kb值是否会发生变化?
(3)若该氨水的起始浓度为0.01 mol·L-1,则达到电离平衡时溶液中OH-的物质的量浓度为
您最近一年使用:0次
解题方法
6 . 含物质的量相同的CH3COOH和CH3COONa混合溶液中:
(1)写出所有电离、水解离子方程式:_______ 。
(2)粒子浓度由大到小顺序为_______ 。
(3)电荷守恒:_______ 。
(4)物料守恒:_______ 。
(1)写出所有电离、水解离子方程式:
(2)粒子浓度由大到小顺序为
(3)电荷守恒:
(4)物料守恒:
您最近一年使用:0次
名校
7 . 下列事实可以证明NH3·H2O是弱碱的是
| A.氨水能跟CuCl2溶液反应生成Cu(OH)2沉淀 |
| B.铵盐受热易分解,放出氨气 |
| C.0.1mol·L-1的氨水可以使酚酞溶液变红 |
| D.0.1mol·L-1的氨水中,c(OH-)约为0.001mol·L-1 |
您最近一年使用:0次
2023-09-08更新
|
269次组卷
|
6卷引用:鲁科版(2019)高二选择性必修第一册第3章 物质在水溶液中的行为 第1节 水与水溶液 课时1 水的电离 电解质在水溶液中的存在形态
解题方法
8 . 常温下,0.1mol/L的下列五种溶液:
①CH3COOH②NaClO③NH4Cl④NaCl⑤CH3COONa,其pH由大到小的排列顺序是_______ 。
①CH3COOH②NaClO③NH4Cl④NaCl⑤CH3COONa,其pH由大到小的排列顺序是
您最近一年使用:0次
9 . 已知Ka(CH3COOH)=1.75×10-5,试计算0.1 mol·L-1 CH3COOH溶液中H+的浓度(写出计算过程) ______ 。
您最近一年使用:0次
10 . 写出下列电解质在水溶液中的电离方程式。
(1)HClO4:___________ 。
(2)HClO:___________ 。
(3)NaHSO3:___________ 。
(1)HClO4:
(2)HClO:
(3)NaHSO3:
您最近一年使用:0次



