1 . 请你查找相关数据,回答下列问题。
(1) 、
、 、
、 三种一元酸的酸性由强到弱的顺序是
三种一元酸的酸性由强到弱的顺序是_______ 。
(2)相同物质的量浓度的 溶液、
溶液、 溶液、
溶液、 溶液的
溶液的 由大到小的顺序是
由大到小的顺序是_______ 。
(3) 溶液中含有
溶液中含有_____ 微粒?请将溶液中各种离子的浓度按由大到小的顺序排列_____ 。
(4)向 溶液中加入少量盐酸,溶液中各种微粒的浓度将如何变化
溶液中加入少量盐酸,溶液中各种微粒的浓度将如何变化_____ ?
(5)加热 溶液,溶液中各种微粒的浓度将如何变化?
溶液,溶液中各种微粒的浓度将如何变化?_____
(1)
 、
、 、
、 三种一元酸的酸性由强到弱的顺序是
三种一元酸的酸性由强到弱的顺序是(2)相同物质的量浓度的
 溶液、
溶液、 溶液、
溶液、 溶液的
溶液的 由大到小的顺序是
由大到小的顺序是(3)
 溶液中含有
溶液中含有(4)向
 溶液中加入少量盐酸,溶液中各种微粒的浓度将如何变化
溶液中加入少量盐酸,溶液中各种微粒的浓度将如何变化(5)加热
 溶液,溶液中各种微粒的浓度将如何变化?
溶液,溶液中各种微粒的浓度将如何变化?
您最近一年使用:0次
2 . 酸碱指示剂一般是有机弱酸或有机弱城。例如,石蕊是一种有机弱酸,如果用 表示石蕊分子,
表示石蕊分子, 在水中发生电离:
在水中发生电离: ,请你用电离平衡的知识解释其指示溶液酸碱性的化学原理。
,请你用电离平衡的知识解释其指示溶液酸碱性的化学原理。_____
 表示石蕊分子,
表示石蕊分子, 在水中发生电离:
在水中发生电离: ,请你用电离平衡的知识解释其指示溶液酸碱性的化学原理。
,请你用电离平衡的知识解释其指示溶液酸碱性的化学原理。
您最近一年使用:0次
解题方法
3 . 1.下列哪些事实能说明醋酸是弱酸?_____
(1)醋酸不易腐蚀衣服。
(2) 的
的 溶液的
溶液的 约为9。
约为9。
(3)进行中和滴定时,等体积等物质的量浓度的 溶液比等体积等物质的量浓度的
溶液比等体积等物质的量浓度的 溶液消耗的
溶液消耗的 溶液多。
溶液多。
(4) 的
的 溶液的
溶液的 约为3。
约为3。
(5)相同体积的 均等于4的盐酸和
均等于4的盐酸和 溶液,用同一物质的量浓度的
溶液,用同一物质的量浓度的 溶液中和,
溶液中和, 溶液消耗的
溶液消耗的 溶液多。
溶液多。
(6)镁粉与一定量稀硫酸反应,如果向其中加入少量醋酸钠,可以降低反应速率,但不改变产生气体的总量。
(1)醋酸不易腐蚀衣服。
(2)
 的
的 溶液的
溶液的 约为9。
约为9。(3)进行中和滴定时,等体积等物质的量浓度的
 溶液比等体积等物质的量浓度的
溶液比等体积等物质的量浓度的 溶液消耗的
溶液消耗的 溶液多。
溶液多。(4)
 的
的 溶液的
溶液的 约为3。
约为3。(5)相同体积的
 均等于4的盐酸和
均等于4的盐酸和 溶液,用同一物质的量浓度的
溶液,用同一物质的量浓度的 溶液中和,
溶液中和, 溶液消耗的
溶液消耗的 溶液多。
溶液多。(6)镁粉与一定量稀硫酸反应,如果向其中加入少量醋酸钠,可以降低反应速率,但不改变产生气体的总量。
您最近一年使用:0次
4 . 物质在水溶液中的行为包括电离和溶解等,人们可以用电离平衡常数和溶度积常数分别描述弱电解质的电离平衡和难溶电解质的沉淀溶解平衡。请你尝试用图示的方法总结物质在水溶液中的行为。______
您最近一年使用:0次
5 . 在22℃时,用 传感器测量
传感器测量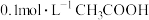 溶液的
溶液的 ,测得
,测得 约为3.0;然后,逐渐升高温度至29℃时,测得
约为3.0;然后,逐渐升高温度至29℃时,测得 降至2.9。加热过程中
降至2.9。加热过程中 变化的原因是
变化的原因是_______ 。
 传感器测量
传感器测量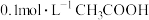 溶液的
溶液的 ,测得
,测得 约为3.0;然后,逐渐升高温度至29℃时,测得
约为3.0;然后,逐渐升高温度至29℃时,测得 降至2.9。加热过程中
降至2.9。加热过程中 变化的原因是
变化的原因是
您最近一年使用:0次
解题方法
6 . 请你列举能证明氨水中存在电离平衡的实验事实________ 。
您最近一年使用:0次
7 . 现有 的
的 溶液,判断当下列条件变化时其中发生的变化。
溶液,判断当下列条件变化时其中发生的变化。
 的
的 溶液,判断当下列条件变化时其中发生的变化。
溶液,判断当下列条件变化时其中发生的变化。| 变化条件 | 醋酸的电离平衡如何移动 |  浓度 浓度 |  浓度 浓度 |  浓度 浓度 |
| 加入水 | ||||
| 加入少量醋酸钠固体 | ||||
| 通入少量氯化氢气体 | ||||
滴加少量 溶液 溶液 |
您最近一年使用:0次
解题方法
8 . 有下列四种物质:
① ②
② ③
③ ④
④
(1)属于强电解质的是_______ ,属于弱电解质的是_______ (填序号)
(2)请写出下列物质的电离方程式。
 :
:_______ ;
 :
:_______ ;
 :
:_______ ;
 :
:_______ 。
①
 ②
② ③
③ ④
④
(1)属于强电解质的是
(2)请写出下列物质的电离方程式。
 :
: :
: :
: :
:
您最近一年使用:0次
2022-11-26更新
|
500次组卷
|
2卷引用:2019鲁科版高中化学选择性必修1第3章第1节 水与水溶液课后习题
9 .  溶液是实验室中的常用试剂。
溶液是实验室中的常用试剂。
(1)请分析 溶液的组成:
溶液的组成:_______ 。
(2)下列说法中,能够解释 溶液呈酸性的是 。
溶液呈酸性的是 。
(3)实验测得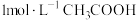 溶液的
溶液的 ,由此确定
,由此确定 是弱电解质,理由是
是弱电解质,理由是_______ 。
 溶液是实验室中的常用试剂。
溶液是实验室中的常用试剂。(1)请分析
 溶液的组成:
溶液的组成:(2)下列说法中,能够解释
 溶液呈酸性的是 。
溶液呈酸性的是 。A. 中含氢元素 中含氢元素 |
B. 电离使溶液中 电离使溶液中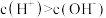 |
C. 能电离出 能电离出 |
D. 能促使水电离出更多的 能促使水电离出更多的 |
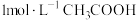 溶液的
溶液的 ,由此确定
,由此确定 是弱电解质,理由是
是弱电解质,理由是
您最近一年使用:0次
解题方法
10 . 用实验确定某酸HA是否为弱电解质,两位同学的方案如下:
甲:①称取一定质量的HA,配制0.1mol•L-1的溶液100mL;②用pH计测出该溶液的pH,根据测定结果即可判断HA是否为弱电解质。
乙:①用已知物质的量浓度的HA溶液、盐酸分别配制pH=2的两种酸溶液各100mL;②分别取这两种溶液各10mL,加水稀释为100mL;③各取相同体积的两种稀释液于两支试管中,同时加入相同纯度的锌粒,根据观察到的实验现象即可判断HA是否为弱电解质。
(1)在两个方案的步骤①中,都要用到的定量仪器是____ 。
(2)甲方案中,若测得溶液的pH____ (填“>”“<”或“=”)1,则可说明HA是弱电解质。
(3)乙方案中,能说明HA是弱电解质的现象是____ (填字母序号)。
A.装盐酸的试管中放出H2的速率较大
B.装HA溶液的试管中放出H2的速率较大
C.两支试管中产生气体的速率一样大
(4)请你对两种方案的可行性作出评价____ 。
(5)请你再设计一个合理而比较容易进行的实验方案(药品可任取),并作简明扼要的表述_____ 。
甲:①称取一定质量的HA,配制0.1mol•L-1的溶液100mL;②用pH计测出该溶液的pH,根据测定结果即可判断HA是否为弱电解质。
乙:①用已知物质的量浓度的HA溶液、盐酸分别配制pH=2的两种酸溶液各100mL;②分别取这两种溶液各10mL,加水稀释为100mL;③各取相同体积的两种稀释液于两支试管中,同时加入相同纯度的锌粒,根据观察到的实验现象即可判断HA是否为弱电解质。
(1)在两个方案的步骤①中,都要用到的定量仪器是
(2)甲方案中,若测得溶液的pH
(3)乙方案中,能说明HA是弱电解质的现象是
A.装盐酸的试管中放出H2的速率较大
B.装HA溶液的试管中放出H2的速率较大
C.两支试管中产生气体的速率一样大
(4)请你对两种方案的可行性作出评价
(5)请你再设计一个合理而比较容易进行的实验方案(药品可任取),并作简明扼要的表述
您最近一年使用:0次
2022-11-25更新
|
80次组卷
|
2卷引用:苏教2020版选择性必修1专题3第四单元 沉淀溶解平衡课后习题



