1 . 下列实验操作、现象和所得出的结论均正确的是
选项 | 实验操作、现象 | 结论 |
A | 取两支试管,均加入 酸性溶液,然后向一支试管中加入 酸性溶液,然后向一支试管中加入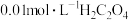 溶液 溶液 ,向另一支试管中加入 ,向另一支试管中加入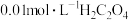 溶液 溶液 ,第一支试管中褪色时间较长 ,第一支试管中褪色时间较长 |  浓度越大,反应速率越快 浓度越大,反应速率越快 |
B | 向淀粉溶液中加适量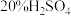 溶液,加热一段时间后冷却,再滴入碘水,溶液未变蓝 溶液,加热一段时间后冷却,再滴入碘水,溶液未变蓝 | 淀粉完全水解 |
C | 在氨水中滴入酚酞溶液,加热一段时间,溶液红色先变深后变浅 | 升高温度,一水合氨的电离程度先增大后减小 |
D | 取两支试管,均加入等体积等浓度的双氧水,然后向试管①中加入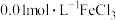 溶液 溶液 ,向试管②中加入 ,向试管②中加入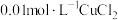 溶液 溶液 ,试管①产生气泡快 ,试管①产生气泡快 | 加入 溶液时,双氧水分解反应的活化能较大 溶液时,双氧水分解反应的活化能较大 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
2 . 常温下 下列物质的水溶液,加热到
下列物质的水溶液,加热到 ,溶液
,溶液 几乎不变的是
几乎不变的是
 下列物质的水溶液,加热到
下列物质的水溶液,加热到 ,溶液
,溶液 几乎不变的是
几乎不变的是| A.氢氧化钾 | B.硫酸铵 | C.盐酸 | D.硫酸 |
您最近半年使用:0次
名校
3 . 某种市售白醋的说明书标明醋酸的质量分数为6%,密度接近 。已知:①常温下,该溶液中醋酸的电离度为0.4%(电离度
。已知:①常温下,该溶液中醋酸的电离度为0.4%(电离度 ),②
),② 。下列关于该市售白醋的说法错误的是
。下列关于该市售白醋的说法错误的是
 。已知:①常温下,该溶液中醋酸的电离度为0.4%(电离度
。已知:①常温下,该溶液中醋酸的电离度为0.4%(电离度 ),②
),② 。下列关于该市售白醋的说法错误的是
。下列关于该市售白醋的说法错误的是A. | B.常温下加水稀释, 增大 增大 |
C.用炒锅烹饪时,可增大醋酸的 | D.可用于除去烧水壶中少量的水垢 |
您最近半年使用:0次
名校
解题方法
4 . 室温下,有浓度均为0.2mol·L-1的下列五种溶液,请回答问题。
①HCl ②NaCl ③CH3COOH ④CH3COONa ⑤Na2CO3
资料:室温下,醋酸Ka=1.7×10-5;碳酸Ka1=4.4×10-7,Ka2=4.7×10-11;次氯酸Ka=4.0×10–8
(1)上述溶液中水的电离被抑制的是________ (填序号,下同),水的电离被促进的是_______ ,用离子方程式表示促进水电离程度最大的溶质与水的作用:________ 。
(2)上述溶液的pH由大到小的顺序为___________ 。
(3)等体积的①和③分别于足量的锌粉反应,起始速率:①____ ③(填“<”、“=”或“>”);生成氢气的量:①____ ③(填“<”、“=”或“>”)。
(4)比较溶液③和④中CH3COO-的物质的量浓度:③____ ④(填“<”、“=”或“>”)。
(5)向溶液①中加水稀释至原体积的2倍,恢复至室温,所得溶液的pH为______ 。
(6)依据电离平衡常数数据,下列方程式书写合理的是______ 。(填字母)
a.CH3COONa溶液中滴加次氯酸:HClO+CH3COONa=CH3COOH+NaClO
b.Na2CO3溶液中滴加少量醋酸:CH3COOH+Na2CO3=NaHCO3+CH3COONa
c.NaClO溶液中通入CO2:CO2+H2O+2NaClO=Na2CO3+2HClO
d.NaHCO3溶液中滴加过量氯水:NaHCO3+Cl2=NaCl+HClO+CO2↑
(7)常温下0.1mol/LCH3COOH溶液加水稀释后,下列各项中数值变大的是______ 。
a.c(H+) b. c.c(H+)·c(OH−) d.
c.c(H+)·c(OH−) d.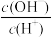 e.
e.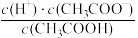
(8)在一条件下,CH3COOH溶液中存在电离平衡:CH3COOH CH3COO−+H+ ΔH>0,下列方法中,可以使0.10mol·L−1CH3COOH溶液中CH3COOH电离程度增大的是
CH3COO−+H+ ΔH>0,下列方法中,可以使0.10mol·L−1CH3COOH溶液中CH3COOH电离程度增大的是_______ 。
a.加入少量0.10mol·L−1的稀盐酸 b.加热
c.加水稀释至0.010mol·L−1 d.加入少量冰醋酸
(9)体积为10mLpH=2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程pH变化如图所示。则HX的电离平衡常数______ (填“大于”、“等于”或“小于”下同)醋酸的平衡常数,稀释后,HX溶液中水电离出来的c(H+)______ 醋酸溶液水电离出来c(H+)。

①HCl ②NaCl ③CH3COOH ④CH3COONa ⑤Na2CO3
资料:室温下,醋酸Ka=1.7×10-5;碳酸Ka1=4.4×10-7,Ka2=4.7×10-11;次氯酸Ka=4.0×10–8
(1)上述溶液中水的电离被抑制的是
(2)上述溶液的pH由大到小的顺序为
(3)等体积的①和③分别于足量的锌粉反应,起始速率:①
(4)比较溶液③和④中CH3COO-的物质的量浓度:③
(5)向溶液①中加水稀释至原体积的2倍,恢复至室温,所得溶液的pH为
(6)依据电离平衡常数数据,下列方程式书写合理的是
a.CH3COONa溶液中滴加次氯酸:HClO+CH3COONa=CH3COOH+NaClO
b.Na2CO3溶液中滴加少量醋酸:CH3COOH+Na2CO3=NaHCO3+CH3COONa
c.NaClO溶液中通入CO2:CO2+H2O+2NaClO=Na2CO3+2HClO
d.NaHCO3溶液中滴加过量氯水:NaHCO3+Cl2=NaCl+HClO+CO2↑
(7)常温下0.1mol/LCH3COOH溶液加水稀释后,下列各项中数值变大的是
a.c(H+) b.
 c.c(H+)·c(OH−) d.
c.c(H+)·c(OH−) d.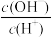 e.
e.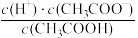
(8)在一条件下,CH3COOH溶液中存在电离平衡:CH3COOH
 CH3COO−+H+ ΔH>0,下列方法中,可以使0.10mol·L−1CH3COOH溶液中CH3COOH电离程度增大的是
CH3COO−+H+ ΔH>0,下列方法中,可以使0.10mol·L−1CH3COOH溶液中CH3COOH电离程度增大的是a.加入少量0.10mol·L−1的稀盐酸 b.加热
c.加水稀释至0.010mol·L−1 d.加入少量冰醋酸
(9)体积为10mLpH=2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程pH变化如图所示。则HX的电离平衡常数

您最近半年使用:0次
名校
5 . 下列方法中不能使0.10mol/L氨水中NH3·H2O电离程度增大的是
| A.加水稀释 | B.微热溶液 |
| C.滴加少量浓盐酸 | D.加入少量氯化铵晶体 |
您最近半年使用:0次
名校
6 . 某二元弱酸H2A在常温下的电离常数 ,
,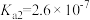 。下列说法不正确的是
。下列说法不正确的是
 ,
,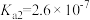 。下列说法不正确的是
。下列说法不正确的是| A.升温会使H2A溶液的pH值变小 |
| B.0.1mol∙L-1NaHA溶液呈酸性 |
| C.0.1mol∙L-1H2A溶液中:c(H+)>2c(A2-)+c(HA-)>c(OH-) |
D.向H2A溶液中加入少量NaOH固体,则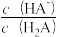 变小 变小 |
您最近半年使用:0次
2024-01-09更新
|
132次组卷
|
2卷引用:广东省东莞市东莞中学2023-2024学年高二上学期期中考试化学试题
名校
7 . 醋酸溶液中存在平衡: ,下列措施既能提高醋酸电离度又能使
,下列措施既能提高醋酸电离度又能使 增大的是
增大的是
 ,下列措施既能提高醋酸电离度又能使
,下列措施既能提高醋酸电离度又能使 增大的是
增大的是| A.升高温度 | B.加水稀释 | C.加 固体 固体 | D.通入 气体 气体 |
您最近半年使用:0次
名校
8 . I. 时,三种酸的电离平衡常数如下:
时,三种酸的电离平衡常数如下:
回答下列问题:
(1)一般情况下,当温度升高时,
___________ (填“增大”“减小”或“不变”)。
(2)下列能使醋酸溶液中 的电离程度增大,而电离平衡常数不变的是___________。
的电离程度增大,而电离平衡常数不变的是___________。
(3)依上表数据写出向NaClO溶液中通少量 的离子方程式:
的离子方程式:___________ 。
(4)pH相同的NaClO和 溶液,其溶液的物质的量浓度的大小关系是
溶液,其溶液的物质的量浓度的大小关系是
____ NaClO(填“ ”“
”“ ”或“
”或“ ”,下同),两溶液中:c(Na+)−c(ClO-)
”,下同),两溶液中:c(Na+)−c(ClO-)____ c(K+)−c(CH3COO-)。
II.常温下,用0.2000mol•L-1盐酸滴定25mL0.2000mol•L-1Na2CO3溶液(溶液均为新配制),其滴定曲线如图所示(忽略溶液混合时体积和温度的变化)。回答下列问题:
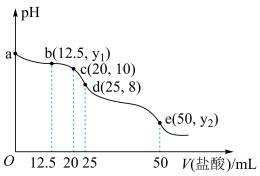
(5)往0.2000mol•L-1Na2CO3溶液中滴入2~3滴无色酚酞,溶液颜色会由无色变为________ ,判断的依据___________ (用离子方程式表示)。
(6)b点混合溶液中主要的溶质有Na2CO3、NaCl和___________ (填化学式),此时 =
=___________ 。
(7)c点混合溶液中,c(Na+)、c(CO )、(HCO
)、(HCO )、c(OH-)、c(H+)由大到小的顺序为
)、c(OH-)、c(H+)由大到小的顺序为___________ 。
(8)d点混合溶液中,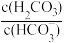 的数值是
的数值是___________ 。
 时,三种酸的电离平衡常数如下:
时,三种酸的电离平衡常数如下:| 化学式 | HClO |  |  |
| 电离平衡常数 |  |  | Ka1=4×10-7,Ka2=5×10-11 |
(1)一般情况下,当温度升高时,

(2)下列能使醋酸溶液中
 的电离程度增大,而电离平衡常数不变的是___________。
的电离程度增大,而电离平衡常数不变的是___________。| A.升高温度 | B.加水稀释 |
C.加少量的 固体 固体 | D.加少量氢氧化钠浓溶液 |
(3)依上表数据写出向NaClO溶液中通少量
 的离子方程式:
的离子方程式:(4)pH相同的NaClO和
 溶液,其溶液的物质的量浓度的大小关系是
溶液,其溶液的物质的量浓度的大小关系是
 ”“
”“ ”或“
”或“ ”,下同),两溶液中:c(Na+)−c(ClO-)
”,下同),两溶液中:c(Na+)−c(ClO-)II.常温下,用0.2000mol•L-1盐酸滴定25mL0.2000mol•L-1Na2CO3溶液(溶液均为新配制),其滴定曲线如图所示(忽略溶液混合时体积和温度的变化)。回答下列问题:

(5)往0.2000mol•L-1Na2CO3溶液中滴入2~3滴无色酚酞,溶液颜色会由无色变为
(6)b点混合溶液中主要的溶质有Na2CO3、NaCl和
 =
=(7)c点混合溶液中,c(Na+)、c(CO
 )、(HCO
)、(HCO )、c(OH-)、c(H+)由大到小的顺序为
)、c(OH-)、c(H+)由大到小的顺序为(8)d点混合溶液中,
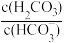 的数值是
的数值是
您最近半年使用:0次
名校
解题方法
9 .  的捕集和利用能有效助力“碳中和”和“碳达峰”。
的捕集和利用能有效助力“碳中和”和“碳达峰”。
Ⅰ.工业上常用饱和 溶液回收捕集废气中的
溶液回收捕集废气中的 和
和 ,其流程为:
,其流程为:
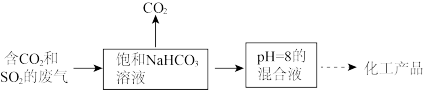
已知:该温度下, 、
、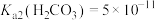 、
、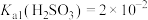 、
、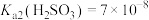 。
。
(1)①写出 的电离平衡常数表达式
的电离平衡常数表达式
___________ 。
② 的混合溶液中含碳微粒主要为
的混合溶液中含碳微粒主要为___________ (不考虑溶液中的 分子),
分子),
___________ 。
Ⅱ.工业上用 与
与 催化合成甲醇,相关反应为:
催化合成甲醇,相关反应为:
(2)已知平衡常数 、
、 、
、 随温度变化的曲线如图所示:
随温度变化的曲线如图所示:
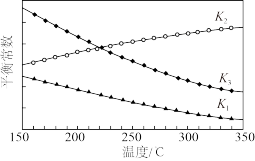
①
___________ 0(填“>”或“<”),判断依据为___________ 。
②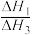 取值范围为
取值范围为___________ 。
(3)一定条件下,向2L的恒容密闭容器中充入3mol 和1mol
和1mol 只发生反应ⅰ和ⅱ,达到平衡状态后,测得平衡时气体压强是开始的0.7倍,
只发生反应ⅰ和ⅱ,达到平衡状态后,测得平衡时气体压强是开始的0.7倍, 的转化率为80%。
的转化率为80%。
①平衡时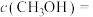
___________ mol⋅L-1。
②反应ii的化学平衡常数
___________ 。
 的捕集和利用能有效助力“碳中和”和“碳达峰”。
的捕集和利用能有效助力“碳中和”和“碳达峰”。Ⅰ.工业上常用饱和
 溶液回收捕集废气中的
溶液回收捕集废气中的 和
和 ,其流程为:
,其流程为:
已知:该温度下,
 、
、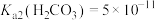 、
、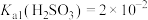 、
、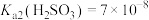 。
。(1)①写出
 的电离平衡常数表达式
的电离平衡常数表达式
②
 的混合溶液中含碳微粒主要为
的混合溶液中含碳微粒主要为 分子),
分子),
Ⅱ.工业上用
 与
与 催化合成甲醇,相关反应为:
催化合成甲醇,相关反应为:| 相关反应 |  (kJ·mol-1) (kJ·mol-1) | 化学平衡常数(K) | |
| ⅰ |  |  |  |
| ⅱ |  |  |  |
| ⅲ |  |  |  |
(2)已知平衡常数
 、
、 、
、 随温度变化的曲线如图所示:
随温度变化的曲线如图所示:
①

②
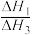 取值范围为
取值范围为(3)一定条件下,向2L的恒容密闭容器中充入3mol
 和1mol
和1mol 只发生反应ⅰ和ⅱ,达到平衡状态后,测得平衡时气体压强是开始的0.7倍,
只发生反应ⅰ和ⅱ,达到平衡状态后,测得平衡时气体压强是开始的0.7倍, 的转化率为80%。
的转化率为80%。①平衡时
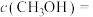
②反应ii的化学平衡常数

您最近半年使用:0次
10 . 醋酸溶液中存在电离平衡: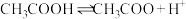 ,下列叙述
,下列叙述不正确 的是
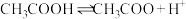 ,下列叙述
,下列叙述| A.升高温度,醋酸的电离常数Ka增大 |
B.0.01 醋酸加水稀释,溶液中导电粒子的数目增大 醋酸加水稀释,溶液中导电粒子的数目增大 |
| C.CH3COOH溶液中加少量的CH3COONa固体,平衡逆向移动 |
| D.25℃时,加入少量冰醋酸会使溶液中c(H+)和CH3COOH电离度都增大 |
您最近半年使用:0次



