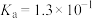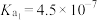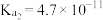解题方法
1 . 在氨水中存在电离平衡: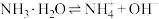 ,下列情况能使电离平衡向左移动的是
,下列情况能使电离平衡向左移动的是
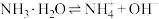 ,下列情况能使电离平衡向左移动的是
,下列情况能使电离平衡向左移动的是| A.加水 | B.通HCl | C.加NH4Cl固体 | D.加CH3COOH |
您最近半年使用:0次
2 . 对于常温下 的乙酸溶液,下列说法正确的是
的乙酸溶液,下列说法正确的是
 的乙酸溶液,下列说法正确的是
的乙酸溶液,下列说法正确的是A.用等浓度 溶液中和等体积该乙酸溶液与 溶液中和等体积该乙酸溶液与 的盐酸,乙酸消耗 的盐酸,乙酸消耗 溶液的体积多 溶液的体积多 |
| B.加水稀释到原体积的10倍后溶液pH变为4 |
| C.加入少量乙酸钠固体,溶液pH降低 |
D.乙酸的电离方程式为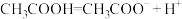 |
您最近半年使用:0次
3 . 稀氨水中存在着下列平衡:NH3·H2O⇌ +OH-,若要使平衡向左移动,同时使c(OH-)增大,应加入的物质或采取的措施是
+OH-,若要使平衡向左移动,同时使c(OH-)增大,应加入的物质或采取的措施是
①NH4Cl固体②硫酸③NaOH固体④水⑤加热⑥加入少量MgSO4固体
 +OH-,若要使平衡向左移动,同时使c(OH-)增大,应加入的物质或采取的措施是
+OH-,若要使平衡向左移动,同时使c(OH-)增大,应加入的物质或采取的措施是①NH4Cl固体②硫酸③NaOH固体④水⑤加热⑥加入少量MgSO4固体
| A.①②③⑤ | B.③⑥ | C.③ | D.③⑤ |
您最近半年使用:0次
4 . 在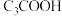 溶液中存在下列电离平衡:
溶液中存在下列电离平衡: 。
。
(1)加入少量的冰醋酸,平衡将_______ ,溶液中 将
将_______  填
填 增大
增大 减小
减小 或
或 不变
不变 。
。
(2)加入一定量蒸馏水,平衡将_______ ,溶液中 将
将_______  填
填 增大
增大 减小
减小 或
或 不变
不变 。
。
(3)加入少量 盐酸,平衡将
盐酸,平衡将_______ ,溶液 将
将_______  填
填 增大
增大 减小
减小 或
或 不变
不变 。
。
(4)加入 溶液,平衡将
溶液,平衡将_______ ,溶液中 将
将_______  填
填 增大
增大 减小
减小 或
或 不变
不变 。
。
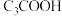 溶液中存在下列电离平衡:
溶液中存在下列电离平衡: 。
。(1)加入少量的冰醋酸,平衡将
 将
将 填
填 增大
增大 减小
减小 或
或 不变
不变 。
。(2)加入一定量蒸馏水,平衡将
 将
将 填
填 增大
增大 减小
减小 或
或 不变
不变 。
。(3)加入少量
 盐酸,平衡将
盐酸,平衡将 将
将 填
填 增大
增大 减小
减小 或
或 不变
不变 。
。(4)加入
 溶液,平衡将
溶液,平衡将 将
将 填
填 增大
增大 减小
减小 或
或 不变
不变 。
。
您最近半年使用:0次
名校
5 . 液氨与纯水类似,也存在微弱的电离: ,T℃时,液氨的离子积常数
,T℃时,液氨的离子积常数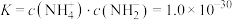 ,若用定义pH的方式来规定
,若用定义pH的方式来规定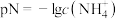 ,则下列叙述正确的是
,则下列叙述正确的是
 ,T℃时,液氨的离子积常数
,T℃时,液氨的离子积常数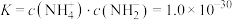 ,若用定义pH的方式来规定
,若用定义pH的方式来规定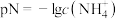 ,则下列叙述正确的是
,则下列叙述正确的是| A.其他条件不变,增加液氨的量,电离平衡正向移动 |
B.液氨达到电离平衡时 |
| C.T℃时1L溶解有0.001molNH4Cl的液氨溶液,其pN=3 |
| D.一定温度下,向液氨中加入氯化铵固体,电离平衡逆向移动,K值减小 |
您最近半年使用:0次
6 . 已知25℃时,部分弱酸的电离平衡常数如下表:
(1)25℃时,在 的
的 溶液中由水电离出来的
溶液中由水电离出来的
__________ .
(2) 溶液显
溶液显_________ 性,用离子方程式表示原因____________ ;请写出少量 通入到过量的
通入到过量的 溶液中发生反应的离子方程式:
溶液中发生反应的离子方程式:_________________________ .
(3) 溶液中加少量的
溶液中加少量的 固体,电离平衡
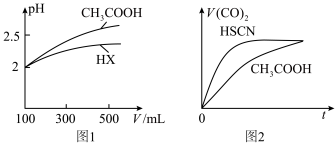
固体,电离平衡__________ 移动(填“正向”、“逆向”或“不”);体积均为100mL,pH均为2的 与一元酸HX溶液,加水稀释过程中pH与溶液体积的关系如图1所示,则
与一元酸HX溶液,加水稀释过程中pH与溶液体积的关系如图1所示,则
_________ (填“>”或“<”) .
.
(4)25℃时,将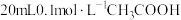 溶液和
溶液和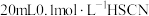 溶液分别与
溶液分别与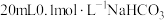 溶液混合,实验测得产生的气体体积
溶液混合,实验测得产生的气体体积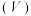 随时间
随时间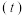 的变化如图2所示:反应初始阶段两种溶液产生
的变化如图2所示:反应初始阶段两种溶液产生 气体的速率存在明显差异的原因是
气体的速率存在明显差异的原因是________________________ ;假设混合后,两份溶液的体积仍相等,则反应结束后所得两溶液中,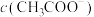
_____________ (填“>”、“<”或“=”) 
弱酸 |
|
|
|
|
电离平衡常数 |
|
|
|
|
(1)25℃时,在
 的
的 溶液中由水电离出来的
溶液中由水电离出来的
(2)
 溶液显
溶液显 通入到过量的
通入到过量的 溶液中发生反应的离子方程式:
溶液中发生反应的离子方程式:(3)
 溶液中加少量的
溶液中加少量的 固体,电离平衡
固体,电离平衡 与一元酸HX溶液,加水稀释过程中pH与溶液体积的关系如图1所示,则
与一元酸HX溶液,加水稀释过程中pH与溶液体积的关系如图1所示,则
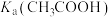 .
.
(4)25℃时,将
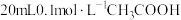 溶液和
溶液和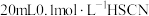 溶液分别与
溶液分别与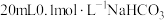 溶液混合,实验测得产生的气体体积
溶液混合,实验测得产生的气体体积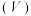 随时间
随时间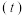 的变化如图2所示:反应初始阶段两种溶液产生
的变化如图2所示:反应初始阶段两种溶液产生 气体的速率存在明显差异的原因是
气体的速率存在明显差异的原因是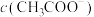

您最近半年使用:0次
名校
7 . 下列事实中,能说明 是弱碱的有
是弱碱的有
①常温下,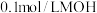 溶液中
溶液中
②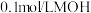 溶液可以使酚酞试液变红
溶液可以使酚酞试液变红
③ 的
的 溶液与等体积
溶液与等体积 的盐酸恰好完全反应
的盐酸恰好完全反应
④常温下,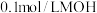 溶液的导电能力比
溶液的导电能力比 溶液弱
溶液弱
⑤常温下,向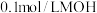 溶液中加入少量
溶液中加入少量 固体,溶液
固体,溶液 减小
减小
 是弱碱的有
是弱碱的有①常温下,
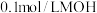 溶液中
溶液中
②
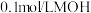 溶液可以使酚酞试液变红
溶液可以使酚酞试液变红③
 的
的 溶液与等体积
溶液与等体积 的盐酸恰好完全反应
的盐酸恰好完全反应④常温下,
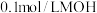 溶液的导电能力比
溶液的导电能力比 溶液弱
溶液弱⑤常温下,向
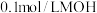 溶液中加入少量
溶液中加入少量 固体,溶液
固体,溶液 减小
减小| A.①④⑤ | B.①③④ | C.②③⑤ | D.③④⑤ |
您最近半年使用:0次
名校
8 . 在一定温度下,冰醋酸加水稀释过程中的导电能力变化如图所示,请回答:
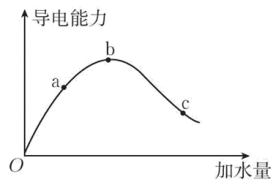
(1)“O”点导电能力为0的理由是___________ 。
(2)a、b、c三点,溶液中c(H+)由大到小的顺序为___________ 。
(3)若使c点溶液中c(CH3COO-)增大,溶液的c(H+)减小,可采取的措施有:
①___________
②___________
③___________ 。

(1)“O”点导电能力为0的理由是
(2)a、b、c三点,溶液中c(H+)由大到小的顺序为
(3)若使c点溶液中c(CH3COO-)增大,溶液的c(H+)减小,可采取的措施有:
①
②
③
您最近半年使用:0次
名校
9 . 水溶液存在离子平衡,回答下列问题:
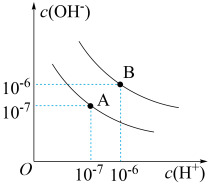
(1)水的电离平衡曲线如图所示。若以A点表示 时水在电离平衡时的离子浓度。当温度升到
时水在电离平衡时的离子浓度。当温度升到 时,水的电离平衡状态到B点,该温度时
时,水的电离平衡状态到B点,该温度时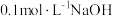 溶液
溶液 为
为__________ 。
(2)一定温度下,向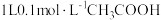 溶液中加入
溶液中加入 固体,则醋酸的电离平衡向
固体,则醋酸的电离平衡向__________ (填“正”或“逆”)反应方向移动:水的电离程度将__________ (填“增大”、“减小”或“不变”)。
(3)常温下,在 硫酸铜溶液中加入氢氧化钠稀溶液,充分搅拌有浅蓝色氢氧化铜沉淀生成,当溶液的
硫酸铜溶液中加入氢氧化钠稀溶液,充分搅拌有浅蓝色氢氧化铜沉淀生成,当溶液的 为8时,
为8时,
_________ 。(已知常温时 的
的 )
)
(4)常温下,向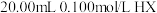 (一元酸)溶液中滴加
(一元酸)溶液中滴加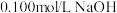 过程中
过程中 变化如图所示。
变化如图所示。
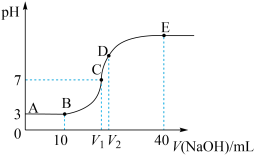
① 的电离常数为
的电离常数为__________ 。
②C点溶液中
_________  (填“>”、“<”或“=”,下同)
(填“>”、“<”或“=”,下同)
③D点时二者恰好完全反应,此时溶液的
_________ 7(填“>”、“<”或“=”),原因是__________ (用离子方程式表示)。

(1)水的电离平衡曲线如图所示。若以A点表示
 时水在电离平衡时的离子浓度。当温度升到
时水在电离平衡时的离子浓度。当温度升到 时,水的电离平衡状态到B点,该温度时
时,水的电离平衡状态到B点,该温度时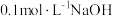 溶液
溶液 为
为(2)一定温度下,向
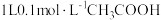 溶液中加入
溶液中加入 固体,则醋酸的电离平衡向
固体,则醋酸的电离平衡向(3)常温下,在
 硫酸铜溶液中加入氢氧化钠稀溶液,充分搅拌有浅蓝色氢氧化铜沉淀生成,当溶液的
硫酸铜溶液中加入氢氧化钠稀溶液,充分搅拌有浅蓝色氢氧化铜沉淀生成,当溶液的 为8时,
为8时,
 的
的 )
)(4)常温下,向
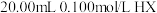 (一元酸)溶液中滴加
(一元酸)溶液中滴加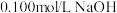 过程中
过程中 变化如图所示。
变化如图所示。
①
 的电离常数为
的电离常数为②C点溶液中

 (填“>”、“<”或“=”,下同)
(填“>”、“<”或“=”,下同)③D点时二者恰好完全反应,此时溶液的

您最近半年使用:0次
名校
10 . 下列方法中不能使0.10mol/L氨水中NH3·H2O电离程度增大的是
| A.加水稀释 | B.微热溶液 |
| C.滴加少量浓盐酸 | D.加入少量氯化铵晶体 |
您最近半年使用:0次