2023·海南·高考真题
真题
1 . 25℃下, 水溶液的pH随其浓度的变化关系如图所示。下列说法正确的是
水溶液的pH随其浓度的变化关系如图所示。下列说法正确的是
 水溶液的pH随其浓度的变化关系如图所示。下列说法正确的是
水溶液的pH随其浓度的变化关系如图所示。下列说法正确的是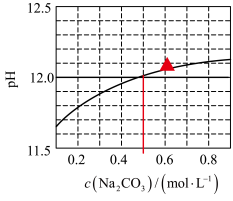
A.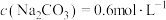 时,溶液中 时,溶液中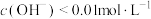 |
B. 水解程度随其浓度增大而减小 水解程度随其浓度增大而减小 |
C.在水中 的 的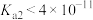 |
D. 的 的 溶液和 溶液和 的 的 溶液等体积混合,得到的溶液 溶液等体积混合,得到的溶液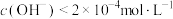 |
您最近一年使用:0次
2023-08-03更新
|
4430次组卷
|
6卷引用:实验05 盐类水解的应用-【同步实验课】2023-2024学年高二化学教材实验大盘点(人教版2019选择性必修1)
(已下线)实验05 盐类水解的应用-【同步实验课】2023-2024学年高二化学教材实验大盘点(人教版2019选择性必修1)2023年高考海南卷化学真题(已下线)不定项选择题(已下线)第31讲盐类的水解(已下线)考点3 盐类水解(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)课时1盐类的水解课堂例题
22-23高二上·全国·课时练习
解题方法
2 . A、B、C、D、E五种溶液分别是NaOH、NH3·H2O、CH3COOH、HCl、NH4HSO4中的一种。常温下进行下列实验:
①B、D均能与pH=3的A溶液反应,当它们以等物质的量混合时均能恰好反应,反应后得到的溶液前者呈酸性,后者呈中性;
②浓度均为0.1mol·L-1C与D溶液等体积混合,溶液呈酸性。
回答下列问题:
(1)D是________ ,E是________ ;
(2)用水稀释0.1 mol·L-1B溶液时,溶液中随着水量的增加而减小的是________ (填写序号)。
a. b.
b. c.c(H+)·c(OH-) d.n(OH-)
c.c(H+)·c(OH-) d.n(OH-)
(3)pH相同的等体积的两份溶液A和E,分别与镁粉反应,若最后仅有一份溶液中存在镁粉,且放出氢气的质量相同,则下列说法正确的是________ (填写序号)。
a.反应所需要的时间E>A
b.开始反应时的速率A>E
c.参加反应的镁粉物质的量A=E
d.E溶液里有镁粉剩余
(4)将等体积、等物质的量浓度B和C混合后溶液,升高温度(溶质不会分解)溶液pH随温度变化如图中___ 曲线(填写序号)。
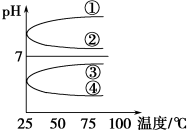
(5)室温下,向0.01mol·L-1 C溶液中滴加0.01mol·L-1 D溶液至中性,得到的溶液中所有离子的物质的量浓度由大到小的顺序为____________________ 。
①B、D均能与pH=3的A溶液反应,当它们以等物质的量混合时均能恰好反应,反应后得到的溶液前者呈酸性,后者呈中性;
②浓度均为0.1mol·L-1C与D溶液等体积混合,溶液呈酸性。
回答下列问题:
(1)D是
(2)用水稀释0.1 mol·L-1B溶液时,溶液中随着水量的增加而减小的是
a.
 b.
b. c.c(H+)·c(OH-) d.n(OH-)
c.c(H+)·c(OH-) d.n(OH-)(3)pH相同的等体积的两份溶液A和E,分别与镁粉反应,若最后仅有一份溶液中存在镁粉,且放出氢气的质量相同,则下列说法正确的是
a.反应所需要的时间E>A
b.开始反应时的速率A>E
c.参加反应的镁粉物质的量A=E
d.E溶液里有镁粉剩余
(4)将等体积、等物质的量浓度B和C混合后溶液,升高温度(溶质不会分解)溶液pH随温度变化如图中

(5)室温下,向0.01mol·L-1 C溶液中滴加0.01mol·L-1 D溶液至中性,得到的溶液中所有离子的物质的量浓度由大到小的顺序为
您最近一年使用:0次
解题方法
3 . 平衡常数是分析平衡问题的重要依据。回答下列问题:
(1)已知: 时,
时, 的
的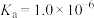 ,则
,则 时,
时, 的
的 溶液的
溶液的
_______ 。
(2)在温度为 时,某研究人员测定
时,某研究人员测定 的电离常数
的电离常数 为
为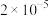 ,
, 的水解常数
的水解常数 为
为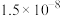 ,则该温度下水的离子积常数
,则该温度下水的离子积常数 为
为_______ ,请判断
_______ (填“>”“<”或“=”) 。
。
(3)化工生产中常用 作沉淀剂除去工业废水中的
作沉淀剂除去工业废水中的 :
: 。该反应的平衡常数
。该反应的平衡常数 为
为_______ ( 和
和 的
的 分别为
分别为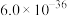 、
、 )。
)。
(4) 时,将
时,将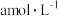 的氨水与
的氨水与 的盐酸等体积混合,所得溶液中
的盐酸等体积混合,所得溶液中 ,则溶液显
,则溶液显_______ (填“酸”“碱”或“中”)性;用含a的代数式表示 的电离常数
的电离常数
_______ 。
(1)已知:
 时,
时, 的
的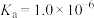 ,则
,则 时,
时, 的
的 溶液的
溶液的
(2)在温度为
 时,某研究人员测定
时,某研究人员测定 的电离常数
的电离常数 为
为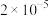 ,
, 的水解常数
的水解常数 为
为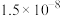 ,则该温度下水的离子积常数
,则该温度下水的离子积常数 为
为
 。
。(3)化工生产中常用
 作沉淀剂除去工业废水中的
作沉淀剂除去工业废水中的 :
: 。该反应的平衡常数
。该反应的平衡常数 为
为 和
和 的
的 分别为
分别为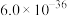 、
、 )。
)。(4)
 时,将
时,将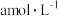 的氨水与
的氨水与 的盐酸等体积混合,所得溶液中
的盐酸等体积混合,所得溶液中 ,则溶液显
,则溶液显 的电离常数
的电离常数
您最近一年使用:0次
4 . 2021年我国制氢量位居世界第一,煤的气化是一种重要的制氢途径。回答下列问题:
(1)在一定温度下,向体积固定的密闭容器中加入足量的 和
和 ,起始压强为
,起始压强为 时,发生下列反应生成水煤气:
时,发生下列反应生成水煤气:
Ⅰ.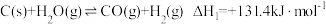
Ⅱ.
①下列说法正确的是_______ ;
A.平衡时向容器中充入惰性气体,反应Ⅰ的平衡逆向移动
B.混合气体的密度保持不变时,说明反应体系已达到平衡
C.平衡时 的体积分数可能大于
的体积分数可能大于
D.将炭块粉碎,可加快反应速率
②反应平衡时, 的转化率为
的转化率为 ,CO的物质的量为
,CO的物质的量为 。此时,整个体系
。此时,整个体系_______ (填“吸收”或“放出”)热量_______ kJ,反应Ⅰ的平衡常数
_______ (以分压表示,分压=总压×物质的量分数)。
(2)一种脱除和利用水煤气中 方法的示意图如下:
方法的示意图如下:
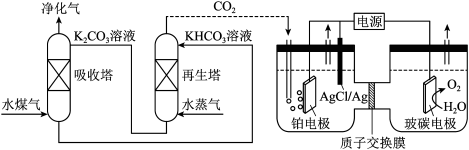
①某温度下,吸收塔中 溶液吸收一定量的
溶液吸收一定量的 后,
后, ,则该溶液的
,则该溶液的
_______ (该温度下 的
的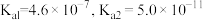 );
);
②再生塔中产生 的离子方程式为
的离子方程式为_______ ;
③利用电化学原理,将 电催化还原为
电催化还原为 ,阴极反应式为
,阴极反应式为_______ 。
(1)在一定温度下,向体积固定的密闭容器中加入足量的
 和
和 ,起始压强为
,起始压强为 时,发生下列反应生成水煤气:
时,发生下列反应生成水煤气:Ⅰ.
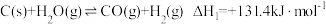
Ⅱ.

①下列说法正确的是
A.平衡时向容器中充入惰性气体,反应Ⅰ的平衡逆向移动
B.混合气体的密度保持不变时,说明反应体系已达到平衡
C.平衡时
 的体积分数可能大于
的体积分数可能大于
D.将炭块粉碎,可加快反应速率
②反应平衡时,
 的转化率为
的转化率为 ,CO的物质的量为
,CO的物质的量为 。此时,整个体系
。此时,整个体系
(2)一种脱除和利用水煤气中
 方法的示意图如下:
方法的示意图如下:
①某温度下,吸收塔中
 溶液吸收一定量的
溶液吸收一定量的 后,
后, ,则该溶液的
,则该溶液的
 的
的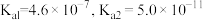 );
);②再生塔中产生
 的离子方程式为
的离子方程式为③利用电化学原理,将
 电催化还原为
电催化还原为 ,阴极反应式为
,阴极反应式为
您最近一年使用:0次
2022-06-10更新
|
11233次组卷
|
20卷引用:模块综合检测卷2
模块综合检测卷22022年新高考湖南化学高考真题(已下线)2022年湖南卷高考真题变式题(15-19)(已下线)专题14 化学反应原理综合题-2022年高考真题模拟题分项汇编(已下线)专题15 化学反应原理综合题-三年(2020-2022)高考真题分项汇编(已下线)考点22 化学平衡状态与化学平衡移动-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)专题18 化学反应原理综合题-备战2023年高考化学母题题源解密(广东卷)广东省汕头市金山中学2022-2023学年高三上学期第二次月考化学试题山东省枣庄市第三中学2022-2023学年高三上学期期中考试化学试题广东省佛山市顺德区第一中学2023届高三上学期12月综合训练化学试题安徽省六安第一中学2022-2023学年高二上学期期末考试化学试题山东省潍坊市昌乐第一中学2022-2023学年高二上学期期末拉练二化学试题(已下线)回归教材重难点08 聚焦热、速率、平衡-【查漏补缺】2023年高考化学三轮冲刺过关(新高考专用)(已下线)专题17 原理综合题(已下线)专题17 原理综合题(已下线)第20练 化学反应原理综合题 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)(已下线)专题14 化学反应原理综合题-2023年高考化学真题题源解密(新高考专用)(已下线)专题15 化学反应原理综合题-2023年高考化学真题题源解密(全国通用)四川省眉山市彭山区第一中学2023-2024学年高三上学期11月月考理综试题 河南省南阳市第一中学校2024届高三上学期阶段检测化学试题(12月)
21-22高二上·江西·期末
5 . H2A为二元酸,其电离过程为:H2A H++HA-,HA-
H++HA-,HA- H++A2-。常温时,向20mL 0.1mol/L H2A水溶液中逐滴滴加0.1mol/L NaOH溶液,混合溶液中H2A、HA-和A2-的物质的量分数(δ)随pH变化的关系如图所示。下列说法正确的是
H++A2-。常温时,向20mL 0.1mol/L H2A水溶液中逐滴滴加0.1mol/L NaOH溶液,混合溶液中H2A、HA-和A2-的物质的量分数(δ)随pH变化的关系如图所示。下列说法正确的是
 H++HA-,HA-
H++HA-,HA- H++A2-。常温时,向20mL 0.1mol/L H2A水溶液中逐滴滴加0.1mol/L NaOH溶液,混合溶液中H2A、HA-和A2-的物质的量分数(δ)随pH变化的关系如图所示。下列说法正确的是
H++A2-。常温时,向20mL 0.1mol/L H2A水溶液中逐滴滴加0.1mol/L NaOH溶液,混合溶液中H2A、HA-和A2-的物质的量分数(δ)随pH变化的关系如图所示。下列说法正确的是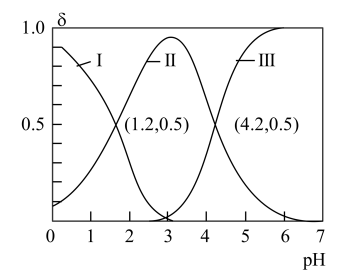
| A.H2A的Kal的数量级为10-1 |
| B.当溶液中c(H2A)=c(A2-)时,pH=2.7 |
| C.曲线Ⅱ表示A2- |
| D.向pH=4.2的溶液中继续滴加NaOH溶液,水的电离程度持续变大 |
您最近一年使用:0次
2022-02-16更新
|
2206次组卷
|
8卷引用:3.1.2 电离平衡常数-2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)
(已下线)3.1.2 电离平衡常数-2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)江西省六校2021-2022学年高二上学期期末联考化学试题(已下线)微专题39 水溶液中平衡图像的拓展与探析-备战2023年高考化学一轮复习考点微专题吉林省长春市十一高中2022-2023学年高二上学期第一学程考试化学试题贵州省凯里市第一中学2022-2023学年高二上学期期末考试化学试题广东省揭阳市惠来县第一中学2022-2023学年高二上学期12月月考化学试题广东省深圳市盐田高级中学2023-2024高二上学期期中考试化学试题甘肃省白银市靖远县第四中学2023-2024学年高二下学期开学化学试题
名校
6 .  时,
时, 的电离常数:
的电离常数: ,
,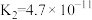 ,下列说法中正确的是
,下列说法中正确的是
 时,
时, 的电离常数:
的电离常数: ,
,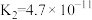 ,下列说法中正确的是
,下列说法中正确的是A.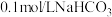 溶液中: 溶液中: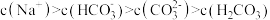 |
B.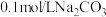 溶液中: 溶液中: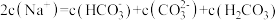 |
C. 和 和 混合液中: 混合液中: |
D.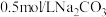 溶液与 溶液与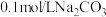 溶液中 溶液中 之比小于5 之比小于5 |
您最近一年使用:0次
2022-01-18更新
|
1025次组卷
|
3卷引用:作业(十九) 溶液中粒子浓度的大小比较
名校
解题方法
7 . 常温下0.2mol/L的一元酸HA溶液与等浓度的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是
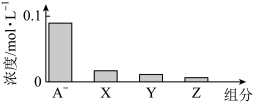
| A.HA为强酸 |
| B.该混合溶液中:c(A-)+c(Y)=c(Na+) |
| C.该混合液pH=7 |
| D.图中X表示HA,Y表示OH-,Z表示H+ |
您最近一年使用:0次
2021-12-01更新
|
517次组卷
|
17卷引用:鲁科版(2019)选择性必修1 第3章 物质在水溶液中的行为 第2节 弱电解质的电离盐类的水解
鲁科版(2019)选择性必修1 第3章 物质在水溶液中的行为 第2节 弱电解质的电离盐类的水解鲁科版(2019)高二选择性必修第一册第3章 物质在水溶液中的行为 第2节 弱电解质的电离 盐类的水解 课时4 溶液中粒子浓度的大小关系3.3.3盐类水解的应用 课后2015届上海市闸北区高三下学期期中练习(二模)化学试卷上海市闸北区2015年高考二模化学试题江西省南昌市第十中学2020-2021学年高二上学期期中考试化学试题江西省南昌市第二中学2020-2021学年高二上学期第三次月考化学试题江西省抚州市黎川县第一中学2020-2021学年高二上学期第三次月考化学试题江西省景德镇一中2020-2021学年高一下学期期末考试化学(2班)试题广东省深圳市西乡中学2021-2022学年高二上学期期中考试化学试题江西省吉安市遂川中学2021-2022学年高二上学期第三次月考(B)化学试题河南省重点高中2021-2022学年高二下学期阶段性调研联考一化学试题(已下线)二轮拔高卷3-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(上海卷)(已下线)第21讲 电离平衡(练)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)2019年高考浙江卷化学试题变式题(单选题21-25)北京市清华大学附属中学2023-2024学年高二上学期第三单元化学统练广东省 江门市棠下中学2023-2024学年高二上学期期中考试化学试题
20-21高二上·河北石家庄·阶段练习
名校
8 . 下列图示与对应的叙述相符的是
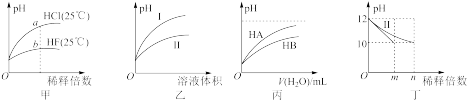

| A.由图甲可知,a点Kw的数值比b点Kw的数值大 |
| B.图乙表示用水稀释pH相同的盐酸和醋酸,I表示醋酸,II表示盐酸 |
| C.图丙表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则相同浓度时NaA溶液的pH小于同浓度的NaB溶液的pH |
| D.图丁表示分别稀释10mLpH均为12的NaOH溶液和氨水时pH的变化,曲线I表示氨水,n>100 |
您最近一年使用:0次
2021-09-16更新
|
558次组卷
|
8卷引用:3.3.1 盐类水解的原理-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)
(已下线)3.3.1 盐类水解的原理-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)河北正定中学2020-2021学年高二上学期第一次半月考化学试题(已下线)必考点07 盐类的水解-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版选择性必修1)黑龙江省双鸭山市第一中学2021-2022学年高二上学期期中考试化学试题山东省淄博市高青县第一中学2021-2022学年高二上学期期中考试化学试题江西省吉安市遂川中学2021-2022学年高二上学期第三次月考(B)化学试题黑龙江省大兴安岭呼玛县高级中学2021-2022学年高二上学期期末考试化学试题安徽省合肥市肥东县综合高中2021-2022学年高二下学期5月月考化学试题
2021·四川巴中·模拟预测
名校
9 . 某浓度的二元弱酸H2B溶液在不同pH下,测得Pc(M)变化如图所示,(已知: Pc(M)=-1gc(M),M代指H2B或HB-或B2-),下列说法正确的是


| A.曲线II表示Pc(HB-)与pH关系 |
| B.pH=5时,c(HB- )<c(B2- )<c(H2B) |
C.由图像数据可以计算出 的值 的值 |
| D.在pH增大的过程中,c(H2B)、c(HB-)、 c(B2-)三者浓度和先减小后增大 |
您最近一年使用:0次
2021-09-13更新
|
2451次组卷
|
9卷引用:章末培优3 专题3 水溶液中的离子反应-2021-2022学年高二化学课后培优练(苏教教版2019选择性必修1)
(已下线)章末培优3 专题3 水溶液中的离子反应-2021-2022学年高二化学课后培优练(苏教教版2019选择性必修1)四川省巴中市2022届高三零诊理科综合化学试题河北饶阳中学2021-2022学年高二上学期第一阶段考试化学试题(已下线)2021年高考全国乙卷化学试题变式题(已下线)备战2022年高考化学精准检测卷【全国卷】03江西省吉安市安福二中、吉安县三中、井大附中三校2021-2022学年高二上学期12月联考化学试题(已下线)第八章 水溶液中的离子反应与平衡 第51讲 反应过程溶液粒子浓度变化的图像分析辽宁省大连市第八中学2021-2022学年高二上学期10月月考化学试题(已下线)微专题 水溶液中函数图像的分析
10 . 常温下,用 的盐酸分别滴定20.00mL浓度均为
的盐酸分别滴定20.00mL浓度均为 三种一元弱酸的钠盐
三种一元弱酸的钠盐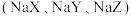 溶液,滴定曲线如图所示。下列判断错误的是
溶液,滴定曲线如图所示。下列判断错误的是
 的盐酸分别滴定20.00mL浓度均为
的盐酸分别滴定20.00mL浓度均为 三种一元弱酸的钠盐
三种一元弱酸的钠盐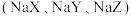 溶液,滴定曲线如图所示。下列判断错误的是
溶液,滴定曲线如图所示。下列判断错误的是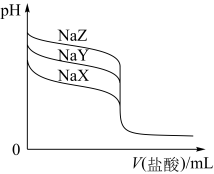
A.该 溶液中: 溶液中: |
B.三种一元弱酸的电离常数: |
C.当 时,三种溶液中: 时,三种溶液中: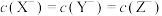 |
D.分别滴加20.00mL盐酸后,再将三种溶液混合: |
您最近一年使用:0次
2021-06-09更新
|
15398次组卷
|
58卷引用:第三章 综合拔高练
第三章 综合拔高练2021年新高考湖南化学高考真题(已下线)作业09 盐类的水解-2021年高二化学暑假作业(人教版2019)(已下线)考点25 盐类的水解-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点25 盐类的水解-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)课时44 滴定曲线、分布系数曲线的分析-2022年高考化学一轮复习小题多维练(全国通用)(已下线)第22讲 水的电离与溶液的pH(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)考向25 水的电离和溶液的酸碱性-备战2022年高考化学一轮复习考点微专题(已下线)第4讲 溶液中离子的浓度大小比较-【微专题·大素养】备战2022年高考化学核心突破(水溶液中的离子反应与平衡)辽宁省东北育才学校2021-2022学年高二上学期期中考试化学试题(已下线)专题12 水溶液中的离子平衡-备战2022年高考化学学霸纠错(全国通用)2021年湖南省高考化学试卷变式题1-10(已下线)第09练 盐类的水解 -2022年【寒假分层作业】高二化学(人教版2019选择性必修1)山西省怀仁市2021-2022学年高二上学期期末调研化学试题(已下线)解密10 水溶液中的离子平衡(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密10 水溶液中的离子平衡(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)专题13 水溶液中的离子平衡-2022年高考化学二轮复习重点专题常考点突破练(已下线)专题07 电解质溶液—2022年高考化学二轮复习讲练测(全国版)-练习福建省福州第一中学2021-2022学年高二上学期期末考试化学试题(已下线)卷09 水溶液中的离子平衡-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)(已下线)押新高考卷13题 水溶液中的离子平衡-备战2022年高考化学临考题号押题(新高考通版)(已下线)回归教材重难点04 水溶液中的离子平衡-【查漏补缺】2022年高考化学三轮冲刺过关(新高考专用)北京市海淀区中关村中学2022届高三下学期三模化学试题(已下线)专题10 水溶液中的离子平衡-三年(2020-2022)高考真题分项汇编广东省揭阳市普宁市华侨中学2021-2022学年高二下学期第三次月考化学试题(已下线)考点28 盐类的水解-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第31练 水的电离和溶液的pH-2023年高考化学一轮复习小题多维练(全国通用)(已下线)第22讲 水的电离与溶液的pH(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)微专题41 水溶液中的三大守恒和浓度大小比较-备战2023年高考化学一轮复习考点微专题(已下线)微专题42 四大平衡常数的计算与应用-备战2023年高考化学一轮复习考点微专题(已下线)易错点25 盐类水解-备战2023年高考化学考试易错题(已下线)专题06 水溶液中的离子平衡(讲)-2023年高考化学二轮复习讲练测(新高考专用)湖南省临湘市第五中学2021-2022学年高二上学期第三次月考化学试题天津市和平区2022-2023学年高二上学期期末质量调查化学试卷天津市和平区2022-2023学年高二上学期期末质量检测化学试题 吉林省长春市第五中学2022-2023学年高二上学期期末考试化学试题湖南省株洲九方中学2022-2023学年高二上学期期中考试化学试题(已下线)专题21 电解质溶液图像分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)第八章 水溶液中的离子反应与平衡 第51讲 反应过程溶液粒子浓度变化的图像分析(已下线)题型135 酸溶液与碱溶液互滴图像分析(已下线)专题11 水溶液中的离子平衡图像(选择题)-2023年高考化学毕业班二轮热点题型归纳与变式演练(已下线)专题四 电解质溶液图象(讲)(已下线)题型26 电离平衡常数、水解平衡常数及其应用图像(已下线)专题16 水溶液中的离子平衡(已下线)专题16 水溶液中的离子平衡广东省四校(华附,省实,广雅,深中)2022-2023学年高二下学期期末联考化学试题(已下线)专题09 水溶液中的离子平衡-2023年高考化学真题题源解密(新高考专用)(已下线)考点28 盐类的水解(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)专题12 水溶液中的离子反应与平衡-2023年高考化学真题题源解密(全国通用)辽宁省大连市第八中学2021-2022学年高二上学期12月月考化学试题(已下线)微专题 水溶液中函数图像的分析(已下线)考点3 盐类水解(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)广东省深圳市盐田高级中学2023-2024高二上学期期中考试化学试题北京市清华大学附属中学2023-2024学年高二上学期第三单元化学统练福建省福清市虞阳中学2022-2023学年高二上学期期末考试化学试题北京市 首都师范大学附属中学2021-2022学年高二上学期期末考试化学试卷湖南省邵东市第三中学2023-2024学年高二上学期1月期末考试化学试卷 天津市南开中学2024届高三下学期第五次月检测化学试卷



