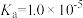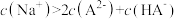H2A为二元酸,其电离过程为:H2A H++HA-,HA-
H++HA-,HA- H++A2-。常温时,向20mL 0.1mol/L H2A水溶液中逐滴滴加0.1mol/L NaOH溶液,混合溶液中H2A、HA-和A2-的物质的量分数(δ)随pH变化的关系如图所示。下列说法正确的是
H++A2-。常温时,向20mL 0.1mol/L H2A水溶液中逐滴滴加0.1mol/L NaOH溶液,混合溶液中H2A、HA-和A2-的物质的量分数(δ)随pH变化的关系如图所示。下列说法正确的是
 H++HA-,HA-
H++HA-,HA- H++A2-。常温时,向20mL 0.1mol/L H2A水溶液中逐滴滴加0.1mol/L NaOH溶液,混合溶液中H2A、HA-和A2-的物质的量分数(δ)随pH变化的关系如图所示。下列说法正确的是
H++A2-。常温时,向20mL 0.1mol/L H2A水溶液中逐滴滴加0.1mol/L NaOH溶液,混合溶液中H2A、HA-和A2-的物质的量分数(δ)随pH变化的关系如图所示。下列说法正确的是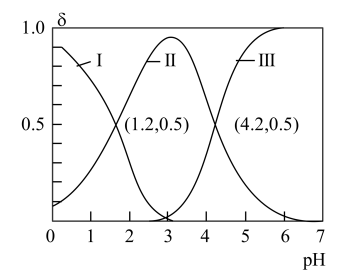
| A.H2A的Kal的数量级为10-1 |
| B.当溶液中c(H2A)=c(A2-)时,pH=2.7 |
| C.曲线Ⅱ表示A2- |
| D.向pH=4.2的溶液中继续滴加NaOH溶液,水的电离程度持续变大 |
21-22高二上·江西·期末 查看更多[8]
江西省六校2021-2022学年高二上学期期末联考化学试题(已下线)3.1.2 电离平衡常数-2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)(已下线)微专题39 水溶液中平衡图像的拓展与探析-备战2023年高考化学一轮复习考点微专题吉林省长春市十一高中2022-2023学年高二上学期第一学程考试化学试题贵州省凯里市第一中学2022-2023学年高二上学期期末考试化学试题广东省揭阳市惠来县第一中学2022-2023学年高二上学期12月月考化学试题广东省深圳市盐田高级中学2023-2024高二上学期期中考试化学试题甘肃省白银市靖远县第四中学2023-2024学年高二下学期开学化学试题
更新时间:2022-02-16 23:15:18
|
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】室温下,下列有关叙述正确的是
①分别向等体积、等物质的量浓度的盐酸和醋酸中滴加NaOH溶液,使溶液呈中性,醋酸消耗的NaOH多;
②等体积、等pH的盐酸和醋酸,分别与NaOH反应,使溶液成恰好中和,醋酸消耗的NaOH多;
③相同条件下,将pH=2的硫酸溶液和pH=2的醋酸溶液分别稀释成pH=5的溶液,所加水的体积前者大;
④pH=3的稀硫酸跟pH=11的氢氧化钠溶液等体积混合,混合溶液的pH<7;
⑤相同条件下,将同体积pH=2的硫酸溶液和pH=2的醋酸溶液分别与锌粒反应后者生成氢气体积比前者大;
⑥同体积同浓度的盐酸和醋酸与足量锌反应,整个反应过程的平均反应速率盐酸的快。
①分别向等体积、等物质的量浓度的盐酸和醋酸中滴加NaOH溶液,使溶液呈中性,醋酸消耗的NaOH多;
②等体积、等pH的盐酸和醋酸,分别与NaOH反应,使溶液成恰好中和,醋酸消耗的NaOH多;
③相同条件下,将pH=2的硫酸溶液和pH=2的醋酸溶液分别稀释成pH=5的溶液,所加水的体积前者大;
④pH=3的稀硫酸跟pH=11的氢氧化钠溶液等体积混合,混合溶液的pH<7;
⑤相同条件下,将同体积pH=2的硫酸溶液和pH=2的醋酸溶液分别与锌粒反应后者生成氢气体积比前者大;
⑥同体积同浓度的盐酸和醋酸与足量锌反应,整个反应过程的平均反应速率盐酸的快。
| A.①②⑤ | B.③④⑤ | C.②④⑤ | D.②⑤⑥ |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】室温下,通过下列实验探究 溶液的性质。下列有关说法正确的是
溶液的性质。下列有关说法正确的是
 溶液的性质。下列有关说法正确的是
溶液的性质。下列有关说法正确的是| 实验 | 实验操作和现象或结论 |
| 1 | 用 试纸测量 试纸测量 溶液的 溶液的 ,测得 ,测得 约为5 约为5 |
| 2 | 向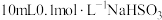 溶液中加入等体积 溶液中加入等体积 氨水溶液,充分混合,溶液 氨水溶液,充分混合,溶液 约为9 约为9 |
| 3 | 向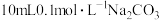 溶液中滴加几滴 溶液中滴加几滴 溶液,无明显现象 溶液,无明显现象 |
| 4 | 向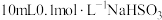 溶液中加入 溶液中加入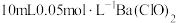 溶液,产生白色沉淀 溶液,产生白色沉淀 |
A.实验1可得出: |
B.实验2所得溶液中存在: |
C.实验3可得出: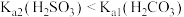 |
D.实验4两溶液混合时有: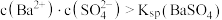 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】已知HA是一元弱酸,MA是难溶盐,且 不发生水解。常温下,向某
不发生水解。常温下,向某 的溶液中逐滴加入MOH溶液后,溶液中
的溶液中逐滴加入MOH溶液后,溶液中 和
和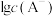 随
随 的变化关系如下图所示。下列说法错误的是
的变化关系如下图所示。下列说法错误的是
 不发生水解。常温下,向某
不发生水解。常温下,向某 的溶液中逐滴加入MOH溶液后,溶液中
的溶液中逐滴加入MOH溶液后,溶液中 和
和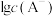 随
随 的变化关系如下图所示。下列说法错误的是
的变化关系如下图所示。下列说法错误的是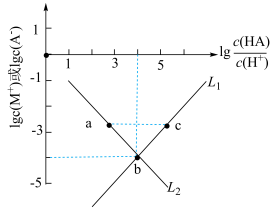
A.曲线 表示 表示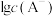 随 随 的变化 的变化 |
B.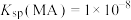 |
| C.pH:a>c |
D.b点时溶液中存在: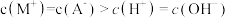 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】常温下,某酸H2A溶液中含A物种的浓度之和为amol·L-1,溶液中各含A物种的pc—pOH关系如图所示。图中pc表示各含A物种的浓度负对数(pc=-lgc),pOH表示OH-的浓度负对数[pOH=-lgc(OH-)];x、y、z三点的坐标:x(7.3,1.3),y(10.0,3.6),z(12.6,1.3)。下列说法不正确的是


| A.曲线③表示pc(H2A)随pOH的变化 |
| B.pH=2的溶液中:c(H2A)>c(HA-)>c(A2-) |
| C.pH=4的溶液中:c(HA-)=amol/L-2c(A2-) |
| D.H2A+A2-⇌2HA-的平衡常数K>1.0×105 |
您最近一年使用:0次


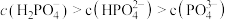
 将先增大后减小
将先增大后减小 生成
生成 沉淀除磷后,溶液
沉淀除磷后,溶液 的平衡常数
的平衡常数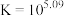
 的NaOH溶液滴定20.00mL的二元酸
的NaOH溶液滴定20.00mL的二元酸 溶液。溶液中,pH、分布系数
溶液。溶液中,pH、分布系数 随滴加NaOH溶液体积
随滴加NaOH溶液体积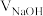 的变化关系如下图所示。
的变化关系如下图所示。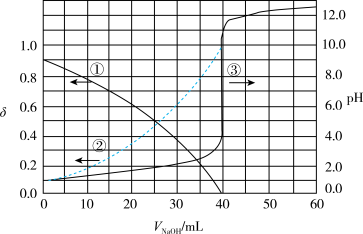
 的分布系数:
的分布系数: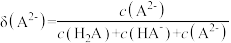 ]
] ,
,
 的电离常数
的电离常数