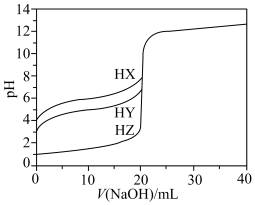
1 . 25 ℃时,用浓度为0.100 0 mol·L-1的NaOH溶液滴定20.00 mL浓度均为0.100 0 mol·L-1的三种酸HX、HY、HZ的溶液,滴定曲线如图所示。
(1)在相同温度下,相同浓度的三种酸溶液的导电能力由强到弱的顺序是____________ 。
(2)V(NaOH)=20.00 mL时,溶液中c(HY)__________ (填“<”“>”或“=”,下同)c(Y-)。若使最终溶液的pH=7,则滴定HZ溶液和滴定HX溶液所需NaOH溶液的体积的关系是HX溶液________ HZ溶液。
(3)将上述HX溶液、HY溶液等体积混合后,用NaOH溶液滴定至HX恰好完全反应时,溶液中各离子浓度的大小关系为_____________ 。
(4)根据滴定曲线,可得Ka(HY)≈________ 。

(1)在相同温度下,相同浓度的三种酸溶液的导电能力由强到弱的顺序是
(2)V(NaOH)=20.00 mL时,溶液中c(HY)
(3)将上述HX溶液、HY溶液等体积混合后,用NaOH溶液滴定至HX恰好完全反应时,溶液中各离子浓度的大小关系为
(4)根据滴定曲线,可得Ka(HY)≈
您最近一年使用:0次
2 . 25 ℃时部分弱酸的电离平衡常数如下表:
(1)在温度相同时,各弱酸的Ka值与酸性的相对强弱的关系为________________ 。
(2)室温下①0.1 mol·L-1 HCOONa,②0.1 mol·L-1 NaClO,③0.1 mol·L-1 Na2CO3,④0.1 mol·L-1 NaHCO3,溶液的pH由大到小的关系为________________ 。
(3)浓度均为0.1 mol·L-1的Na2SO3和Na2CO3的混合溶液中,SO 、CO
、CO 、HSO
、HSO 、HCO
、HCO 浓度由大到小的顺序为
浓度由大到小的顺序为____________________ 。
(4)下列离子方程式书写正确的是__________ (填字母)。
a.2ClO-+H2O+CO2=2HClO+CO
b.2HCOOH+CO =2HCOO-+H2O+CO2↑
=2HCOO-+H2O+CO2↑
c.H2SO3+2HCOO-=2HCOOH+SO
d.Cl2+H2O+2CO =2HCO
=2HCO +Cl-+ClO-
+Cl-+ClO-
(5)常温下,pH=3的HCOOH溶液与pH=11的NaOH溶液等体积混合后,溶液中离子浓度由大到小的顺序为________________________ 。
弱酸 | HCOOH | HClO | H2CO3 | H2SO3 |
电离平衡 常数/(mol·L-1) | Ka=1.8×10-4 | Ka=4.7×10-8 | Ka1=4.2×10-7 Ka2=5.6×10-11 | Ka1=1.54×10-2 Ka2=1.02×10-7 |
(2)室温下①0.1 mol·L-1 HCOONa,②0.1 mol·L-1 NaClO,③0.1 mol·L-1 Na2CO3,④0.1 mol·L-1 NaHCO3,溶液的pH由大到小的关系为
(3)浓度均为0.1 mol·L-1的Na2SO3和Na2CO3的混合溶液中,SO
 、CO
、CO 、HSO
、HSO 、HCO
、HCO 浓度由大到小的顺序为
浓度由大到小的顺序为(4)下列离子方程式书写正确的是
a.2ClO-+H2O+CO2=2HClO+CO

b.2HCOOH+CO
 =2HCOO-+H2O+CO2↑
=2HCOO-+H2O+CO2↑c.H2SO3+2HCOO-=2HCOOH+SO

d.Cl2+H2O+2CO
 =2HCO
=2HCO +Cl-+ClO-
+Cl-+ClO-(5)常温下,pH=3的HCOOH溶液与pH=11的NaOH溶液等体积混合后,溶液中离子浓度由大到小的顺序为
您最近一年使用:0次
3 . 已知在25 ℃时,氨水中NH3·H2O的电离常数Kb=1.8×10-5 mol·L-1,回答下列问题:
(1)氨水中NH3·H2O的电离常数表达式Kb=___________ 。
(2)当向该氨水中加入一定量的NaOH溶液时,Kb值是否会发生变化?___________ (填“会”或“不会”)。
(3)若该氨水的起始浓度为0.01 mol·L-1,则达到电离平衡时溶液中OH-的物质的量浓度为___________ 。
(1)氨水中NH3·H2O的电离常数表达式Kb=
(2)当向该氨水中加入一定量的NaOH溶液时,Kb值是否会发生变化?
(3)若该氨水的起始浓度为0.01 mol·L-1,则达到电离平衡时溶液中OH-的物质的量浓度为
您最近一年使用:0次
解题方法
4 . 含物质的量相同的CH3COOH和CH3COONa混合溶液中:
(1)写出所有电离、水解离子方程式:_______ 。
(2)粒子浓度由大到小顺序为_______ 。
(3)电荷守恒:_______ 。
(4)物料守恒:_______ 。
(1)写出所有电离、水解离子方程式:
(2)粒子浓度由大到小顺序为
(3)电荷守恒:
(4)物料守恒:
您最近一年使用:0次
解题方法
5 . 常温下,0.1mol/L的下列五种溶液:
①CH3COOH②NaClO③NH4Cl④NaCl⑤CH3COONa,其pH由大到小的排列顺序是_______ 。
①CH3COOH②NaClO③NH4Cl④NaCl⑤CH3COONa,其pH由大到小的排列顺序是
您最近一年使用:0次
6 . 已知Ka(CH3COOH)=1.75×10-5,试计算0.1 mol·L-1 CH3COOH溶液中H+的浓度(写出计算过程) ______ 。
您最近一年使用:0次
解题方法
7 . 现有如下各化合物:①酒精,②氯化铵,③氢氧化钡,④氨水,⑤蔗糖,⑥高氯酸,⑦氢硫酸,⑧硫酸氢钾,⑨磷酸,⑩硫酸。请用物质的序号填写下列空白。
(1)属于电解质的有:___________ 。
(2)属于强电解质的有:___________ 。
(3)属于弱电解质的有:___________ 。
(1)属于电解质的有:
(2)属于强电解质的有:
(3)属于弱电解质的有:
您最近一年使用:0次
8 . 写出下列电解质在水溶液中的电离方程式。
(1)HClO4:___________ 。
(2)HClO:___________ 。
(3)NaHSO3:___________ 。
(1)HClO4:
(2)HClO:
(3)NaHSO3:
您最近一年使用:0次
9 . 有下列物质的溶液①CH3COOH ②HCl ③H2SO4 ④NaHSO4。
(1)若四种溶液的物质的量浓度相同,其c平(H+)的大小比较为___________ (用序号表示,下同)。
(2)若四种溶液的c平(H+)相同,其物质的量浓度的大小比较为___________ 。
(1)若四种溶液的物质的量浓度相同,其c平(H+)的大小比较为
(2)若四种溶液的c平(H+)相同,其物质的量浓度的大小比较为
您最近一年使用:0次
10 . 水体中的含氮化合物是引起富营养化的主要污染物,分析监测水体中的硝酸(盐)和亚硝酸(盐)含量,控制水体中的含氮污染物,对水资源的循环利用意义重大。
(1)亚硝酸(HNO2)是一种弱酸,其电离平衡常数的表达式为_________ 。
(2)水体中亚硝酸的含量可以利用KI溶液进行分析测定。该测定反应中,含氮的生成物可以是NO、N2O、NH2OH、NH3等。
①NH2OH中,氮元素的化合价为________ 。
②某水样中含有亚硝酸盐,加入少量稀硫酸酸化后,用KI溶液测定,且选用淀粉溶液作指示剂,反应中含N的生成物为NO,反应的离子方程式为________ ,其中氧化产物为________ (写化学式)。
(1)亚硝酸(HNO2)是一种弱酸,其电离平衡常数的表达式为
(2)水体中亚硝酸的含量可以利用KI溶液进行分析测定。该测定反应中,含氮的生成物可以是NO、N2O、NH2OH、NH3等。
①NH2OH中,氮元素的化合价为
②某水样中含有亚硝酸盐,加入少量稀硫酸酸化后,用KI溶液测定,且选用淀粉溶液作指示剂,反应中含N的生成物为NO,反应的离子方程式为
您最近一年使用:0次



