1 . 相同物质的量浓度的NaCN和NaClO相比,NaCN溶液的pH较大,则下列关于同温、同体积、同浓度的HCN和HClO的说法正确的是
| A.酸的强弱:HCN<HClO |
| B.pH:HClO>HCN |
| C.与NaOH恰好完全反应时,消耗NaOH的物质的量:HClO>HCN |
| D.酸根离子浓度:c平(CN-)<c平(ClO-) |
您最近一年使用:0次
2 . 已知K2HPO4溶液呈碱性,即HPO 结合H+的能力大于其电离产生H+的能力。溶液中存在如下平衡:①HPO
结合H+的能力大于其电离产生H+的能力。溶液中存在如下平衡:①HPO +H2O
+H2O H3O++PO
H3O++PO ,②HPO
,②HPO +H2O
+H2O OH-+H2PO
OH-+H2PO ,③H2O
,③H2O H++OH-。下列操作能使该溶液中c平(H3O+)增大的是
H++OH-。下列操作能使该溶液中c平(H3O+)增大的是
 结合H+的能力大于其电离产生H+的能力。溶液中存在如下平衡:①HPO
结合H+的能力大于其电离产生H+的能力。溶液中存在如下平衡:①HPO +H2O
+H2O H3O++PO
H3O++PO ,②HPO
,②HPO +H2O
+H2O OH-+H2PO
OH-+H2PO ,③H2O
,③H2O H++OH-。下列操作能使该溶液中c平(H3O+)增大的是
H++OH-。下列操作能使该溶液中c平(H3O+)增大的是| A.加水 | B.加热 |
| C.加消石灰 | D.加K2HPO4固体 |
您最近一年使用:0次
3 . 常温下,将等体积、等物质的量浓度的NH4HCO3与NaCl溶液混合,析出部分NaHCO3晶体,过滤,所得滤液pH<7。下列关于滤液中的离子浓度关系不正确的是
A.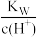 >1.0×10-7 mol·L-1 >1.0×10-7 mol·L-1 |
B.c(Na+)=c( )+c( )+c( )+c(H2CO3) )+c(H2CO3) |
C.c(H+)+c( )=c(OH-)+c( )=c(OH-)+c( )+2c( )+2c( ) ) |
D.c(Cl-)>c( )>c( )>c( )>c( )>c( ) ) |
您最近一年使用:0次
解题方法
4 . 下列说法正确的是
| A.强电解质一定是离子化合物,弱电解质一定是共价化合物 |
| B.强电解质一定是易溶于水的化合物,弱电解质一定是难溶于水的化合物 |
| C.CO2的水溶液导电能力很弱,所以CO2是弱电解质 |
| D.属于共价化合物的电解质在熔化状态下一般不导电 |
您最近一年使用:0次
2023-08-27更新
|
541次组卷
|
2卷引用:作业(十六) 水的电离电解质在水溶液中的存在形态
解题方法
5 . 强弱电解质的本质区别是
| A.导电能力 | B.相对分子质量 |
| C.电离程度 | D.溶解度 |
您最近一年使用:0次
2023-08-27更新
|
367次组卷
|
2卷引用:作业(十六) 水的电离电解质在水溶液中的存在形态
6 . 已知在t1、t2温度下水的电离平衡曲线如图所示,则下列说法不正确的是
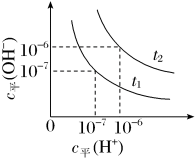

| A.t1<t2 |
| B.一定温度下,改变水溶液中c平(H+)或c平(OH-)的浓度,KW不会发生变化 |
| C.t2温度c平(H+)为1×10-2 mol·L-1的HCl溶液中,水电离出的c平(H+)=1×10-10 mol·L-1 |
| D.将t1温度下0.1 mol·L-1的盐酸稀释,溶液中所有离子的浓度均相应减小 |
您最近一年使用:0次
7 . 按如图Ⅰ所示的装置来测定烧杯中溶液的导电能力的强弱。
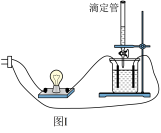
(1)若烧杯中盛放的是Ba(OH)2溶液,当从滴定管中逐渐加入相同物质的量浓度的某种溶液(A)时,溶液的导电性的变化趋势如图Ⅱ所示。
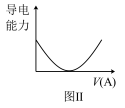
A溶液中含有的溶质可能是___________ (至少写出一种),并写出相应的离子反应的离子方程式: ___________ 。
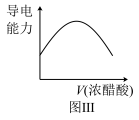
(2)若烧杯中盛放的是浓氨水,当从滴定管中逐渐加入相同浓度的浓醋酸时,溶液的导电性的变化趋势如图Ⅲ所示,则实验中观察的灯泡变化的现象是___________ ,原因是___________ 。
(3)由(1)和(2)两个实验对比可知,溶液导电性的强弱取决于___________ ,在相同温度和浓度的条件下,可溶性的强电解质的导电能力___________ (填“强”或“弱”)于弱电解质的导电能力。

(1)若烧杯中盛放的是Ba(OH)2溶液,当从滴定管中逐渐加入相同物质的量浓度的某种溶液(A)时,溶液的导电性的变化趋势如图Ⅱ所示。

A溶液中含有的溶质可能是
(2)若烧杯中盛放的是浓氨水,当从滴定管中逐渐加入相同浓度的浓醋酸时,溶液的导电性的变化趋势如图Ⅲ所示,则实验中观察的灯泡变化的现象是

(3)由(1)和(2)两个实验对比可知,溶液导电性的强弱取决于
您最近一年使用:0次
解题方法
8 . 若HA为一元弱酸,MOH为一元弱碱,已知:MA水解常数为Kh,HA的电离常数为Ka,MOH的电离常数Kb,水的离子积为KW试推导Kh、Ka、Kb、KW之间的关系___________ 。
您最近一年使用:0次
9 . 在一定温度下,有a.盐酸 b.硫酸 c.醋酸三种酸。
(1)当三种酸物质的量浓度相同时,c平(H+)由大到小的顺序是___________ (用字母表示,下同)。
(2)同体积、同物质的量浓度的三种酸,中和NaOH的能力由大到小的顺序是___________ 。
(3)若三者c平(H+)相同时,物质的量浓度由大到小的顺序是___________ 。
(4)将c平(H+)相同的三种酸均加水稀释至原来的100倍后,c平(H+)由大到小的顺序是___________ 。
(5)将c平(H+)相同且体积也相同的三种酸,分别与等浓度的NaOH稀溶液反应至pH=7,则消耗NaOH溶液的体积大小关系为___________ 。
(1)当三种酸物质的量浓度相同时,c平(H+)由大到小的顺序是
(2)同体积、同物质的量浓度的三种酸,中和NaOH的能力由大到小的顺序是
(3)若三者c平(H+)相同时,物质的量浓度由大到小的顺序是
(4)将c平(H+)相同的三种酸均加水稀释至原来的100倍后,c平(H+)由大到小的顺序是
(5)将c平(H+)相同且体积也相同的三种酸,分别与等浓度的NaOH稀溶液反应至pH=7,则消耗NaOH溶液的体积大小关系为
您最近一年使用:0次
10 . 完成下列问题。
(1)甲、乙两瓶氨水的浓度分别为1 mol·L-1和0.1 mol·L-1,则甲、乙两瓶氨水中c平(OH-)之比___________ (填“大于”“等于”或“小于”)10,请说明理由:____________________ 。
(2)常温下,将pH=10的NH3·H2O溶液稀释至原体积的10倍。
①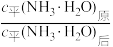
___________ 10(填“>”“<”或“=”,下同)。
②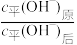
__________ 10。
③pH值范围是___________ 。
(1)甲、乙两瓶氨水的浓度分别为1 mol·L-1和0.1 mol·L-1,则甲、乙两瓶氨水中c平(OH-)之比
(2)常温下,将pH=10的NH3·H2O溶液稀释至原体积的10倍。
①
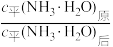
②
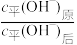
③pH值范围是
您最近一年使用:0次



