已知在t1、t2温度下水的电离平衡曲线如图所示,则下列说法不正确的是
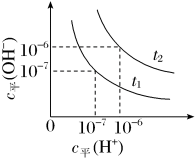

| A.t1<t2 |
| B.一定温度下,改变水溶液中c平(H+)或c平(OH-)的浓度,KW不会发生变化 |
| C.t2温度c平(H+)为1×10-2 mol·L-1的HCl溶液中,水电离出的c平(H+)=1×10-10 mol·L-1 |
| D.将t1温度下0.1 mol·L-1的盐酸稀释,溶液中所有离子的浓度均相应减小 |
更新时间:2023-08-27 10:43:03
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】常压下,研究 在盐酸中的溶解度(用溶解
在盐酸中的溶解度(用溶解 的物质的量浓度表示)。随盐酸浓度的变化,不同温度下
的物质的量浓度表示)。随盐酸浓度的变化,不同温度下 的溶解度见图1,溶液中含氯微粒的浓度变化见图2,下列说法正确的是
的溶解度见图1,溶液中含氯微粒的浓度变化见图2,下列说法正确的是
 在盐酸中的溶解度(用溶解
在盐酸中的溶解度(用溶解 的物质的量浓度表示)。随盐酸浓度的变化,不同温度下
的物质的量浓度表示)。随盐酸浓度的变化,不同温度下 的溶解度见图1,溶液中含氯微粒的浓度变化见图2,下列说法正确的是
的溶解度见图1,溶液中含氯微粒的浓度变化见图2,下列说法正确的是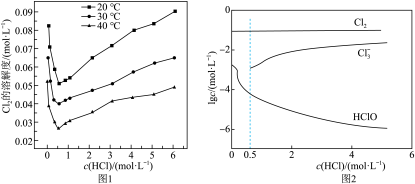
A.由图1可知,温度升高,在一定浓度的盐酸中 溶解度增大 溶解度增大 |
B.由图2可知,随盐酸浓度增大,与水反应的 逐渐增多 逐渐增多 |
C.盐酸浓度小于 时,主要发生的反应为 时,主要发生的反应为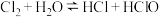 |
D.盐酸浓度大于 时,随盐酸浓度增大HClO浓度减小的主要原因是HClO分解 时,随盐酸浓度增大HClO浓度减小的主要原因是HClO分解 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】在一定温度下,将气体X和气体Y各0.16 mol充入10 L恒容密闭容器中,发生反应X(g)+ Y(g) 2Z(g) △H<0,一段时间后达到平衡。反应过程中测定的数据如下表:
2Z(g) △H<0,一段时间后达到平衡。反应过程中测定的数据如下表:
下列说法正确的是
 2Z(g) △H<0,一段时间后达到平衡。反应过程中测定的数据如下表:
2Z(g) △H<0,一段时间后达到平衡。反应过程中测定的数据如下表: | t / min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
| A.该温度下此反应的平衡常数K = 1.44 |
| B.其他条件不变,降低温度,反应达到新平衡前v(逆)>v(正) |
| C.反应前2 min的平均速率v(Z) = 2.0×10-3 mol/(L·min) |
| D.其他条件不变,再充入0.2 mol X,平衡时Y的体积分数增大 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】常温下,分别取未知浓度的MOH和HA溶液,加水稀释至原体积的n倍。稀释过程中,两溶液pH的变化如图所示。下列叙述正确的是
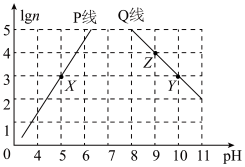
| A.P线代表HA的稀释图像且HA为强酸 |
| B.水的电离程度:Z>Y=X |
C.将X点溶液与Y点溶液混合至中性时, |
D.将X点溶液与Z点溶液等体积混合,所得溶液中一定有: |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】在25℃时,将1.0Lw mol·L-lCH3COOH溶液与0.1molNaOH固体混合,充分反应。然后向混合液中加入CH3COOH或CH3COONa固体(忽略体积和温度变化),引起溶液pH的变化如图所示。下列叙述正确的是


| A.a、b、c对应的混合液中,水的电离程度由大到小的顺序是c>a>b |
| B.b点混合液中c(Na+)>c(CH3COO-) |
C.加入CH3COOH过程中,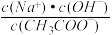 增大 增大 |
D.25℃时,CH3COOH的电离平衡常数Ka= |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】NA为阿伏加德罗常数的值,下列说法正确的是
| A.18 g D2O和18 g H2O中含有的质子数均为10NA |
| B.2 L 0.5 mol·L-1亚硫酸溶液中含有的H+离子数为2NA |
| C.过氧化钠与水反应时,生成0.1 mol氧气转移的电子数为0.2NA |
| D.50 mL 12 mol·L-1盐酸与足量MnO2共热,转移的电子数为0.3NA |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】电位滴定法是根据滴定过程中指示电极电位的变化来确定滴定终点的一种滴定分析方法。常温下,利用盐酸滴定某溶液中碳酸钠的含量,其电位滴定曲线与pH曲线如图所示。(已知碳酸的电离常数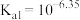 ,
,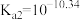 )下列说法正确的是
)下列说法正确的是
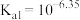 ,
,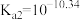 )下列说法正确的是
)下列说法正确的是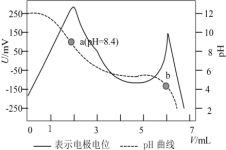
| A.该滴定过程需要两种指示剂 |
B.b点溶液中存在: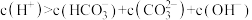 |
C.水的电离程度:a点 b点 b点 |
D.a点溶液中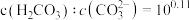 |
您最近一年使用:0次

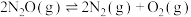 ,其他条件不变时,容器I、Ⅱ、Ⅲ 中
,其他条件不变时,容器I、Ⅱ、Ⅲ 中 的平衡转化率随温度的变化如图所示。
的平衡转化率随温度的变化如图所示。



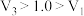
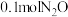 ,平衡向正反应方向移动,
,平衡向正反应方向移动, 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是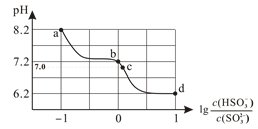
 )=c(SO
)=c(SO )>c(OH-)>c(H+)
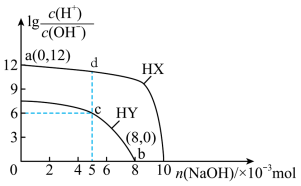
)>c(OH-)>c(H+)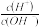 随n(NaOH)的变化如图所示。下列说法正确的是(
随n(NaOH)的变化如图所示。下列说法正确的是(