2024高三·全国·专题练习
1 . 研发CO2、NO利用技术,降低空气中CO2、NO含量成为研究热点。
(1)CO2在固体催化表面加氢合成甲烷过程中发生以下两个反应:
主反应:CO2(g)+4H2(g)⇌CH4(g)+2H2O(g)ΔH1=-156.9 kJ·mol-1
副反应:CO2(g)+H2(g)⇌CO(g)+H2O(g)ΔH2=+41.1 kJ·mol-1
已知:2H2(g)+O2(g)=2H2O(g)ΔH3=-395.6 kJ·mol-1,则CH4燃烧的热化学方程式CH4(g)+2O2(g)=CO2(g)+2H2O(g)ΔH=___________ 。
(2)利用电化学方法通过微生物电催化可将CO2有效地转化为H2C2O4,装置如图所示,阴极的电极反应式为___________ ;当体系的温度升高到一定程度,电极反应的速率反而迅速下降,其主要原因___________ 。___________ 。___________ 。
② 其他条件相同,等离子体的电功率与NO转化率的关系如图所示,当电功率大于30 W时,NO转化率下降的原因可能是___________ 。
(1)CO2在固体催化表面加氢合成甲烷过程中发生以下两个反应:
主反应:CO2(g)+4H2(g)⇌CH4(g)+2H2O(g)ΔH1=-156.9 kJ·mol-1
副反应:CO2(g)+H2(g)⇌CO(g)+H2O(g)ΔH2=+41.1 kJ·mol-1
已知:2H2(g)+O2(g)=2H2O(g)ΔH3=-395.6 kJ·mol-1,则CH4燃烧的热化学方程式CH4(g)+2O2(g)=CO2(g)+2H2O(g)ΔH=
(2)利用电化学方法通过微生物电催化可将CO2有效地转化为H2C2O4,装置如图所示,阴极的电极反应式为

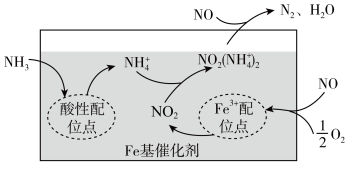
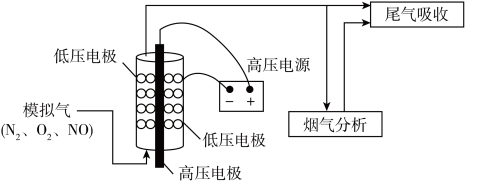
② 其他条件相同,等离子体的电功率与NO转化率的关系如图所示,当电功率大于30 W时,NO转化率下降的原因可能是

您最近半年使用:0次
2 . 如图所示的是以黄铁矿( )为主要原料接触法制硫酸工业的流程示意图(A.沸腾炉 B.接触室 C.吸收塔)
)为主要原料接触法制硫酸工业的流程示意图(A.沸腾炉 B.接触室 C.吸收塔) 接触氧化的反应,下图中的甲、乙、丙分别表示在不同条件下,
接触氧化的反应,下图中的甲、乙、丙分别表示在不同条件下, 在反应混合物中的体积分数(Y)与时间(X)的关系,请按要求填写:
在反应混合物中的体积分数(Y)与时间(X)的关系,请按要求填写:______ 表示有催化剂的情况;
②若乙图两条曲线分别表示不同压强的情况,则______ 表示压强较大的情况;
③若丙图两条曲线分别表示600℃和400℃的情况,则______ 表示600℃的情况。
(2)在生产中常使用过量的空气是为了______ 。
(3)接触法制硫酸的沸腾炉处产生的炉气必须经过净化处理,目的是为了______ 。
(4)从⑤处排出的气体是______(填序号)
(5)在B设备中加热到400℃~500℃是由于①加快反应速率,②______ 。
(6)对从进口⑧喷进的液体的叙述最准确的是______ (填序号)。
A.水 B.98.3%的浓硫酸 C.稀硫酸
(7)吸收塔排出的尾气先用氨水吸收,再用浓硫酸处理得到较高浓度的 和铵盐,
和铵盐, 既可作为生产硫酸的原料循环再利用,也可用于工业制溴过程中吸收潮湿空气中的
既可作为生产硫酸的原料循环再利用,也可用于工业制溴过程中吸收潮湿空气中的 ,请写出
,请写出 吸收
吸收 的离子方程式:
的离子方程式:______ 。
 )为主要原料接触法制硫酸工业的流程示意图(A.沸腾炉 B.接触室 C.吸收塔)
)为主要原料接触法制硫酸工业的流程示意图(A.沸腾炉 B.接触室 C.吸收塔)
 接触氧化的反应,下图中的甲、乙、丙分别表示在不同条件下,
接触氧化的反应,下图中的甲、乙、丙分别表示在不同条件下, 在反应混合物中的体积分数(Y)与时间(X)的关系,请按要求填写:
在反应混合物中的体积分数(Y)与时间(X)的关系,请按要求填写: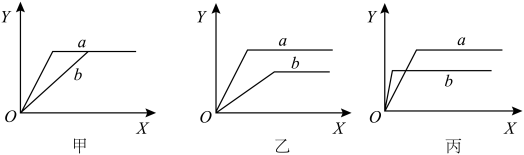
②若乙图两条曲线分别表示不同压强的情况,则
③若丙图两条曲线分别表示600℃和400℃的情况,则
(2)在生产中常使用过量的空气是为了
(3)接触法制硫酸的沸腾炉处产生的炉气必须经过净化处理,目的是为了
(4)从⑤处排出的气体是______(填序号)
A. 、 、 | B. 、 、 | C. 、 、 | D.水蒸气 |
(5)在B设备中加热到400℃~500℃是由于①加快反应速率,②
(6)对从进口⑧喷进的液体的叙述最准确的是
A.水 B.98.3%的浓硫酸 C.稀硫酸
(7)吸收塔排出的尾气先用氨水吸收,再用浓硫酸处理得到较高浓度的
 和铵盐,
和铵盐, 既可作为生产硫酸的原料循环再利用,也可用于工业制溴过程中吸收潮湿空气中的
既可作为生产硫酸的原料循环再利用,也可用于工业制溴过程中吸收潮湿空气中的 ,请写出
,请写出 吸收
吸收 的离子方程式:
的离子方程式:
您最近半年使用:0次
3 . 利用向制取生物柴油的副产物甘油( )中通入一定量的水蒸气,可实现重整制氢。经一系列反应可获得
)中通入一定量的水蒸气,可实现重整制氢。经一系列反应可获得 、CO、
、CO、 、
、 等组成气体,通过调整反应的组成和条件可提高
等组成气体,通过调整反应的组成和条件可提高 产率。请回答:
产率。请回答:
(1)制氢的几个主要反应如下
反应1: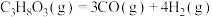
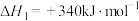
反应2:
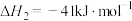
反应3:
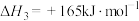
反应4: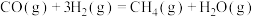

(1)计算
______ ,并判断该反应的自发性______ 。
(2)①温度控制不当,气相产物之间会发生积碳副反应从而影响氢气产率,反应如下:
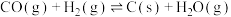
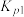 ,
,
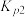 ;若仅考虑积碳副反应,一定温度下,测得在1.0MPa恒压反应体系中达到平衡时组分的分压(即组分的物质的量分数×总压),
;若仅考虑积碳副反应,一定温度下,测得在1.0MPa恒压反应体系中达到平衡时组分的分压(即组分的物质的量分数×总压), ,则平衡常数
,则平衡常数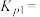
______ 。
②生产过程中,为减小积碳对氢气产率及催化剂的影响,下列措施合适的是______ (填序号)。
A.减小压强 B.通入过量的氧气 C.通入适量的水蒸气 D.选择合适的催化剂
③上述各反应达到平衡时,体系中各物质的物质的量分数受温度的影响如图,请结合图像解释,在图示温度范围内随着温度升高 的摩尔分数先迅速上升后缓慢下降的原因是
的摩尔分数先迅速上升后缓慢下降的原因是______ 。______ (表示在催化剂表面吸附态)(填序号)
A.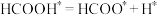
B.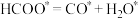
C.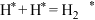
 )中通入一定量的水蒸气,可实现重整制氢。经一系列反应可获得
)中通入一定量的水蒸气,可实现重整制氢。经一系列反应可获得 、CO、
、CO、 、
、 等组成气体,通过调整反应的组成和条件可提高
等组成气体,通过调整反应的组成和条件可提高 产率。请回答:
产率。请回答:(1)制氢的几个主要反应如下
反应1:
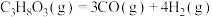
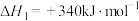
反应2:

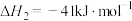
反应3:

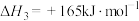
反应4:
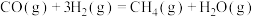

(1)计算

(2)①温度控制不当,气相产物之间会发生积碳副反应从而影响氢气产率,反应如下:
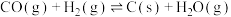
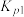 ,
,
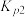 ;若仅考虑积碳副反应,一定温度下,测得在1.0MPa恒压反应体系中达到平衡时组分的分压(即组分的物质的量分数×总压),
;若仅考虑积碳副反应,一定温度下,测得在1.0MPa恒压反应体系中达到平衡时组分的分压(即组分的物质的量分数×总压), ,则平衡常数
,则平衡常数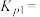
②生产过程中,为减小积碳对氢气产率及催化剂的影响,下列措施合适的是
A.减小压强 B.通入过量的氧气 C.通入适量的水蒸气 D.选择合适的催化剂
③上述各反应达到平衡时,体系中各物质的物质的量分数受温度的影响如图,请结合图像解释,在图示温度范围内随着温度升高
 的摩尔分数先迅速上升后缓慢下降的原因是
的摩尔分数先迅速上升后缓慢下降的原因是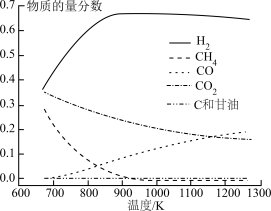
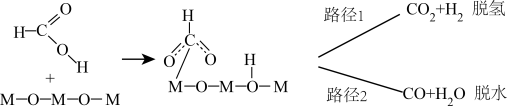
A.
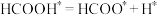
B.
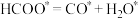
C.
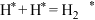
您最近半年使用:0次
4 . 化学与生产、生活密切相关。下列说法错误的是
A.葡萄酒中添加适量的 可以起到杀菌和抗氧化的作用 可以起到杀菌和抗氧化的作用 |
| B.碳酸钡在医疗上可被用作消化系统X射线检查的内服药剂,俗称“钡餐” |
| C.制玻璃过程中加入某些金属氧化物或盐可以得到有色玻璃 |
| D.合成氨工业一般选择400~500℃的主要原因是让催化剂的活性大,反应速率快 |
您最近半年使用:0次
名校
解题方法
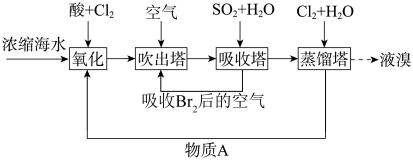
5 . 海洋资源的利用具有广阔的前景。利用空气吹出法从海水中提取溴的流程如图:
(1)“吸收塔”中发生反应的离子方程式为_______ 。
(2)“蒸馏塔”具有将溴单质与水溶液分离的作用,其温度应控制在_____ (填序号)。
A.40∼50℃ B.60∼70℃ C.100℃以上
(3)物质A_____ (填化学式)可以循环利用。
(4)探究“氧化”的适宜条件,测得不同条件下溶液中被氧化的 的百分含量如图:
的百分含量如图: 表示加入氯元素与海水中溴元素物质的量之比。
表示加入氯元素与海水中溴元素物质的量之比。
①结合实际生产,“氧化”的适宜条件为______ 。
②海水中溴元素的浓度是64mg/L,经该方法处理后1m3海水最终得到38.4gBr2,则该实验海水中溴元素的提取率为______ 。
③吸收后的空气进行循环利用,吹出时,吹出塔中 吹出率与吸收塔中
吹出率与吸收塔中 流量的关系如图所示,当
流量的关系如图所示,当 流量过大,
流量过大, 吹出率反而下降,其原因:
吹出率反而下降,其原因:______ 。
(1)“吸收塔”中发生反应的离子方程式为
(2)“蒸馏塔”具有将溴单质与水溶液分离的作用,其温度应控制在
A.40∼50℃ B.60∼70℃ C.100℃以上
(3)物质A
(4)探究“氧化”的适宜条件,测得不同条件下溶液中被氧化的
 的百分含量如图:
的百分含量如图: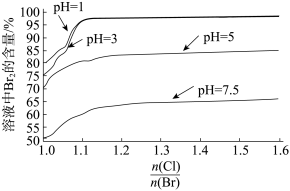
 表示加入氯元素与海水中溴元素物质的量之比。
表示加入氯元素与海水中溴元素物质的量之比。①结合实际生产,“氧化”的适宜条件为
②海水中溴元素的浓度是64mg/L,经该方法处理后1m3海水最终得到38.4gBr2,则该实验海水中溴元素的提取率为
③吸收后的空气进行循环利用,吹出时,吹出塔中
 吹出率与吸收塔中
吹出率与吸收塔中 流量的关系如图所示,当
流量的关系如图所示,当 流量过大,
流量过大, 吹出率反而下降,其原因:
吹出率反而下降,其原因:
您最近半年使用:0次
名校
解题方法
6 . 有关工业固氮的说法正确的是
| A.使用铁催化剂可提高反应物的转化率 |
B.循环使用 、 、 可提高 可提高 的产率 的产率 |
C.温度控制在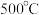 左右有利于反应向正方向进行 左右有利于反应向正方向进行 |
| D.增大压强有利于加快反应速率,所以压强越大越好 |
您最近半年使用:0次
名校
解题方法
7 . 下图所示为工业合成氨的流程图。下列有关生产条件的调控作用分析错误的是
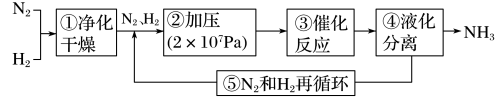
| A.步骤①中“净化”可以防止杂质对催化剂产生影响 |
| B.步骤②中“加压”可以加快反应速率,因此压强越大越好 |
| C.步骤③一般选择控制反应温度为400~500℃左右 |
| D.步骤④⑤有利于提高原料的利用率,能节约生产成本 |
您最近半年使用:0次
名校
解题方法
8 . 氯化钡是重要的化工原料,是制备其他钡盐的主要中间原料,以毒重石(主要成分为 ,还含有
,还含有 及含Ca、Mg、Fe、Al的化合物)为原料制备
及含Ca、Mg、Fe、Al的化合物)为原料制备 的工艺流程如下:
的工艺流程如下: 、
、 、
、 、
、 形式存在于溶液中。
形式存在于溶液中。
回答下列问题:
(1)在“浸取”时,除温度、酸的浓度、液固比等因素影响钡的浸出率外,还有___________ 因素。
(2)下表列举了不同温度、盐酸的浓度、液固比下钡的浸出率实验数据,每个实验只改变一个条件:
分析表中数据,温度越高钡的浸出率越低的可能原因是___________ ;判断“浸取”的最佳液固比为___________ 。
(3)常温时,几种金属离子沉淀的pH如图所示,加 时发生反应的离子方程式为
时发生反应的离子方程式为___________ ;“调pH(Ⅰ)”时,调节溶液 ,则“滤渣Ⅱ”的主要成分为
,则“滤渣Ⅱ”的主要成分为___________ (填化学式)。___________ 。
 ,还含有
,还含有 及含Ca、Mg、Fe、Al的化合物)为原料制备
及含Ca、Mg、Fe、Al的化合物)为原料制备 的工艺流程如下:
的工艺流程如下: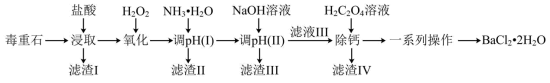
 、
、 、
、 、
、 形式存在于溶液中。
形式存在于溶液中。回答下列问题:
(1)在“浸取”时,除温度、酸的浓度、液固比等因素影响钡的浸出率外,还有
(2)下表列举了不同温度、盐酸的浓度、液固比下钡的浸出率实验数据,每个实验只改变一个条件:
| 改变的条件 | 温度(℃) | 盐酸的浓度(%) | 液固比 | ||||||||
| 30 | 55 | 75 | 10 | 15 | 20 | 25 | 3:1 | 4:1 | 5:1 | 6:1 | |
| 钡的浸出率(%) | 74.31 | 69.60 | 68.42 | 59.21 | 74.31 | 74.15 | 55.32 | 59.84 | 65.12 | 74.31 | 74.35 |
(3)常温时,几种金属离子沉淀的pH如图所示,加
 时发生反应的离子方程式为
时发生反应的离子方程式为 ,则“滤渣Ⅱ”的主要成分为
,则“滤渣Ⅱ”的主要成分为
您最近半年使用:0次
名校
9 . 中国科学家首次实现了二氧化碳到淀粉的从头合成,CO2的捕集、利用与封存成为科学家研究的重要课题。
以CO2、C2H6为原料合成C2H4涉及的主要反应如下:
I.CO2(g)+C2H6(g) C2H4(g)+H2O(g)+CO(g) ΔH=+177kJ·mol-1 (主反应)
C2H4(g)+H2O(g)+CO(g) ΔH=+177kJ·mol-1 (主反应)
II.C2H6(g) CH4(g)+H2(g)+C(s) ΔH=+9kJ·mol-1 (副反应)
CH4(g)+H2(g)+C(s) ΔH=+9kJ·mol-1 (副反应)
(1)反应I的反应历程可分为如下两步:
i. C2H6(g) C2H4(g)+H2(g) ΔH1 (反应速率较快)
C2H4(g)+H2(g) ΔH1 (反应速率较快)
ii. H2(g)+CO2(g) H2O(g)+CO(g) ΔH2=+44kJ·mol-1 (反应速率较慢)
H2O(g)+CO(g) ΔH2=+44kJ·mol-1 (反应速率较慢)
①∆H1=_______
②相比于提高c(C2H6),提高c(CO2)对反应I速率影响更大,原因是_______ 。
(2)向恒压密闭容器中充入CO2和C2H6合成C2H4,发生主反应,温度对催化剂K-Fe-Mn/Si-2性能的影响如图所示,工业生产综合各方面的因素,反应选择800℃的原因是_______ 。 C2H4(g)+2H2(g) ΔH>0,温度T时,向2L的恒容反应器中充入2molCH4,仅发生上述反应,反应过程中CH4的物质的量随时间变化如图所示:
C2H4(g)+2H2(g) ΔH>0,温度T时,向2L的恒容反应器中充入2molCH4,仅发生上述反应,反应过程中CH4的物质的量随时间变化如图所示:
____ (用含有x的代数式表示);当温度升高时,k正增大m倍,k逆增大n倍,则m_____ n(填“>”、“<”或“=”)。
以CO2、C2H6为原料合成C2H4涉及的主要反应如下:
I.CO2(g)+C2H6(g)
 C2H4(g)+H2O(g)+CO(g) ΔH=+177kJ·mol-1 (主反应)
C2H4(g)+H2O(g)+CO(g) ΔH=+177kJ·mol-1 (主反应)II.C2H6(g)
 CH4(g)+H2(g)+C(s) ΔH=+9kJ·mol-1 (副反应)
CH4(g)+H2(g)+C(s) ΔH=+9kJ·mol-1 (副反应)(1)反应I的反应历程可分为如下两步:
i. C2H6(g)
 C2H4(g)+H2(g) ΔH1 (反应速率较快)
C2H4(g)+H2(g) ΔH1 (反应速率较快)ii. H2(g)+CO2(g)
 H2O(g)+CO(g) ΔH2=+44kJ·mol-1 (反应速率较慢)
H2O(g)+CO(g) ΔH2=+44kJ·mol-1 (反应速率较慢)①∆H1=
②相比于提高c(C2H6),提高c(CO2)对反应I速率影响更大,原因是
(2)向恒压密闭容器中充入CO2和C2H6合成C2H4,发生主反应,温度对催化剂K-Fe-Mn/Si-2性能的影响如图所示,工业生产综合各方面的因素,反应选择800℃的原因是
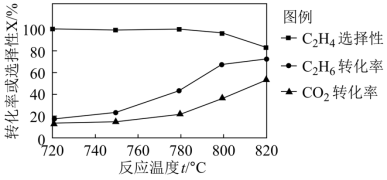
 C2H4(g)+2H2(g) ΔH>0,温度T时,向2L的恒容反应器中充入2molCH4,仅发生上述反应,反应过程中CH4的物质的量随时间变化如图所示:
C2H4(g)+2H2(g) ΔH>0,温度T时,向2L的恒容反应器中充入2molCH4,仅发生上述反应,反应过程中CH4的物质的量随时间变化如图所示: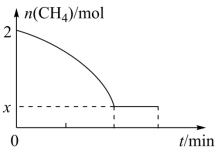

您最近半年使用:0次
10 . 环戊二烯是一种重要的有机合成原料,用其制备环戊烯涉及的反应如下:
(1)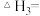
______ (用含“ ”和“
”和“ ”的式子表示),该反应在
”的式子表示),该反应在______ (填“高温”或“低温”)条件下能自发进行。
(2)下列操作中,能提高环戊二烯平衡转化率的是______ (填标号)。
A.增加环戊二烯的用量 B.恒温恒压下通入惰性气体 C.移除环戊烯
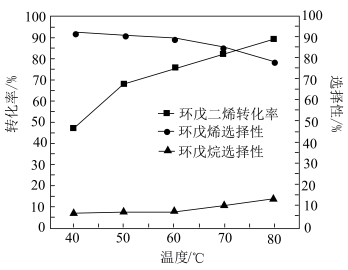
(3)保持其他条件不变,在相同时间内,环戊二烯转化率及环戊烯、环戊烷的选择性与温度的关系如下图所示:______ (填标号)。
A.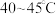 B.
B.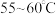 C.
C.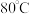 左右
左右
②随着温度的升高,环戊二烯转化率升高而环戊烯选择性降低,其原因是______ 。
(4)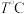 ,向恒容密闭容器中加入
,向恒容密闭容器中加入 环戊二烯
环戊二烯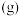 和
和
 ,反应达到平衡时,环戊二烯的转化率为
,反应达到平衡时,环戊二烯的转化率为 ,环戊烷物质的量为
,环戊烷物质的量为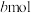 ,则用气体物质的量分数
,则用气体物质的量分数 表示的主反应的平衡常数
表示的主反应的平衡常数
______ (用含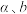 的计算式表示)。
的计算式表示)。
(5)用环戊二烯制备的二茂铁 可用作火箭燃料添加剂、汽油抗爆剂、橡胶熟化剂、紫外线吸收剂等。二茂铁的晶胞结构如图所示(未画出微粒),密度为
可用作火箭燃料添加剂、汽油抗爆剂、橡胶熟化剂、紫外线吸收剂等。二茂铁的晶胞结构如图所示(未画出微粒),密度为 ,设阿伏加德罗常数的值为
,设阿伏加德罗常数的值为 ,则一个晶胞中含
,则一个晶胞中含 的数目为
的数目为______ 。
主反应: ;
;
副反应1: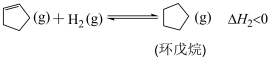 。
。
副反应2:
(1)
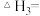
 ”和“
”和“ ”的式子表示),该反应在
”的式子表示),该反应在(2)下列操作中,能提高环戊二烯平衡转化率的是
A.增加环戊二烯的用量 B.恒温恒压下通入惰性气体 C.移除环戊烯
(3)保持其他条件不变,在相同时间内,环戊二烯转化率及环戊烯、环戊烷的选择性与温度的关系如下图所示:
A.
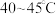 B.
B.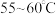 C.
C.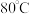 左右
左右②随着温度的升高,环戊二烯转化率升高而环戊烯选择性降低,其原因是
(4)
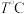 ,向恒容密闭容器中加入
,向恒容密闭容器中加入 环戊二烯
环戊二烯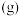 和
和
 ,反应达到平衡时,环戊二烯的转化率为
,反应达到平衡时,环戊二烯的转化率为 ,环戊烷物质的量为
,环戊烷物质的量为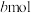 ,则用气体物质的量分数
,则用气体物质的量分数 表示的主反应的平衡常数
表示的主反应的平衡常数
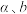 的计算式表示)。
的计算式表示)。(5)用环戊二烯制备的二茂铁
 可用作火箭燃料添加剂、汽油抗爆剂、橡胶熟化剂、紫外线吸收剂等。二茂铁的晶胞结构如图所示(未画出微粒),密度为
可用作火箭燃料添加剂、汽油抗爆剂、橡胶熟化剂、紫外线吸收剂等。二茂铁的晶胞结构如图所示(未画出微粒),密度为 ,设阿伏加德罗常数的值为
,设阿伏加德罗常数的值为 ,则一个晶胞中含
,则一个晶胞中含 的数目为
的数目为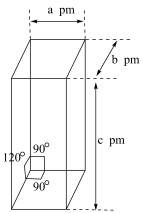
您最近半年使用:0次



