名校
解题方法
1 .  可被用于治疗消化道疾病。某学习探究小组在实验室进行了制备
可被用于治疗消化道疾病。某学习探究小组在实验室进行了制备 以及含量测定的实验。已知:常温下
以及含量测定的实验。已知:常温下 不溶于水,较稳定,与酸反应生成
不溶于水,较稳定,与酸反应生成 ;加热时会分解生成
;加热时会分解生成 和
和 。
。
请回答下列问题:
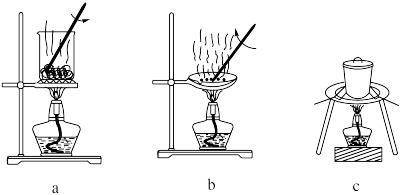
(1)灼烧。灼烧 制
制 时,可使用的实验装置有
时,可使用的实验装置有___________ (填字母)。
(2)转化。向 中先加入稳定剂和
中先加入稳定剂和 溶液,充分反应后,过滤、洗涤、干燥,可得粗品
溶液,充分反应后,过滤、洗涤、干燥,可得粗品 。
。
①写出制备 时发生反应的化学方程式:
时发生反应的化学方程式:___________ 。
②“转化”阶段有大量热量放出,为了提高 的产率,添加
的产率,添加 溶液时,比较理想的操作方法为
溶液时,比较理想的操作方法为___________ 。
(3)测定。某研究小组拟用下图装置测定样品(含 杂质)中
杂质)中 的含量。
的含量。

①实验时在稀盐酸中加入 溶液的作用是
溶液的作用是___________ (用化学方程式表示)。
②为了减小实验误差,在每次读数前需要进行的操作是___________ 、___________ 。
③该小组记录的实验数据如下:样品的质量为 ;反应开始前量气管的读数为
;反应开始前量气管的读数为 ;反应结束冷却到室温后量气管的读数为
;反应结束冷却到室温后量气管的读数为 ,已知:室温条件下气体摩尔体积为
,已知:室温条件下气体摩尔体积为 ,则样品中过氧化镁的质量分数为
,则样品中过氧化镁的质量分数为___________  (用含
(用含 的代数式表示);若反应结束后读取量气管中气体的体积时,液面左低右高,则测得
的代数式表示);若反应结束后读取量气管中气体的体积时,液面左低右高,则测得 的质量分数
的质量分数___________ (填“偏大”“偏小”或“无影响”)。
 可被用于治疗消化道疾病。某学习探究小组在实验室进行了制备
可被用于治疗消化道疾病。某学习探究小组在实验室进行了制备 以及含量测定的实验。已知:常温下
以及含量测定的实验。已知:常温下 不溶于水,较稳定,与酸反应生成
不溶于水,较稳定,与酸反应生成 ;加热时会分解生成
;加热时会分解生成 和
和 。
。请回答下列问题:
(1)灼烧。灼烧
 制
制 时,可使用的实验装置有
时,可使用的实验装置有
(2)转化。向
 中先加入稳定剂和
中先加入稳定剂和 溶液,充分反应后,过滤、洗涤、干燥,可得粗品
溶液,充分反应后,过滤、洗涤、干燥,可得粗品 。
。①写出制备
 时发生反应的化学方程式:
时发生反应的化学方程式:②“转化”阶段有大量热量放出,为了提高
 的产率,添加
的产率,添加 溶液时,比较理想的操作方法为
溶液时,比较理想的操作方法为(3)测定。某研究小组拟用下图装置测定样品(含
 杂质)中
杂质)中 的含量。
的含量。
①实验时在稀盐酸中加入
 溶液的作用是
溶液的作用是②为了减小实验误差,在每次读数前需要进行的操作是
③该小组记录的实验数据如下:样品的质量为
 ;反应开始前量气管的读数为
;反应开始前量气管的读数为 ;反应结束冷却到室温后量气管的读数为
;反应结束冷却到室温后量气管的读数为 ,已知:室温条件下气体摩尔体积为
,已知:室温条件下气体摩尔体积为 ,则样品中过氧化镁的质量分数为
,则样品中过氧化镁的质量分数为 (用含
(用含 的代数式表示);若反应结束后读取量气管中气体的体积时,液面左低右高,则测得
的代数式表示);若反应结束后读取量气管中气体的体积时,液面左低右高,则测得 的质量分数
的质量分数
您最近一年使用:0次
2023-10-06更新
|
797次组卷
|
5卷引用:广西南宁市第二中学2023-2024学年高二上学期11月期中考试化学试题
2 . 通过控制化学反应条件,可以使化学反应速率按我们的需求变化。下列现象的反应速率需要减小的是
| A.用白醋清理水壶中的水垢 | B.作肥料的厨余垃圾的腐败 |
| C.轮胎的老化 | D.汽车尾气的净化 |
您最近一年使用:0次
名校
解题方法
3 . 化学反应速率和限度与生产、生活密切相关。
(1)某温度下, 恒容密闭容器中,X、Y、Z三种物质的物质的量随反应时间的变化曲线如图所示。
恒容密闭容器中,X、Y、Z三种物质的物质的量随反应时间的变化曲线如图所示。

①从反应开始到 内,用
内,用 的浓度变化表示的平均反应速率为
的浓度变化表示的平均反应速率为_______ mol·L-1·min-1。
②该反应的化学方程式为_______ 。
③若 均为气体,在
均为气体,在 时,向容器中通入氩气(容器体积不变),
时,向容器中通入氩气(容器体积不变), 的反应速率将
的反应速率将_______ (填“变大”、“不变”或“变小”)。
④若 均为气体,下列能说明该反应达到平衡状态的是
均为气体,下列能说明该反应达到平衡状态的是_______ (填字母)。
a. 三种气体的浓度相等
三种气体的浓度相等
b.混合气体的质量不随时间变化
c.混合气体的密度不随时间变化
d.单位时间内消耗X和 的物质的量之比为
的物质的量之比为
(2)实验室用 溶液与
溶液与 溶液反应探究条件的改变对化学反应速率的影响,设计的实验方案如下表(已知
溶液反应探究条件的改变对化学反应速率的影响,设计的实验方案如下表(已知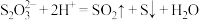 ):
):
①对比实验1和2可探究_______ 因素对化学反应速率的影响。
②对比实验1和3来探究浓度对化学反应速率的影响,则
_______ ,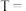
_______ 。
(1)某温度下,
 恒容密闭容器中,X、Y、Z三种物质的物质的量随反应时间的变化曲线如图所示。
恒容密闭容器中,X、Y、Z三种物质的物质的量随反应时间的变化曲线如图所示。
①从反应开始到
 内,用
内,用 的浓度变化表示的平均反应速率为
的浓度变化表示的平均反应速率为②该反应的化学方程式为
③若
 均为气体,在
均为气体,在 时,向容器中通入氩气(容器体积不变),
时,向容器中通入氩气(容器体积不变), 的反应速率将
的反应速率将④若
 均为气体,下列能说明该反应达到平衡状态的是
均为气体,下列能说明该反应达到平衡状态的是a.
 三种气体的浓度相等
三种气体的浓度相等b.混合气体的质量不随时间变化
c.混合气体的密度不随时间变化
d.单位时间内消耗X和
 的物质的量之比为
的物质的量之比为
(2)实验室用
 溶液与
溶液与 溶液反应探究条件的改变对化学反应速率的影响,设计的实验方案如下表(已知
溶液反应探究条件的改变对化学反应速率的影响,设计的实验方案如下表(已知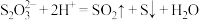 ):
):| 实验序号 | 体积/ | 温度/ | 溶液出现浑浊的时间/s | ||
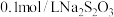 溶液 溶液 | 水 | 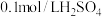 溶液 溶液 | |||
| 1 | 2.0 | 0.0 | 2.0 | 25 |  |
| 2 | 2.0 | 0.0 | 2.0 | 50 |  |
| 3 | 1.0 | V | 2.0 | T |  |
②对比实验1和3来探究浓度对化学反应速率的影响,则

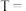
您最近一年使用:0次
2023-07-28更新
|
277次组卷
|
2卷引用:广西南宁市第八中学2023-2024学年高二上学期开学考化学试题
名校
解题方法
4 . 关于合成氨反应
 ,下列说法不正确的是
,下列说法不正确的是

 ,下列说法不正确的是
,下列说法不正确的是| A.使用高效催化剂能减小反应活化能 |
B.为了提高原料利用率, 和 和 循环使用 循环使用 |
C.工业合成氨温度为700K是因为升高温度有利于提高 的平衡转化率 的平衡转化率 |
| D.恒温恒容下,若体系的总压强不再改变,说明该反应已达平衡状态 |
您最近一年使用:0次
2023-07-16更新
|
226次组卷
|
3卷引用:广西百色市德保高中2023-2024学年高二上学期11月期中考试化学试题
广西百色市德保高中2023-2024学年高二上学期11月期中考试化学试题福建省宁德市区域性学业质量检测2022-2023学年高二上学期2月期末考试化学试题(已下线)专题05 化学反应的方向 化学反应的调控 -【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(人教版2019)
名校
解题方法
5 . 工业上以软锰矿(主要成分为 ,还含有少量
,还含有少量 )和辉钼矿(主要成分为为
)和辉钼矿(主要成分为为 ,还含有少量Si、Ni的氧化物)为原料,制备四钼酸铵晶体
,还含有少量Si、Ni的氧化物)为原料,制备四钼酸铵晶体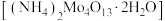 和硫酸锰晶体的工艺流程如下。
和硫酸锰晶体的工艺流程如下。

已知: ,常温下,NiS和MnS的
,常温下,NiS和MnS的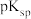 分别为19.4和12.6;
分别为19.4和12.6; 。
。
回答下列问题:
(1)为了提高焙烧效率,可以采取的措施有___________ (写一条即可);“高温焙烧”时 、
、 转化为
转化为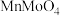 、
、 ,写出该反应的化学方程式
,写出该反应的化学方程式___________ 。
(2)“酸浸”时,硫酸浓度对Mo、Mn浸出率的影响如图所示。

“酸浸”时硫酸的最佳浓度为___________  ,理由是
,理由是___________ 。
(3)黄钠铁矾的化学式为 ,生成黄钠铁矾的离子方程式为
,生成黄钠铁矾的离子方程式为___________ ;“除铁”后的溶液中 ,当溶液中可溶组分浓度
,当溶液中可溶组分浓度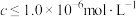 时,可认为已除尽,则“除镍”应控制溶液pH的范围是
时,可认为已除尽,则“除镍”应控制溶液pH的范围是___________ [已知 ,该溶液中
,该溶液中 和pH的关系为
和pH的关系为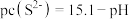 ;忽略溶液体积变化]。
;忽略溶液体积变化]。
(4)“萃取”的原理为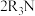 (叔胺)
(叔胺)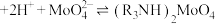 ,则“反萃取”中的试剂X最适宜选用
,则“反萃取”中的试剂X最适宜选用___________ (填标号)。
a.稀硫酸 b. 溶液 c.NaOH溶液 d.氨水
溶液 c.NaOH溶液 d.氨水
从“母液”中回收的副产品主要是___________ (填名称)。
 ,还含有少量
,还含有少量 )和辉钼矿(主要成分为为
)和辉钼矿(主要成分为为 ,还含有少量Si、Ni的氧化物)为原料,制备四钼酸铵晶体
,还含有少量Si、Ni的氧化物)为原料,制备四钼酸铵晶体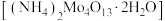 和硫酸锰晶体的工艺流程如下。
和硫酸锰晶体的工艺流程如下。
已知:
 ,常温下,NiS和MnS的
,常温下,NiS和MnS的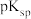 分别为19.4和12.6;
分别为19.4和12.6; 。
。回答下列问题:
(1)为了提高焙烧效率,可以采取的措施有
 、
、 转化为
转化为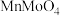 、
、 ,写出该反应的化学方程式
,写出该反应的化学方程式(2)“酸浸”时,硫酸浓度对Mo、Mn浸出率的影响如图所示。

“酸浸”时硫酸的最佳浓度为
 ,理由是
,理由是(3)黄钠铁矾的化学式为
 ,生成黄钠铁矾的离子方程式为
,生成黄钠铁矾的离子方程式为 ,当溶液中可溶组分浓度
,当溶液中可溶组分浓度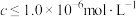 时,可认为已除尽,则“除镍”应控制溶液pH的范围是
时,可认为已除尽,则“除镍”应控制溶液pH的范围是 ,该溶液中
,该溶液中 和pH的关系为
和pH的关系为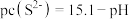 ;忽略溶液体积变化]。
;忽略溶液体积变化]。(4)“萃取”的原理为
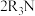 (叔胺)
(叔胺)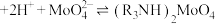 ,则“反萃取”中的试剂X最适宜选用
,则“反萃取”中的试剂X最适宜选用a.稀硫酸 b.
 溶液 c.NaOH溶液 d.氨水
溶液 c.NaOH溶液 d.氨水从“母液”中回收的副产品主要是
您最近一年使用:0次
2023-05-12更新
|
593次组卷
|
2卷引用:广西南宁市第二中学2023-2024学年高三10月教学质量调研化学试题
解题方法
6 . 氮的氧化物(NOx)是大气主要污染物,有效去除大气中的NOx是环境保护的重要课题。
(1)N2O又称笑气,有轻微的麻醉作用,N2O在一定条件下可分解为N2、O2。回答下列问题:
已知:①N2(g)+O2(g)=2NO(g) ΔH1=+180.5kJ/mol
②2NO(g)+O2(g)=2NO2(g) ΔH2=-114.14kJ/mol
③3NO(g)=N2O(g)+NO2(g) ΔH3=-115.52kJ/mol
则反应2NO2(g)=N2(g)+2O2(g) ΔH=_____ kJ/mol。
(2)汽车尾气中的NO和CO可在催化剂作用下生成无污染的气体而除去。在密闭容器中充入10molCO和8molNO发生反应,测得平衡时NO的体积分数与温度、压强的关系如图:
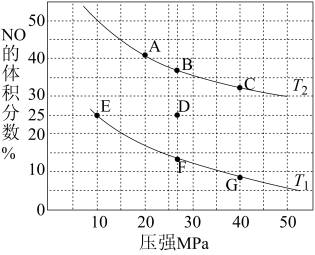
①已知T2>T1,则反应2NO(g)+2CO(g) N2(g)+2CO2(g),ΔH
N2(g)+2CO2(g),ΔH_____ 0(填“>”“=”或“<”)。
②该反应达到平衡后,为同时提高反应速率和NO的转化率,可采取的措施有_____ (填字母序号)。
a.改用高效催化剂 b.缩小容器的体积 c.增加CO的浓度 d.升高温度
③压强为10MPa、温度为T1下,若反应进行到10min达到平衡状态,压强保持不变,此时容器的体积为4L,则用N2的浓度变化表示的平均反应速率v(N2)=____ ,该温度下用分压表示的平衡常数Kp=____ MPa-1(分压=总压×物质的量分数)。
④在D点,对反应容器升温的同时扩大体积至体系压强减小,重新达到的平衡状态可能是图中A~G点中_____ 点。
(3)在有氧条件下,新型催化剂M能催化NH3与NOx反应生成N2,将一定比例的O2、NH3和NOx的混合气体匀速通入装有催化剂M的反应器中反应,反应相同时间,NOx的去除率随反应温度的变化曲线如图所示。
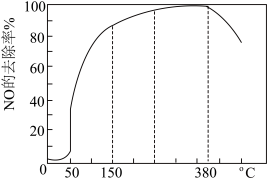
问:在50℃~150℃范围内随温度升高,NOx的去除率迅速上升的原因是_____ 。
(1)N2O又称笑气,有轻微的麻醉作用,N2O在一定条件下可分解为N2、O2。回答下列问题:
已知:①N2(g)+O2(g)=2NO(g) ΔH1=+180.5kJ/mol
②2NO(g)+O2(g)=2NO2(g) ΔH2=-114.14kJ/mol
③3NO(g)=N2O(g)+NO2(g) ΔH3=-115.52kJ/mol
则反应2NO2(g)=N2(g)+2O2(g) ΔH=
(2)汽车尾气中的NO和CO可在催化剂作用下生成无污染的气体而除去。在密闭容器中充入10molCO和8molNO发生反应,测得平衡时NO的体积分数与温度、压强的关系如图:

①已知T2>T1,则反应2NO(g)+2CO(g)
 N2(g)+2CO2(g),ΔH
N2(g)+2CO2(g),ΔH②该反应达到平衡后,为同时提高反应速率和NO的转化率,可采取的措施有
a.改用高效催化剂 b.缩小容器的体积 c.增加CO的浓度 d.升高温度
③压强为10MPa、温度为T1下,若反应进行到10min达到平衡状态,压强保持不变,此时容器的体积为4L,则用N2的浓度变化表示的平均反应速率v(N2)=
④在D点,对反应容器升温的同时扩大体积至体系压强减小,重新达到的平衡状态可能是图中A~G点中
(3)在有氧条件下,新型催化剂M能催化NH3与NOx反应生成N2,将一定比例的O2、NH3和NOx的混合气体匀速通入装有催化剂M的反应器中反应,反应相同时间,NOx的去除率随反应温度的变化曲线如图所示。

问:在50℃~150℃范围内随温度升高,NOx的去除率迅速上升的原因是
您最近一年使用:0次
名校
7 . 合成氨反应为
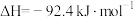 。下列有关该反应的说法正确的是
。下列有关该反应的说法正确的是

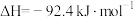 。下列有关该反应的说法正确的是
。下列有关该反应的说法正确的是| A.催化剂增大了正、逆反应的活化能 |
| B.升高温度,该反应的平衡常数增大 |
| C.正反应的活化能小于逆反应的活化能 |
D.反应在高温、高压和催化剂条件下进行可提高 的平衡转化率 的平衡转化率 |
您最近一年使用:0次
2022-07-02更新
|
836次组卷
|
4卷引用:广西北海市2021-2022学年高二下学期期末检测化学试题
广西北海市2021-2022学年高二下学期期末检测化学试题(已下线)2.4 化学反应的调控-2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)(已下线)2.4.1 合成氨生产适宜条件的选择-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)河北省衡水市第二中学2023-2024学年高二上学期开学考试化学试题
名校
8 . 用于净化汽车尾气的反应:2NO(g)+2CO(g) 2CO2(g)+N2(g),已知常温下该反应速率极慢,570K时平衡常数为1×1059。下列说法正确的是
2CO2(g)+N2(g),已知常温下该反应速率极慢,570K时平衡常数为1×1059。下列说法正确的是
 2CO2(g)+N2(g),已知常温下该反应速率极慢,570K时平衡常数为1×1059。下列说法正确的是
2CO2(g)+N2(g),已知常温下该反应速率极慢,570K时平衡常数为1×1059。下列说法正确的是| A.该反应在常温下进行不需要催化剂 |
| B.提高尾气净化效率的最佳途径是研制高效催化剂 |
| C.装有尾气净化装置的汽车排出的气体中不再含有NO或CO |
| D.570K时该反应正向进行的程度很大,故使用催化剂并无实际意义 |
您最近一年使用:0次
2022-04-11更新
|
97次组卷
|
2卷引用:广西柳州市第三中学2022-2023学年高二上学期10月月考化学试题
9 . 2019年12月4日“全球碳计划”发布报告说,全球 排放量增速趋缓。人们还需要更有力的政策来逐步淘汰化石燃料的使用。
排放量增速趋缓。人们还需要更有力的政策来逐步淘汰化石燃料的使用。 的综合利用是解决温室问题的有效途径。
的综合利用是解决温室问题的有效途径。
(1)一种途径是用 转化为成为有机物实现碳循环。如:
转化为成为有机物实现碳循环。如:
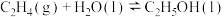
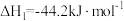

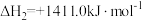 。
。
①已知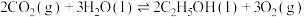 ,其正反应的活化能为
,其正反应的活化能为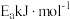 ,则逆反应的活化能为
,则逆反应的活化能为___________  。
。
②工业生产用氯乙烷在碱性条件下水解获得乙醇,反应的离子方程式为 ,已知:
,已知: 为速率方程,研究表明,
为速率方程,研究表明, 浓度减半,反应速率减半,而
浓度减半,反应速率减半,而 浓度减半对反应速率没有影响,则反应速率方程式为
浓度减半对反应速率没有影响,则反应速率方程式为___________ (用含有k的表达式表示)。
(2)利用工业废气中的CO2可以制取甲醇和水蒸气,一定条件下,往2L恒容密闭容器中充入1molCO2和3molH2,在不同催化剂作用下发生反应I、反应II与反应III,相同时间内CO2的转化率随温度变化如图所示:
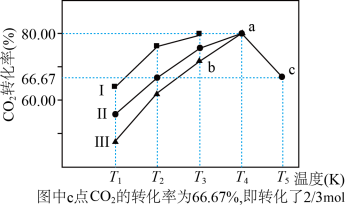
①催化剂效果最佳的反应是___________ (填“曲线I”“曲线II”或“曲线III”)对应的反应。
②b点,v(正)___________ (填“>”,“<”,“=”)v(逆)。
③若此反应在a点时已达平衡状态,a点的转化率比c点高的原因是___________ 。
④c点时该反应的平衡常数K=___________ 。
(3)用钌的配合物作催化剂,一定条件下可直接光催化分解 ,发生反应:
,发生反应:
①该反应的
___________ 0(填“>”“<”“=”),
②
___________ 0(填“>”“<”“=”),③在低温下,该反应___________ 自发进行(填“能”或“不能”)。
 排放量增速趋缓。人们还需要更有力的政策来逐步淘汰化石燃料的使用。
排放量增速趋缓。人们还需要更有力的政策来逐步淘汰化石燃料的使用。 的综合利用是解决温室问题的有效途径。
的综合利用是解决温室问题的有效途径。(1)一种途径是用
 转化为成为有机物实现碳循环。如:
转化为成为有机物实现碳循环。如: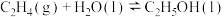
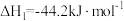

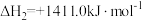 。
。①已知
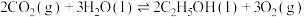 ,其正反应的活化能为
,其正反应的活化能为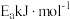 ,则逆反应的活化能为
,则逆反应的活化能为 。
。②工业生产用氯乙烷在碱性条件下水解获得乙醇,反应的离子方程式为
 ,已知:
,已知: 为速率方程,研究表明,
为速率方程,研究表明, 浓度减半,反应速率减半,而
浓度减半,反应速率减半,而 浓度减半对反应速率没有影响,则反应速率方程式为
浓度减半对反应速率没有影响,则反应速率方程式为(2)利用工业废气中的CO2可以制取甲醇和水蒸气,一定条件下,往2L恒容密闭容器中充入1molCO2和3molH2,在不同催化剂作用下发生反应I、反应II与反应III,相同时间内CO2的转化率随温度变化如图所示:

①催化剂效果最佳的反应是
②b点,v(正)
③若此反应在a点时已达平衡状态,a点的转化率比c点高的原因是
④c点时该反应的平衡常数K=
(3)用钌的配合物作催化剂,一定条件下可直接光催化分解
 ,发生反应:
,发生反应:
①该反应的

②

您最近一年使用:0次
2021-12-05更新
|
202次组卷
|
2卷引用: 广西钦州市2022-2023学年高二上学期第2次教学质量监测化学试卷
名校
10 . 由丙烯合成正丁醛的反应: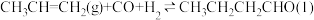 。该反应为正向放热的可逆反应,为增大反应速率和提高原料气的转化率,你认为应该采用的适宜反应条件是
。该反应为正向放热的可逆反应,为增大反应速率和提高原料气的转化率,你认为应该采用的适宜反应条件是
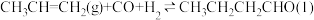 。该反应为正向放热的可逆反应,为增大反应速率和提高原料气的转化率,你认为应该采用的适宜反应条件是
。该反应为正向放热的可逆反应,为增大反应速率和提高原料气的转化率,你认为应该采用的适宜反应条件是| A.低温、高压、催化剂 | B.适当的温度、高压、催化剂 |
| C.常温、常压、催化剂 | D.适当的温度、常压、催化剂 |
您最近一年使用:0次
2021-10-13更新
|
173次组卷
|
4卷引用:广西浦北中学2021-2022学年高二上学期第一次月考化学试题



