解题方法
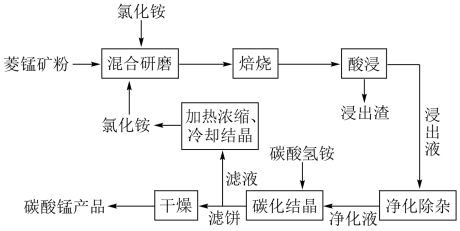
1 . 工业采用氯化铵焙烧菱锰矿制备高纯碳酸锰的流程如图所示: 其余为
其余为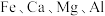 等元素。
等元素。
②部分阳离子沉淀时溶液的 :
:
③“焙烧”过程中主要反应为 。
。
(1)结合图1、2、3,分析“焙烧”过程中最佳的焙烧温度、焙烧时间、 分别为
分别为___________ 、___________ 、___________ 。 ,作用是
,作用是___________ ,再调节溶液 的范围为
的范围为___________ ,将 和
和 变为沉淀而除去,然后加入
变为沉淀而除去,然后加入 将
将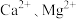 变为氟化物沉淀除去。
变为氟化物沉淀除去。
(3)“碳化结晶”步骤中,加入碳酸氢铵时反应的离子方程式为___________ 。
(4)上述流程中可循环使用的物质是___________ (填化学式)。
(5)现用滴定法测定产品中锰的含量。实验步骤:称取 试样,向其中加入稍过量的磷酸和硝酸,加热使产品中
试样,向其中加入稍过量的磷酸和硝酸,加热使产品中 完全转化为
完全转化为 (其中
(其中 转化为
转化为 );加入稍过量的硫酸铵,发生反应
);加入稍过量的硫酸铵,发生反应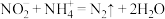 以除去
以除去 ;加入稀硫酸酸化,用
;加入稀硫酸酸化,用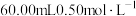 硫酸亚铁铵标准溶液进行滴定,发生的反应为
硫酸亚铁铵标准溶液进行滴定,发生的反应为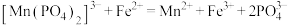 ;用
;用 酸性
酸性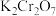 溶液恰好除去过量的
溶液恰好除去过量的 。
。
①酸性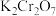 溶液与
溶液与 反应的离子方程式为
反应的离子方程式为___________ 。
②试样中锰的质量分数为___________ 。
 其余为
其余为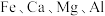 等元素。
等元素。②部分阳离子沉淀时溶液的
 :
:| 离子 |  |  |  |  |  |
开始沉淀的 | 4.1 | 2.2 | 10.6 | 8.1 | 9.1 |
沉淀完全的 | 4.7 | 3.2 | 13.1 | 10.1 | 11.1 |
 。
。(1)结合图1、2、3,分析“焙烧”过程中最佳的焙烧温度、焙烧时间、
 分别为
分别为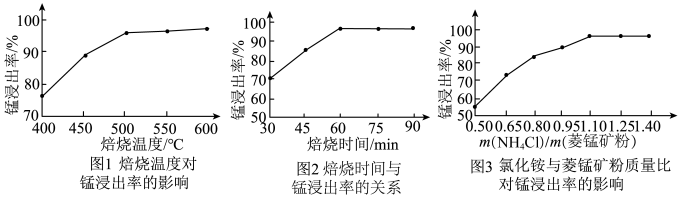
 ,作用是
,作用是 的范围为
的范围为 和
和 变为沉淀而除去,然后加入
变为沉淀而除去,然后加入 将
将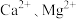 变为氟化物沉淀除去。
变为氟化物沉淀除去。(3)“碳化结晶”步骤中,加入碳酸氢铵时反应的离子方程式为
(4)上述流程中可循环使用的物质是
(5)现用滴定法测定产品中锰的含量。实验步骤:称取
 试样,向其中加入稍过量的磷酸和硝酸,加热使产品中
试样,向其中加入稍过量的磷酸和硝酸,加热使产品中 完全转化为
完全转化为 (其中
(其中 转化为
转化为 );加入稍过量的硫酸铵,发生反应
);加入稍过量的硫酸铵,发生反应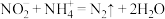 以除去
以除去 ;加入稀硫酸酸化,用
;加入稀硫酸酸化,用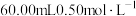 硫酸亚铁铵标准溶液进行滴定,发生的反应为
硫酸亚铁铵标准溶液进行滴定,发生的反应为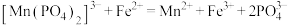 ;用
;用 酸性
酸性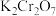 溶液恰好除去过量的
溶液恰好除去过量的 。
。①酸性
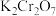 溶液与
溶液与 反应的离子方程式为
反应的离子方程式为②试样中锰的质量分数为
您最近一年使用:0次
名校
解题方法
2 . 肼(N2H4)的熔点2.0℃、沸点113.5℃,极易溶于水,在碱性介质中具有还原性。在强碱性介质中,用次氯酸钠氧化尿素[CO(NH2)2]可得粗肼,再经蒸馏得到肼溶液。回答下列问题:
I.制备NaClO强碱性溶液
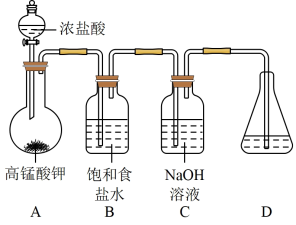
(1)在加入实验药品之前必须进行的操作是_______ 。
(2)A为氯气发生装置,A中反应的化学方程式是_______ 。
(3)次氯酸钠高于35℃容易分解。制备NaClO 强碱性溶液时需要注意的两个关键问题是_______ 。
II.制备N2H4

(4)仪器F的名称是_______ 。
(5)通入N2目的是_______ 。
(6)次氯酸钠氧化尿素的温度一般控制在105~108℃。E中制得肼的离子方程式为_______ .。
(7)向三颈烧瓶中加入NaClO强碱性溶液应当_______ . (填“一次大量”或“分批少量”)加入,充分反应后制得粗肼。蒸馏提纯时应调节控温槽的温度略高于_______ ℃,得到肼溶液。
I.制备NaClO强碱性溶液

(1)在加入实验药品之前必须进行的操作是
(2)A为氯气发生装置,A中反应的化学方程式是
(3)次氯酸钠高于35℃容易分解。制备NaClO 强碱性溶液时需要注意的两个关键问题是
II.制备N2H4

(4)仪器F的名称是
(5)通入N2目的是
(6)次氯酸钠氧化尿素的温度一般控制在105~108℃。E中制得肼的离子方程式为
(7)向三颈烧瓶中加入NaClO强碱性溶液应当
您最近一年使用:0次
2021-03-05更新
|
585次组卷
|
3卷引用:青海省西宁市2021届高三复习检测一(一模)理科综合化学试题
解题方法
3 . 研究氮氧化物的反应机理,对于消除其对环境的污染具有重要意义。
(1)升高温度,绝大多数的化学反应速率增大,但是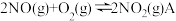 的反应速率却随着温度的升高而减小。查阅资料得知,该反应历程分为以下两步:
的反应速率却随着温度的升高而减小。查阅资料得知,该反应历程分为以下两步:
Ⅰ.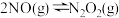 (快)
(快) 
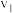 正
正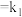 正
正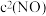
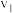 逆
逆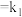 逆
逆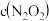
Ⅱ.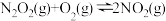 (慢)
(慢) 
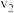 正
正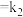 正
正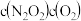
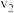 逆
逆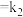 逆
逆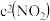
回答:
①反应 的
的
____ (用含 和
和 的式子表示)。一定温度下,反应
的式子表示)。一定温度下,反应 达到平衡状态,写出用
达到平衡状态,写出用 正、
正、 逆、
逆、 正、
正、 逆表示的平衡常数表达式
逆表示的平衡常数表达式
____ 。
②决定 反应速率的是反应Ⅱ,则反应Ⅰ的活化能
反应速率的是反应Ⅱ,则反应Ⅰ的活化能 与反应Ⅱ的活化能
与反应Ⅱ的活化能 的大小关系为
的大小关系为
____  (填“
(填“ ”“
”“ ”或“
”或“ ”)。
”)。
(2)亚硝酸氯( )是有机合成中重要的试剂,可
)是有机合成中重要的试剂,可 与
与 在一定条件下合成。在
在一定条件下合成。在 容器恒温条件下,将物质的量之和为
容器恒温条件下,将物质的量之和为 的
的 和
和 以不同的氮氯比进行如下反应:
以不同的氮氯比进行如下反应: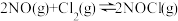
 ,平衡时某反应物的转化率与氮氯比及不同温度的关系结果如下图。
,平衡时某反应物的转化率与氮氯比及不同温度的关系结果如下图。
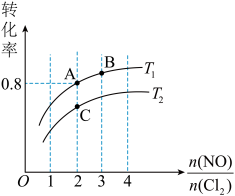
①判断图中温度 、
、 的关系:
的关系:
____  。(填“
。(填“ ”、“
”、“ ”或“
”或“ ”)
”)
②图中纵坐标为物质____ (填化学式)的转化率,理由是_____ 。
③图中 、
、 、
、 三点中平衡时
三点中平衡时 体积分数最大的是
体积分数最大的是____ 。(填“ ”、“
”、“ ”或“
”或“ ”)
”)
④ 温度下,该反应的平衡常数
温度下,该反应的平衡常数
____ 。
(1)升高温度,绝大多数的化学反应速率增大,但是
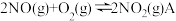 的反应速率却随着温度的升高而减小。查阅资料得知,该反应历程分为以下两步:
的反应速率却随着温度的升高而减小。查阅资料得知,该反应历程分为以下两步:Ⅰ.
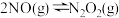 (快)
(快) 
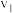 正
正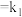 正
正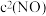
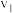 逆
逆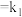 逆
逆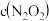
Ⅱ.
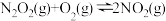 (慢)
(慢) 
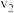 正
正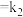 正
正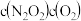
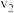 逆
逆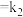 逆
逆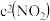
回答:
①反应
 的
的
 和
和 的式子表示)。一定温度下,反应
的式子表示)。一定温度下,反应 达到平衡状态,写出用
达到平衡状态,写出用 正、
正、 逆、
逆、 正、
正、 逆表示的平衡常数表达式
逆表示的平衡常数表达式
②决定
 反应速率的是反应Ⅱ,则反应Ⅰ的活化能
反应速率的是反应Ⅱ,则反应Ⅰ的活化能 与反应Ⅱ的活化能
与反应Ⅱ的活化能 的大小关系为
的大小关系为
 (填“
(填“ ”“
”“ ”或“
”或“ ”)。
”)。(2)亚硝酸氯(
 )是有机合成中重要的试剂,可
)是有机合成中重要的试剂,可 与
与 在一定条件下合成。在
在一定条件下合成。在 容器恒温条件下,将物质的量之和为
容器恒温条件下,将物质的量之和为 的
的 和
和 以不同的氮氯比进行如下反应:
以不同的氮氯比进行如下反应: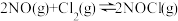
 ,平衡时某反应物的转化率与氮氯比及不同温度的关系结果如下图。
,平衡时某反应物的转化率与氮氯比及不同温度的关系结果如下图。
①判断图中温度
 、
、 的关系:
的关系:
 。(填“
。(填“ ”、“
”、“ ”或“
”或“ ”)
”)②图中纵坐标为物质
③图中
 、
、 、
、 三点中平衡时
三点中平衡时 体积分数最大的是
体积分数最大的是 ”、“
”、“ ”或“
”或“ ”)
”)④
 温度下,该反应的平衡常数
温度下,该反应的平衡常数
您最近一年使用:0次
名校
解题方法
4 . 下列过程中,需要增大化学反应速率的是
| A.钢铁腐蚀 | B.食物腐败 | C.塑料老化 | D.工业合成氮 |
您最近一年使用:0次
2020-04-22更新
|
333次组卷
|
19卷引用:2015-2016学年青海省西宁四中高二上学期期末化学试卷
2015-2016学年青海省西宁四中高二上学期期末化学试卷(已下线)2010-2011学年江西省鄱阳县油墩街中学高一下学期期中考试化学试卷(已下线)2013-2014浙江省宁波市高一下学期期末考试化学试卷2014-2015学年广东省惠州市高一下学期期末考试化学文科试卷2015-2016学年四川省广安二中高一下学期期中化学试卷2016-2017学年河北省武邑中学高二上入学考试化学试卷2016-2017学年河北省武邑中学高二上8.28周考化学卷2016-2017学年河北省武邑中学高二上9.21周考化学卷2016-2017学年天津市河东区高二上学期期中质检化学试卷湖北省天门市三校2016-2017学年高一下学期期中考试化学试题山西省怀仁县第八中学2016-2017学年高一(普通班)下学期期末考试化学试题福建省三明市第一中学2017-2018学年高二上学期期中考试(理)化学试题【全国百强校】福建省三明市第一中学2018-2019学年高二(理)上学期期中考试化学试题江西省上饶市鄱阳县第二中学2019-2020学年高二上学期期中考试化学试题河南省周口市陈州高级中学2019-2020学年高一下学期摸底考试化学试题山西省新绛县第二中学2019-2020学年高二上学期第一次考试化学试题江苏省盐城市伍佑中学2020-2021学年高一下学期第一次阶段考试化学试题江苏省镇江实验高级中学2020-2021学年高一下学期第一次月考化学试题北京景山学校2021-2022学年高一下学期期中考试化学试题
名校
解题方法
5 . 化学反应中常伴随着能量变化。将Al条打磨后,插入6 mol/L盐酸中。
(1)Al与盐酸反应的离子方程式是________ 。
(2)该反应的能量变化可用下图中的________ 表示(填序号)。
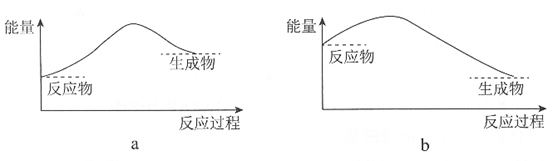
(3)H2的产生速率随时间的变化如图所示。

t1~t2速率变化的主要原因是________ 。
t2~t3速率变化的主要原因是________ 。
(1)Al与盐酸反应的离子方程式是
(2)该反应的能量变化可用下图中的

(3)H2的产生速率随时间的变化如图所示。

t1~t2速率变化的主要原因是
t2~t3速率变化的主要原因是
您最近一年使用:0次
2018-09-20更新
|
271次组卷
|
3卷引用:青海省海东市第二中学2020-2021学年高一下学期期中考试化学试题
6 . 氮是生产硝酸、尿素等物质的重要原料。
(1)氨催化氧化法是工业制硝酸的主要方法。已知:
2NO(g)+3H2(g) 2NH3(g)+02(g) △H1=-272.9kJ/mol
2NH3(g)+02(g) △H1=-272.9kJ/mol
2H2(g)+02(g) 2H2O(g) △H2=-483.6kJ/mol
2H2O(g) △H2=-483.6kJ/mol
则4NH3(g)+5O2(g) 4NO(g)+6H2O(g) △H3=
4NO(g)+6H2O(g) △H3=__________
(2)恒容密闭容器中进行合成知反应:N2(g)+3H2(g) 2NH3(g) △H4==-92.4kJ/mol,其化学平衡常数(K)与温度的关系如下表:
2NH3(g) △H4==-92.4kJ/mol,其化学平衡常数(K)与温度的关系如下表:
K1____ K2(填“>”或“<”),其判断理由是_____________ 。
(3)向氨合成塔中充入10molN2和40molH2合成氨,一定温度(T)下平衡混合物中氨气的体积分数与压强(p)的关系如图1所示。
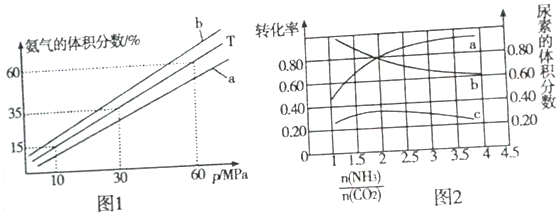
①下列说法正确的是______ (填字母)。
A.由图1可知增大体系压强(p)有利于增大氨气在混合气体中的体积分数
B.若图1中T=500℃,则温度为450℃时对应的曲线是b
C.工业上采用500℃温度的主要目的是提高氮气的转化率
D.当3v正(H2)=2v逆(NH3)时,反应达到平衡状态
②当温度为T、氨气的体积分数为25%时,N2的转化率为__________ 。
(4)工业上用NH3生产硝酸时,将NH3和O2按体积比1:2混合通入某特定条件的密闭容器中进行反应,所有物质不与外界交换,最后得到溶液中溶质的质量分数为_______ 。
(5)氮碳比[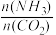 ]对合成尿素的反应:2NH3(g)+CO2(g)
]对合成尿素的反应:2NH3(g)+CO2(g) CO(NH2)2(g)+H2O(g)有影响。T℃时,在2L的恒容密闭容器中,将物质的量之和为3mol的NH3和CO2以不同的氨碳比进行反应,结果如图2所示,a、b分别表示CO2成NH3的转化率,c表示平衡体系中尿素的体积分数,当
CO(NH2)2(g)+H2O(g)有影响。T℃时,在2L的恒容密闭容器中,将物质的量之和为3mol的NH3和CO2以不同的氨碳比进行反应,结果如图2所示,a、b分别表示CO2成NH3的转化率,c表示平衡体系中尿素的体积分数,当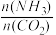 =
=_______ 时,尿素的产量最大,该条件下反应的平衡常数K=________ 。
(1)氨催化氧化法是工业制硝酸的主要方法。已知:
2NO(g)+3H2(g)
 2NH3(g)+02(g) △H1=-272.9kJ/mol
2NH3(g)+02(g) △H1=-272.9kJ/mol 2H2(g)+02(g)
 2H2O(g) △H2=-483.6kJ/mol
2H2O(g) △H2=-483.6kJ/mol则4NH3(g)+5O2(g)
 4NO(g)+6H2O(g) △H3=
4NO(g)+6H2O(g) △H3=(2)恒容密闭容器中进行合成知反应:N2(g)+3H2(g)
 2NH3(g) △H4==-92.4kJ/mol,其化学平衡常数(K)与温度的关系如下表:
2NH3(g) △H4==-92.4kJ/mol,其化学平衡常数(K)与温度的关系如下表:| 温度/K | 298 | 398 | 498 | … |
| 平衡常数(K) | 4.1×106 | K1 | K2 | … |
K1
(3)向氨合成塔中充入10molN2和40molH2合成氨,一定温度(T)下平衡混合物中氨气的体积分数与压强(p)的关系如图1所示。

①下列说法正确的是
A.由图1可知增大体系压强(p)有利于增大氨气在混合气体中的体积分数
B.若图1中T=500℃,则温度为450℃时对应的曲线是b
C.工业上采用500℃温度的主要目的是提高氮气的转化率
D.当3v正(H2)=2v逆(NH3)时,反应达到平衡状态
②当温度为T、氨气的体积分数为25%时,N2的转化率为
(4)工业上用NH3生产硝酸时,将NH3和O2按体积比1:2混合通入某特定条件的密闭容器中进行反应,所有物质不与外界交换,最后得到溶液中溶质的质量分数为
(5)氮碳比[
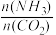 ]对合成尿素的反应:2NH3(g)+CO2(g)
]对合成尿素的反应:2NH3(g)+CO2(g) CO(NH2)2(g)+H2O(g)有影响。T℃时,在2L的恒容密闭容器中,将物质的量之和为3mol的NH3和CO2以不同的氨碳比进行反应,结果如图2所示,a、b分别表示CO2成NH3的转化率,c表示平衡体系中尿素的体积分数,当
CO(NH2)2(g)+H2O(g)有影响。T℃时,在2L的恒容密闭容器中,将物质的量之和为3mol的NH3和CO2以不同的氨碳比进行反应,结果如图2所示,a、b分别表示CO2成NH3的转化率,c表示平衡体系中尿素的体积分数,当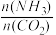 =
=
您最近一年使用:0次
7 . 【化学——选修2:化学与技术】联合生产是实现节能减排的重要措施,工业上合成氨和硝酸的联合生产具有重要意义。下面是工业上合成氨的简易流程:
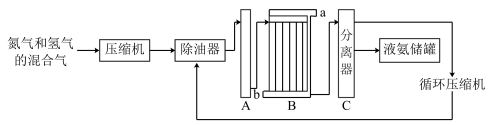
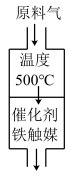
(1)设备A内部结构如右下图所示,其名称是________ ,其中发生的化学反应方程式为_________ ;生产中原料气必须进行脱硫,目的是____________ 。选择500℃进行反应的主要原因是___________ ;
(2)设备B的名称是冷凝塔,图中a和b是两个通水口,其中入水口是___ (填“a”或“b”)。
(3)氮气和氢气的混合气体通过压缩机压缩的原因是________________________________ 。
(4)生产出来的NH3可以用来生产硝酸。其中在氨气催化氧化过程中,不同温度下生成产物可能有所不同,温度对氨氧化产物产率的影响如下图所示;当温度大于900℃时,NO的产率下降的主要原因是__________________ 。

(5)某化肥厂用NH3制备NH4NO3。已知:由NH3制NO的产率是94%,NO制HNO3的产率是89%,则制HNO3所用NH3的质量占总耗NH3质量(不考虑其它损耗)的____ %(保留两位有效数字)。


(1)设备A内部结构如右下图所示,其名称是
(2)设备B的名称是冷凝塔,图中a和b是两个通水口,其中入水口是
(3)氮气和氢气的混合气体通过压缩机压缩的原因是
(4)生产出来的NH3可以用来生产硝酸。其中在氨气催化氧化过程中,不同温度下生成产物可能有所不同,温度对氨氧化产物产率的影响如下图所示;当温度大于900℃时,NO的产率下降的主要原因是

(5)某化肥厂用NH3制备NH4NO3。已知:由NH3制NO的产率是94%,NO制HNO3的产率是89%,则制HNO3所用NH3的质量占总耗NH3质量(不考虑其它损耗)的
您最近一年使用:0次



