名校
解题方法
1 . 下列有关合成氨条件选择的说法正确的是
| A.适当增加氢气的浓度可提高氮气的平衡转化率 | B.温度越高,速率越快,生产效益越好 |
| C.使用铁触媒能提高合成氨反应的平衡转化率 | D.将氨及时液化分离不利于提高氨的产率 |
您最近一年使用:0次
2023-12-03更新
|
127次组卷
|
3卷引用:新疆乌鲁木齐市六校联考2023-2024学年高二上学期期末考试化学试题
解题方法
2 . 对于反应2SO2(g)+O2(g)  2SO3(g);ΔH=-196.6 kJ·mol−1,下列说法正确的是
2SO3(g);ΔH=-196.6 kJ·mol−1,下列说法正确的是
 2SO3(g);ΔH=-196.6 kJ·mol−1,下列说法正确的是
2SO3(g);ΔH=-196.6 kJ·mol−1,下列说法正确的是| A.反应物的总键能大于生成物的总键能 |
B.反应的平衡常数可表示为K=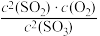 |
| C.从平衡体系中分离出SO3,正反应速率变快 |
| D.工业生产采用常压操作,可能是因为常压下SO2的转化率已经很高了 |
您最近一年使用:0次
2023-11-11更新
|
158次组卷
|
2卷引用:新疆乌鲁木齐第六十一中学2023-2024学年高二上学期期中考试化学试题
名校
3 . 下列有关工业合成氮反应:
 的说法
的说法不正确 的是

 的说法
的说法| A.合成氨采取循环操作目的是提高氮气和氢气的利用率 |
B.除原料气中CO反应: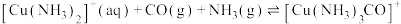  ,适宜低温高压环境 ,适宜低温高压环境 |
| C.合成塔压强调控在10MPa~30MPa之间,是对生产设备条件和经济成本的综合考虑结果 |
| D.合成塔使用热交换控制体系温度400~500℃左右,主要目的是有利于平衡正向移动 |
您最近一年使用:0次
2023-11-10更新
|
248次组卷
|
4卷引用:新疆生产建设兵团第三师图木舒克市第一中学2023-2024学年高二上学期第二次月考试化学试卷
新疆生产建设兵团第三师图木舒克市第一中学2023-2024学年高二上学期第二次月考试化学试卷浙江省钱塘联盟2023-2024学年高二上学期11月期中联考化学试题课时1化学反应的调控随堂练习(已下线)寒假作业04 化学反应的方向及调控-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)
名校
4 . 如下图所示为工业合成氨的流程图。下列说法不正确的是
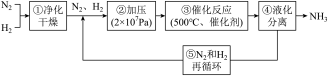

| A.步骤①中“净化”可以防止催化剂中毒 |
| B.步骤②中“加压”既可以提高原料的转化率,又可以加快反应速率 |
| C.步骤③、④、⑤均有利于提高原料平衡的转化率 |
| D.为提高反应物的转化率应及时将氨从混合气中分离出去 |
您最近一年使用:0次
2023-10-26更新
|
327次组卷
|
7卷引用:新疆兵团第三师图木舒克市鸿德实验学校2023-2024学年高二上学期期中考试化学试卷
5 . 铬和钒具有广泛用途。铬钒渣中铬和钒以低价态含氧酸盐形式存在,主要杂质为铁、铝、硅、磷等的化合物,从铬钒渣中分离提取铬和钒的一种流程如下图所示:

已知:最高价铬酸根在酸性介质中以Cr2O 存在,在碱性介质中以CrO
存在,在碱性介质中以CrO 存在。
存在。
回答下列问题:
(1)煅烧过程中,钒和铬被氧化为相应的最高价含氧酸盐,其中含铬化合物主要为___________ (填化学式)。
(2)水浸渣中主要有SiO2和___________ 。
(3)“沉淀”步骤调pH到弱碱性,主要除去的杂质是___________ 。
(4)“除硅磷”步骤中,使硅、磷分别以MgSiO3和MgNH4PO4的形式沉淀,该步需要控制溶液的pH≈9以达到最好的除杂效果,若pH<9时,会导致___________ ;pH>9时,会导致___________ 。
(5)“分离钒”步骤中,将溶液pH调到1.8左右得到V2O5沉淀,V2O5在pH<1时,溶解为VO 或VO3+在碱性条件下,溶解为VO
或VO3+在碱性条件下,溶解为VO 或VO
或VO ,上述性质说明V2O5具有
,上述性质说明V2O5具有___________ (填标号)。
A.酸性 B.碱性 C.两性
(6)“还原”步骤中加入焦亚硫酸钠(Na2S2O5)溶液,反应的离子方程式为___________ 。

已知:最高价铬酸根在酸性介质中以Cr2O
 存在,在碱性介质中以CrO
存在,在碱性介质中以CrO 存在。
存在。回答下列问题:
(1)煅烧过程中,钒和铬被氧化为相应的最高价含氧酸盐,其中含铬化合物主要为
(2)水浸渣中主要有SiO2和
(3)“沉淀”步骤调pH到弱碱性,主要除去的杂质是
(4)“除硅磷”步骤中,使硅、磷分别以MgSiO3和MgNH4PO4的形式沉淀,该步需要控制溶液的pH≈9以达到最好的除杂效果,若pH<9时,会导致
(5)“分离钒”步骤中,将溶液pH调到1.8左右得到V2O5沉淀,V2O5在pH<1时,溶解为VO
 或VO3+在碱性条件下,溶解为VO
或VO3+在碱性条件下,溶解为VO 或VO
或VO ,上述性质说明V2O5具有
,上述性质说明V2O5具有A.酸性 B.碱性 C.两性
(6)“还原”步骤中加入焦亚硫酸钠(Na2S2O5)溶液,反应的离子方程式为
您最近一年使用:0次
2023-06-10更新
|
18071次组卷
|
18卷引用:新疆维吾尔自治区阿克苏地区第二中学2023-2024学年高三上学期第二次月考化学试题
新疆维吾尔自治区阿克苏地区第二中学2023-2024学年高三上学期第二次月考化学试题2023年高考新课标理综化学真题(已下线)T26-工业流程题(已下线)2023年高考化学真题完全解读(新课标卷:适用安徽、云南、山西、吉林、黑龙江五省)(PPT+Word)(已下线)专题18 工艺流程题(已下线)2023年高考山东卷化学真题变式题(工业流程题)(已下线)专题18 工艺流程题(已下线)专题18 工艺流程题(已下线)第19练 化学工艺流程题 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)四川省绵阳市高中理科突击班2023-2024学年高三上学期第零次诊断性考试理综化学试题(已下线)专题13 工艺流程综合题-2023年高考化学真题题源解密(新高考专用)(已下线)专题13 工艺流程综合题-2023年高考化学真题题源解密(全国通用)四川省遂宁市第二中学校2023-2024学年高三上学期第一次诊断性考试理综试题(已下线)考点47 无机工艺流程(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)山东省滨州市2023-2024学年高三上学期11月期中考试化学试题(已下线)题型06 化工微流程-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)题型16 无机化工流程综合分析-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)题型三 工艺流程中的答题规范-备战2024年高考化学答题技巧与模板构建
名校
解题方法
6 . 如图所示为工业合成氨的流程图。下列说法错误的是
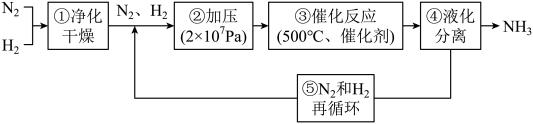

| A.步骤①中“净化”可以防止催化剂中毒 |
| B.步骤②中“加压”既可以提高原料的转化率,又可以加快反应速率 |
| C.步骤③、④、⑤均有利于提高原料平衡的转化率 |
| D.为保持足够高的反应速率,应在反应达到一定转化率时及时将氨从混合气中分离出去 |
您最近一年使用:0次
2022-12-07更新
|
253次组卷
|
4卷引用:新疆乌鲁木齐市第八中学2022-2023学年高二上学期期末考试化学试题
新疆乌鲁木齐市第八中学2022-2023学年高二上学期期末考试化学试题山东省临沂市第二中学2021-2022学年高二10月月考化学试题(已下线)专题06 化学反应的方向及调控【考题猜想】(6大题型)-2023-2024学年高二化学期中考点大串讲(人教版2019选择性必修1)广东省 广州市西关培英中学2023-2024学年高二上学期11月期中化学试题
名校
解题方法
7 . 合成氨问题,关乎到世界化工发展和粮食安全问题。下列合成氨工业的叙述中,不正确的是
| A.高压条件比常压条件更有利于合成氨的反应 |
| B.合成氨时采用循环操作,可以提高原料利用率 |
| C.工业生产采用500℃而不采用常温,是为了提高合成氨的转化率 |
| D.铁触媒的使用有利于提高合成氨的生产效率 |
您最近一年使用:0次
2022-11-13更新
|
217次组卷
|
3卷引用:新疆乌鲁木齐八一中学2023-2024学年高二上学期11月期中化学试题
8 . 下列有关合成氨工业的说法中正确的是
| A.铁触媒作催化剂可加快反应速率,且有利于化学平衡向合成氨的方向移动 |
| B.升高温度可以加快反应速率,且有利于化学平衡向合成氨的方向移动 |
| C.增大压强能缩短达到平衡状态所用的时间 |
| D.合成氨采用的压强是10~30MPa,因为该压强下铁触媒的活性最高 |
您最近一年使用:0次
2022-07-26更新
|
748次组卷
|
17卷引用:新疆昌吉州行知学校2022-2023学年高二上学期第一次线上月考化学试题
新疆昌吉州行知学校2022-2023学年高二上学期第一次线上月考化学试题吉林省长春外国语学校2021-2022学年高二上学期第一次月考化学试题湖南省益阳市箴言中学2021-2022学年高二上学期10月月考化学试题(已下线)必考点04 化学反应的方向和调控-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版2019选择性必修1)湖南省怀化市第五中学2021-2022学年高二上学期期中考试化学试题黑龙江省大兴安岭实验中学(西校区)2021-2022学年高二上学期第一次月考化学试题(已下线)第29练 化学反应的调控-2023年高考化学一轮复习小题多维练(全国通用)(已下线)第12讲 化学反应的调控-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)(已下线)2.4.1 合成氨生产适宜条件的选择-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)天津市第二十五中学2022 -2023学年高二上学期期中考试化学试题湖南省隆回县第二中学2022-2023学年高二上学期线上课程摸底(期中)考试化学试题黑龙江省哈尔滨市宾县第二中学2021-2022学年高二上学期第二次月考化学试题重庆市为明学校2022-2023学年高二上学期期末检测化学试题第四节 化学反应的调控河南省周口市太康县2022-2023学年高二上学期11月期中考试化学试题第二章 第四节 化学反应的调控(已下线)专题06 化学反应的方向及调控【考题猜想】(6大题型)-2023-2024学年高二化学期中考点大串讲(人教版2019选择性必修1)
名校
解题方法
9 . 乙烯是制造塑料、合成橡胶和合成纤维等化学产品的基本原料。C2H6裂解制C2H4是化学工业的一个重要研究课题,目前裂解方法有电催化、光催化裂解、直接裂解、氧气或二氧化碳氧化乙烷裂解等。乙烷直接裂解、乙烷二氧化碳氧化裂解和乙烷氧气氧化裂解的反应如下:
(Ⅰ)C2H6(g) C2H4(g)+H2(g) △H1=+125kJ·mol-1
C2H4(g)+H2(g) △H1=+125kJ·mol-1
(Ⅱ)CO2(g)+C2H6(g) C2H4(g)+CO(g)+H2O(g) △H2=+177kJ·mol-1
C2H4(g)+CO(g)+H2O(g) △H2=+177kJ·mol-1
(Ⅲ)2C2H6(g)+O2(g) 2C2H4(g)+2H2O(g) △H3=-211.6kJ·mol-1
2C2H4(g)+2H2O(g) △H3=-211.6kJ·mol-1
回答下列问题:
(1)已知键能:E(C—H)=416kJ·mol-1,E(H—H)=436kJ·mol-1,由此计算生成1mol碳碳π键放出的能量为_______ kJ。
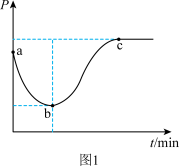
(2)在一绝热的恒容密闭容器中,通入一定量的C2H6发生反应(Ⅰ),反应过程中容器内压强(P)与时间(t)变化如图1所示,随着反应进行,a~b段压强减小的原因是_______ 。
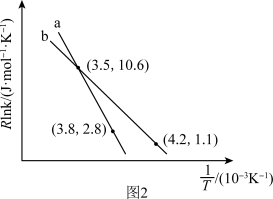
(3)反应(Ⅱ)的Arrhenius经验公式实验数据如图2中曲线a所示,已知Arrhenius经验公式Rlnk=- +C(Ea为活化能,k为速率常数,R和C为常数)。反应的活化能Ea=
+C(Ea为活化能,k为速率常数,R和C为常数)。反应的活化能Ea=_______ kJ·mol-1。当改变外界条件时,实验数据如图中曲线b所示,则实验可能改变的外界条件是_______ 。
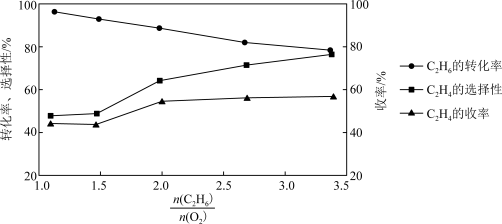
(4)乙烷氧气氧化裂解制乙烯,除发生反应(Ⅲ)之外,还发生副反应(Ⅳ):2C2H6(g)+7O2(g) 4CO2(g)+6H2O(g)。在800℃时用乙烷氧气氧化裂解制乙烯,乙烷的转化率、乙烯的选择性和收率随投料比
4CO2(g)+6H2O(g)。在800℃时用乙烷氧气氧化裂解制乙烯,乙烷的转化率、乙烯的选择性和收率随投料比 的变化关系如图所示:
的变化关系如图所示:
已知:C2H4的选择性=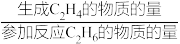 ×100%
×100%
C2H4的收率=C2H6的转化率×C2H4的选择性
①控制 =2而不采用选择性更高的
=2而不采用选择性更高的 =3.5,除可防止积碳外,另一原因是
=3.5,除可防止积碳外,另一原因是_______ ; <2时,
<2时, 越小,乙烷的转化率越大,乙烯的选择性和收率越小的原因是
越小,乙烷的转化率越大,乙烯的选择性和收率越小的原因是_______ 。
②一定温度和压强为5.8pMPa条件下,将C2H6和O2按物质的量之比为2∶3通入密闭弹性容器中发生反应,平衡时,C2H4选择性为60%,C2H4的收率为48%。该温度下,反应2C2H6(g)+O2(g) 2C2H4(g)+2H2O(g)的Kp=
2C2H4(g)+2H2O(g)的Kp=_______ (用含字母p的代数式表示,带单位。已知Kp是用反应体系中气体的分压来表示的平衡常数,分压=总压×物质的量分数)。
(Ⅰ)C2H6(g)
 C2H4(g)+H2(g) △H1=+125kJ·mol-1
C2H4(g)+H2(g) △H1=+125kJ·mol-1(Ⅱ)CO2(g)+C2H6(g)
 C2H4(g)+CO(g)+H2O(g) △H2=+177kJ·mol-1
C2H4(g)+CO(g)+H2O(g) △H2=+177kJ·mol-1(Ⅲ)2C2H6(g)+O2(g)
 2C2H4(g)+2H2O(g) △H3=-211.6kJ·mol-1
2C2H4(g)+2H2O(g) △H3=-211.6kJ·mol-1回答下列问题:
(1)已知键能:E(C—H)=416kJ·mol-1,E(H—H)=436kJ·mol-1,由此计算生成1mol碳碳π键放出的能量为
(2)在一绝热的恒容密闭容器中,通入一定量的C2H6发生反应(Ⅰ),反应过程中容器内压强(P)与时间(t)变化如图1所示,随着反应进行,a~b段压强减小的原因是

(3)反应(Ⅱ)的Arrhenius经验公式实验数据如图2中曲线a所示,已知Arrhenius经验公式Rlnk=-
 +C(Ea为活化能,k为速率常数,R和C为常数)。反应的活化能Ea=
+C(Ea为活化能,k为速率常数,R和C为常数)。反应的活化能Ea=
(4)乙烷氧气氧化裂解制乙烯,除发生反应(Ⅲ)之外,还发生副反应(Ⅳ):2C2H6(g)+7O2(g)
 4CO2(g)+6H2O(g)。在800℃时用乙烷氧气氧化裂解制乙烯,乙烷的转化率、乙烯的选择性和收率随投料比
4CO2(g)+6H2O(g)。在800℃时用乙烷氧气氧化裂解制乙烯,乙烷的转化率、乙烯的选择性和收率随投料比 的变化关系如图所示:
的变化关系如图所示:
已知:C2H4的选择性=
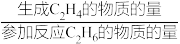 ×100%
×100%C2H4的收率=C2H6的转化率×C2H4的选择性
①控制
 =2而不采用选择性更高的
=2而不采用选择性更高的 =3.5,除可防止积碳外,另一原因是
=3.5,除可防止积碳外,另一原因是 <2时,
<2时, 越小,乙烷的转化率越大,乙烯的选择性和收率越小的原因是
越小,乙烷的转化率越大,乙烯的选择性和收率越小的原因是②一定温度和压强为5.8pMPa条件下,将C2H6和O2按物质的量之比为2∶3通入密闭弹性容器中发生反应,平衡时,C2H4选择性为60%,C2H4的收率为48%。该温度下,反应2C2H6(g)+O2(g)
 2C2H4(g)+2H2O(g)的Kp=
2C2H4(g)+2H2O(g)的Kp=
您最近一年使用:0次
2022-04-14更新
|
1384次组卷
|
3卷引用:新疆塔城地区第二中学2022-2023学年高二上学期11月月考化学试题
名校
解题方法
10 . 工业利用含镍废料(以镍铁钙合金为主)制取NiC2O4(草酸镍),再经过高温煅烧NiC2O4制取Ni2O3的流程如图1所示。
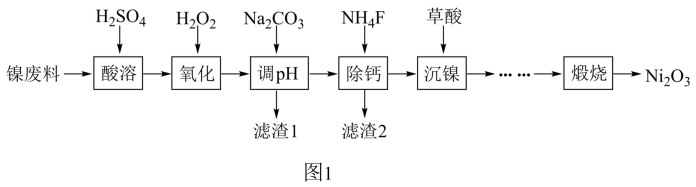
已知:NiC2O4、CaC2O4均难溶于水;Fe3+完全沉淀的pH约为3.2。
(1)“酸溶”时加快溶解速率的方法____ (写两种即可)。
(2)加入H2O2发生的主要反应的离子方程式为____ 。
(3)加入Na2CO3溶液调节pH至4.0~5.0,其目的为____ 。
(4)加入NH4F溶液可将Ca2+转化为CaF2沉淀除去,已知25℃时Ksp(CaF2)=1.6×10-10,要使溶液中Ca2+沉淀完全[c(Ca2+)≤1.0×10-5mol·L-1],则“除钙”时需控制NH4F的浓度至少为____ mol·L-1。
(5)隔绝空气高温煅烧NiC2O4可制得Ni2O3,NiC2O4受热分解的化学方程式为____ 。
(6)Ni2O3还可用于制备合成氨的催化剂ConNi1-nFe2O4。在其他条件相同时合成氨的相对初始速率随催化剂中n值变化的曲线如图2:
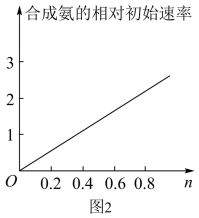
由图可知Co2+、Ni2+两种离子中催化效果更好的是____ 。

已知:NiC2O4、CaC2O4均难溶于水;Fe3+完全沉淀的pH约为3.2。
(1)“酸溶”时加快溶解速率的方法
(2)加入H2O2发生的主要反应的离子方程式为
(3)加入Na2CO3溶液调节pH至4.0~5.0,其目的为
(4)加入NH4F溶液可将Ca2+转化为CaF2沉淀除去,已知25℃时Ksp(CaF2)=1.6×10-10,要使溶液中Ca2+沉淀完全[c(Ca2+)≤1.0×10-5mol·L-1],则“除钙”时需控制NH4F的浓度至少为
(5)隔绝空气高温煅烧NiC2O4可制得Ni2O3,NiC2O4受热分解的化学方程式为
(6)Ni2O3还可用于制备合成氨的催化剂ConNi1-nFe2O4。在其他条件相同时合成氨的相对初始速率随催化剂中n值变化的曲线如图2:

由图可知Co2+、Ni2+两种离子中催化效果更好的是
您最近一年使用:0次
2022-03-16更新
|
66次组卷
|
4卷引用:新疆疏附县第二中学2021-2022学年高三上学期11月月考化学试题



