1 . 下列有关工业合成氨反应:
 的说法
的说法不正确 的是

 的说法
的说法| A.合成氨采取循环操作目的是提高氮气和氢气的利用率 |
B.除原料气中CO反应: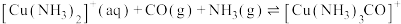  ,适宜低温高压环境 ,适宜低温高压环境 |
| C.合成塔压强调控在10MPa~30MPa之间,是对生产设备条件和经济成本的综合考虑结果 |
| D.合成塔使用热交换控制体系温度400~500℃左右,主要目的是有利于平衡正向移动 |
您最近一年使用:0次
2023-11-10更新
|
251次组卷
|
5卷引用:新疆生产建设兵团第三师图木舒克市第一中学2023-2024学年高二上学期第二次月考试化学试卷
新疆生产建设兵团第三师图木舒克市第一中学2023-2024学年高二上学期第二次月考试化学试卷浙江省钱塘联盟2023-2024学年高二上学期11月期中联考化学试题【定心卷】2.4 化学反应的调控随堂练习-人教版2023-2024学年选择性必修1(已下线)寒假作业04 化学反应的方向及调控-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)宁夏回族自治区石嘴山市平罗县平罗中学2023-2024学年高二下学期5月期中化学试题
2 . 铬和钒具有广泛用途。铬钒渣中铬和钒以低价态含氧酸盐形式存在,主要杂质为铁、铝、硅、磷等的化合物,从铬钒渣中分离提取铬和钒的一种流程如下图所示:

已知:最高价铬酸根在酸性介质中以Cr2O 存在,在碱性介质中以CrO
存在,在碱性介质中以CrO 存在。
存在。
回答下列问题:
(1)煅烧过程中,钒和铬被氧化为相应的最高价含氧酸盐,其中含铬化合物主要为___________ (填化学式)。
(2)水浸渣中主要有SiO2和___________ 。
(3)“沉淀”步骤调pH到弱碱性,主要除去的杂质是___________ 。
(4)“除硅磷”步骤中,使硅、磷分别以MgSiO3和MgNH4PO4的形式沉淀,该步需要控制溶液的pH≈9以达到最好的除杂效果,若pH<9时,会导致___________ ;pH>9时,会导致___________ 。
(5)“分离钒”步骤中,将溶液pH调到1.8左右得到V2O5沉淀,V2O5在pH<1时,溶解为VO 或VO3+在碱性条件下,溶解为VO
或VO3+在碱性条件下,溶解为VO 或VO
或VO ,上述性质说明V2O5具有
,上述性质说明V2O5具有___________ (填标号)。
A.酸性 B.碱性 C.两性
(6)“还原”步骤中加入焦亚硫酸钠(Na2S2O5)溶液,反应的离子方程式为___________ 。

已知:最高价铬酸根在酸性介质中以Cr2O
 存在,在碱性介质中以CrO
存在,在碱性介质中以CrO 存在。
存在。回答下列问题:
(1)煅烧过程中,钒和铬被氧化为相应的最高价含氧酸盐,其中含铬化合物主要为
(2)水浸渣中主要有SiO2和
(3)“沉淀”步骤调pH到弱碱性,主要除去的杂质是
(4)“除硅磷”步骤中,使硅、磷分别以MgSiO3和MgNH4PO4的形式沉淀,该步需要控制溶液的pH≈9以达到最好的除杂效果,若pH<9时,会导致
(5)“分离钒”步骤中,将溶液pH调到1.8左右得到V2O5沉淀,V2O5在pH<1时,溶解为VO
 或VO3+在碱性条件下,溶解为VO
或VO3+在碱性条件下,溶解为VO 或VO
或VO ,上述性质说明V2O5具有
,上述性质说明V2O5具有A.酸性 B.碱性 C.两性
(6)“还原”步骤中加入焦亚硫酸钠(Na2S2O5)溶液,反应的离子方程式为
您最近一年使用:0次
2023-06-10更新
|
18953次组卷
|
18卷引用:新疆维吾尔自治区阿克苏地区第二中学2023-2024学年高三上学期第二次月考化学试题
新疆维吾尔自治区阿克苏地区第二中学2023-2024学年高三上学期第二次月考化学试题2023年高考新课标理综化学真题(已下线)T26-工业流程题(已下线)2023年高考化学真题完全解读(新课标卷:适用安徽、云南、山西、吉林、黑龙江五省)(PPT+Word)(已下线)专题18 工艺流程题(已下线)2023年高考山东卷化学真题变式题(工业流程题)(已下线)专题18 工艺流程题(已下线)专题18 工艺流程题(已下线)第19练 化学工艺流程题 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)四川省绵阳市高中理科突击班2023-2024学年高三上学期第零次诊断性考试理综化学试题(已下线)专题13 工艺流程综合题-2023年高考化学真题题源解密(新高考专用)(已下线)专题13 工艺流程综合题-2023年高考化学真题题源解密(全国通用)四川省遂宁市第二中学校2023-2024学年高三上学期第一次诊断性考试理综试题(已下线)考点47 无机工艺流程(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)山东省滨州市2023-2024学年高三上学期11月期中考试化学试题(已下线)题型06 化工微流程-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)题型16 无机化工流程综合分析-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)题型三 工艺流程中的答题规范-备战2024年高考化学答题技巧与模板构建
名校
解题方法
3 . 乙烯是制造塑料、合成橡胶和合成纤维等化学产品的基本原料。C2H6裂解制C2H4是化学工业的一个重要研究课题,目前裂解方法有电催化、光催化裂解、直接裂解、氧气或二氧化碳氧化乙烷裂解等。乙烷直接裂解、乙烷二氧化碳氧化裂解和乙烷氧气氧化裂解的反应如下:
(Ⅰ)C2H6(g) C2H4(g)+H2(g) △H1=+125kJ·mol-1
C2H4(g)+H2(g) △H1=+125kJ·mol-1
(Ⅱ)CO2(g)+C2H6(g) C2H4(g)+CO(g)+H2O(g) △H2=+177kJ·mol-1
C2H4(g)+CO(g)+H2O(g) △H2=+177kJ·mol-1
(Ⅲ)2C2H6(g)+O2(g) 2C2H4(g)+2H2O(g) △H3=-211.6kJ·mol-1
2C2H4(g)+2H2O(g) △H3=-211.6kJ·mol-1
回答下列问题:
(1)已知键能:E(C—H)=416kJ·mol-1,E(H—H)=436kJ·mol-1,由此计算生成1mol碳碳π键放出的能量为_______ kJ。
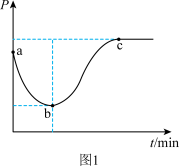
(2)在一绝热的恒容密闭容器中,通入一定量的C2H6发生反应(Ⅰ),反应过程中容器内压强(P)与时间(t)变化如图1所示,随着反应进行,a~b段压强减小的原因是_______ 。
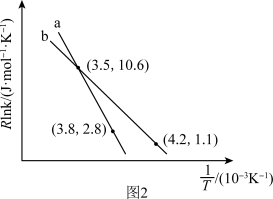
(3)反应(Ⅱ)的Arrhenius经验公式实验数据如图2中曲线a所示,已知Arrhenius经验公式Rlnk=- +C(Ea为活化能,k为速率常数,R和C为常数)。反应的活化能Ea=
+C(Ea为活化能,k为速率常数,R和C为常数)。反应的活化能Ea=_______ kJ·mol-1。当改变外界条件时,实验数据如图中曲线b所示,则实验可能改变的外界条件是_______ 。
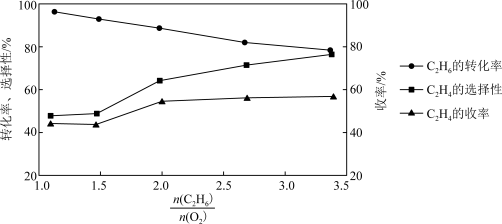
(4)乙烷氧气氧化裂解制乙烯,除发生反应(Ⅲ)之外,还发生副反应(Ⅳ):2C2H6(g)+7O2(g) 4CO2(g)+6H2O(g)。在800℃时用乙烷氧气氧化裂解制乙烯,乙烷的转化率、乙烯的选择性和收率随投料比
4CO2(g)+6H2O(g)。在800℃时用乙烷氧气氧化裂解制乙烯,乙烷的转化率、乙烯的选择性和收率随投料比 的变化关系如图所示:
的变化关系如图所示:
已知:C2H4的选择性=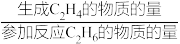 ×100%
×100%
C2H4的收率=C2H6的转化率×C2H4的选择性
①控制 =2而不采用选择性更高的
=2而不采用选择性更高的 =3.5,除可防止积碳外,另一原因是
=3.5,除可防止积碳外,另一原因是_______ ; <2时,
<2时, 越小,乙烷的转化率越大,乙烯的选择性和收率越小的原因是
越小,乙烷的转化率越大,乙烯的选择性和收率越小的原因是_______ 。
②一定温度和压强为5.8pMPa条件下,将C2H6和O2按物质的量之比为2∶3通入密闭弹性容器中发生反应,平衡时,C2H4选择性为60%,C2H4的收率为48%。该温度下,反应2C2H6(g)+O2(g) 2C2H4(g)+2H2O(g)的Kp=
2C2H4(g)+2H2O(g)的Kp=_______ (用含字母p的代数式表示,带单位。已知Kp是用反应体系中气体的分压来表示的平衡常数,分压=总压×物质的量分数)。
(Ⅰ)C2H6(g)
 C2H4(g)+H2(g) △H1=+125kJ·mol-1
C2H4(g)+H2(g) △H1=+125kJ·mol-1(Ⅱ)CO2(g)+C2H6(g)
 C2H4(g)+CO(g)+H2O(g) △H2=+177kJ·mol-1
C2H4(g)+CO(g)+H2O(g) △H2=+177kJ·mol-1(Ⅲ)2C2H6(g)+O2(g)
 2C2H4(g)+2H2O(g) △H3=-211.6kJ·mol-1
2C2H4(g)+2H2O(g) △H3=-211.6kJ·mol-1回答下列问题:
(1)已知键能:E(C—H)=416kJ·mol-1,E(H—H)=436kJ·mol-1,由此计算生成1mol碳碳π键放出的能量为
(2)在一绝热的恒容密闭容器中,通入一定量的C2H6发生反应(Ⅰ),反应过程中容器内压强(P)与时间(t)变化如图1所示,随着反应进行,a~b段压强减小的原因是

(3)反应(Ⅱ)的Arrhenius经验公式实验数据如图2中曲线a所示,已知Arrhenius经验公式Rlnk=-
 +C(Ea为活化能,k为速率常数,R和C为常数)。反应的活化能Ea=
+C(Ea为活化能,k为速率常数,R和C为常数)。反应的活化能Ea=
(4)乙烷氧气氧化裂解制乙烯,除发生反应(Ⅲ)之外,还发生副反应(Ⅳ):2C2H6(g)+7O2(g)
 4CO2(g)+6H2O(g)。在800℃时用乙烷氧气氧化裂解制乙烯,乙烷的转化率、乙烯的选择性和收率随投料比
4CO2(g)+6H2O(g)。在800℃时用乙烷氧气氧化裂解制乙烯,乙烷的转化率、乙烯的选择性和收率随投料比 的变化关系如图所示:
的变化关系如图所示:
已知:C2H4的选择性=
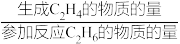 ×100%
×100%C2H4的收率=C2H6的转化率×C2H4的选择性
①控制
 =2而不采用选择性更高的
=2而不采用选择性更高的 =3.5,除可防止积碳外,另一原因是
=3.5,除可防止积碳外,另一原因是 <2时,
<2时, 越小,乙烷的转化率越大,乙烯的选择性和收率越小的原因是
越小,乙烷的转化率越大,乙烯的选择性和收率越小的原因是②一定温度和压强为5.8pMPa条件下,将C2H6和O2按物质的量之比为2∶3通入密闭弹性容器中发生反应,平衡时,C2H4选择性为60%,C2H4的收率为48%。该温度下,反应2C2H6(g)+O2(g)
 2C2H4(g)+2H2O(g)的Kp=
2C2H4(g)+2H2O(g)的Kp=
您最近一年使用:0次
2022-04-14更新
|
1385次组卷
|
3卷引用:新疆塔城地区第二中学2022-2023学年高二上学期11月月考化学试题
4 . 工业上利用铁的氧化物在高温条件下循环裂解水制氢气的流程如图所示。

(1)反应I的化学方程式为:Fe3O4(s)+CO(g) 3FeO(s)+CO2(g),反应Ⅱ的化学方程式为
3FeO(s)+CO2(g),反应Ⅱ的化学方程式为_______ ,对比反应I、Ⅱ,铁的氧化物在循环裂解水制氢气过程中的作用是_______ 。
(2)反应III为:CO2(g)+C(s)⇌2CO(g) ∆H>0。为了提高达平衡后CO的产量,理论上可以采取的合理措施有_______ (任写一条措施)。
(3)流程图中碳的氧化物可用来制备碳酰肼[CO(NHNH2)2,其中碳元素为+4价]。加热条件下,碳酰肼能将锅炉内表面锈蚀后的氧化铁转化为结构紧密的四氧化三铁保护层,并生成氮气、水和二氧化碳。该反应的化学方程式为_______ 。
(4)①高铁酸盐是常用的水处理剂。高铁酸钠(Na2FeO4)可用如下反应制备:
2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑
若生成2mol Na2FeO4,则反应中电子转移的物质的量为_______ mol。
②高铁酸盐可将水体中的Mn2+氧化为MnO2进行除去,若氧化含Mn2+ 1mg的水体样本,需要1.2mg·L-1高铁酸钾_______ L。

(1)反应I的化学方程式为:Fe3O4(s)+CO(g)
 3FeO(s)+CO2(g),反应Ⅱ的化学方程式为
3FeO(s)+CO2(g),反应Ⅱ的化学方程式为(2)反应III为:CO2(g)+C(s)⇌2CO(g) ∆H>0。为了提高达平衡后CO的产量,理论上可以采取的合理措施有
(3)流程图中碳的氧化物可用来制备碳酰肼[CO(NHNH2)2,其中碳元素为+4价]。加热条件下,碳酰肼能将锅炉内表面锈蚀后的氧化铁转化为结构紧密的四氧化三铁保护层,并生成氮气、水和二氧化碳。该反应的化学方程式为
(4)①高铁酸盐是常用的水处理剂。高铁酸钠(Na2FeO4)可用如下反应制备:
2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑
若生成2mol Na2FeO4,则反应中电子转移的物质的量为
②高铁酸盐可将水体中的Mn2+氧化为MnO2进行除去,若氧化含Mn2+ 1mg的水体样本,需要1.2mg·L-1高铁酸钾
您最近一年使用:0次
名校
解题方法
5 . 以天然气(CH4)为原料合成甲醇(CH3OH)。有关热化学方程式如下:
①2CH4(g)+O2(g)= 2CO(g)+4H2(g) ΔH1=-70.8 kJ·mol-1
②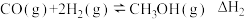
③
(1)ΔH2=________ kJ·mol-1。 反应①自发进行的条件是_________ (填序号)。
a 高温 b 低温 c 任何环境都自发 d 任何环境都不自发
(2)若在一定温度下的恒压容器中只投入1 mol CO和1 mol H2只发生反应②,下列量不再变化时可以判断反应达到平衡的是_________ 。
a 压强 b 密度 c 混合气的平均摩尔质量 d CO的体积分数
(3)在体积可变的密闭容器中投入1 mol CO和2 mol H2,在不同条件下发生反应: 。实验测得平衡时CH3OH的物质的量随温度、压强的变化如图1所示。
。实验测得平衡时CH3OH的物质的量随温度、压强的变化如图1所示。
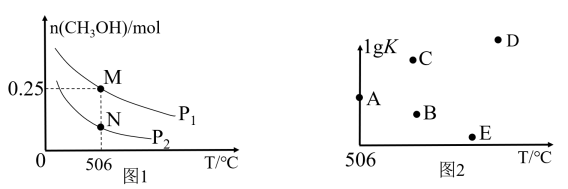
①M点时,H2的转化率为__________ ;压强:p1_______ p2 (填“>”、“<”或“=”)。
②反应速率:N点ʋ正 (CO)________ M点ʋ逆 (CO)(填“>”、“<”或“=”)。
③温度为506 ℃时,若压强为p1、在密闭容器中进行上述反应(起始投料不变),平衡时容器体积为1L,则平衡常数K=__________ (用分数表示)。在不同温度下上述反应的平衡常数的对数(lg K)如图2所示,则B、C、D、E四点中能正确表示该反应的lg K与T的关系的点为_______ (填字母)。
④在2 L恒容密闭容器中充入a(a>0) mol H2、2 mol CO和6 mol CH3OH(g),在506 ℃下进行上述反应。为了使该反应逆向进行,a的范围为____________ 。
①2CH4(g)+O2(g)= 2CO(g)+4H2(g) ΔH1=-70.8 kJ·mol-1
②
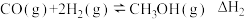
③

(1)ΔH2=
a 高温 b 低温 c 任何环境都自发 d 任何环境都不自发
(2)若在一定温度下的恒压容器中只投入1 mol CO和1 mol H2只发生反应②,下列量不再变化时可以判断反应达到平衡的是
a 压强 b 密度 c 混合气的平均摩尔质量 d CO的体积分数
(3)在体积可变的密闭容器中投入1 mol CO和2 mol H2,在不同条件下发生反应:
 。实验测得平衡时CH3OH的物质的量随温度、压强的变化如图1所示。
。实验测得平衡时CH3OH的物质的量随温度、压强的变化如图1所示。
①M点时,H2的转化率为
②反应速率:N点ʋ正 (CO)
③温度为506 ℃时,若压强为p1、在密闭容器中进行上述反应(起始投料不变),平衡时容器体积为1L,则平衡常数K=
④在2 L恒容密闭容器中充入a(a>0) mol H2、2 mol CO和6 mol CH3OH(g),在506 ℃下进行上述反应。为了使该反应逆向进行,a的范围为
您最近一年使用:0次
2020-12-01更新
|
156次组卷
|
2卷引用:新疆昌吉州教育共同体2020-2021学年高二上学期期中考试化学试题
解题方法
6 . 某空间站中宇航员的呼吸保障系统原理如图所示。

Sabatier系统中发生反应为:
反应I:CO2(g)+4H2(g) CH4(g)+2H2O(g)△H1
CH4(g)+2H2O(g)△H1
反应II:CO2(g)+H2(g) CO(g)+H2O(g)△H2=+41.2kJ/mol
CO(g)+H2O(g)△H2=+41.2kJ/mol
(1)常温常压下,已知:
①H2和CH4的燃烧热(△H)分别为-285.5kJ·mol-1和-890.0kJ·mol-1;
②H2O(l)=H2O(g)△H3=+44.0kJ·mol-1。则△H1=__________ kJ·mol-1。
(2)按 =4的混合气体充入Sabatier系统,当气体总压强为0.1MPa,平衡时各物质的物质的量分数如图所示;不同压强时,CO2的平衡转化率如图所示:
=4的混合气体充入Sabatier系统,当气体总压强为0.1MPa,平衡时各物质的物质的量分数如图所示;不同压强时,CO2的平衡转化率如图所示:

①Sabatier系统中应选择适宜的温度是__________ 。
②200~550℃时,CO2的物质的量分数随温度升高而增大的原因是__________ 。
③当温度一定时,随压强升高,CO2的平衡转化率增大,其原因是__________ 。
(3)一种新的循环利用方案是用Bosch反应[CO2(g)+2H2(g) C(s)+2H2O(g)]代替Sabatier系统。
C(s)+2H2O(g)]代替Sabatier系统。
①分析Bosch反应的熵值变化为:△S__________ 0(选填“>”或“<”)。
②温度一定时,在2L密闭容器中按 =2投料进行Bosch反应,达到平衡时体系的压强为原来压强p0的0.7倍,该温度下反应平衡常数Kp为
=2投料进行Bosch反应,达到平衡时体系的压强为原来压强p0的0.7倍,该温度下反应平衡常数Kp为__________ (用含p0的表达式表示,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
③下列措施能提高Bosch反应中CO2转化率的是_________ (填标号)。
A.加快反应器中气体的流速B.提高原料气中CO2所占比例
C.增大催化剂的表面积D.反应器前段加热,后段冷却

Sabatier系统中发生反应为:
反应I:CO2(g)+4H2(g)
 CH4(g)+2H2O(g)△H1
CH4(g)+2H2O(g)△H1反应II:CO2(g)+H2(g)
 CO(g)+H2O(g)△H2=+41.2kJ/mol
CO(g)+H2O(g)△H2=+41.2kJ/mol(1)常温常压下,已知:
①H2和CH4的燃烧热(△H)分别为-285.5kJ·mol-1和-890.0kJ·mol-1;
②H2O(l)=H2O(g)△H3=+44.0kJ·mol-1。则△H1=
(2)按
 =4的混合气体充入Sabatier系统,当气体总压强为0.1MPa,平衡时各物质的物质的量分数如图所示;不同压强时,CO2的平衡转化率如图所示:
=4的混合气体充入Sabatier系统,当气体总压强为0.1MPa,平衡时各物质的物质的量分数如图所示;不同压强时,CO2的平衡转化率如图所示:
①Sabatier系统中应选择适宜的温度是
②200~550℃时,CO2的物质的量分数随温度升高而增大的原因是
③当温度一定时,随压强升高,CO2的平衡转化率增大,其原因是
(3)一种新的循环利用方案是用Bosch反应[CO2(g)+2H2(g)
 C(s)+2H2O(g)]代替Sabatier系统。
C(s)+2H2O(g)]代替Sabatier系统。①分析Bosch反应的熵值变化为:△S
②温度一定时,在2L密闭容器中按
 =2投料进行Bosch反应,达到平衡时体系的压强为原来压强p0的0.7倍,该温度下反应平衡常数Kp为
=2投料进行Bosch反应,达到平衡时体系的压强为原来压强p0的0.7倍,该温度下反应平衡常数Kp为③下列措施能提高Bosch反应中CO2转化率的是
A.加快反应器中气体的流速B.提高原料气中CO2所占比例
C.增大催化剂的表面积D.反应器前段加热,后段冷却
您最近一年使用:0次
2020-07-07更新
|
158次组卷
|
3卷引用:新疆维吾尔自治区巴州二中2021届高三第六次月考化学试题
新疆维吾尔自治区巴州二中2021届高三第六次月考化学试题湖南省衡阳市2020届高三下学期第二次联考(二模)理综化学试题(已下线)第六单元 化学反应速率和化学平衡测试题-2021年高考化学一轮复习名师精讲练【学科网名师堂】



