对于反应2SO2(g)+O2(g)  2SO3(g);ΔH=-196.6 kJ·mol−1,下列说法正确的是
2SO3(g);ΔH=-196.6 kJ·mol−1,下列说法正确的是
 2SO3(g);ΔH=-196.6 kJ·mol−1,下列说法正确的是
2SO3(g);ΔH=-196.6 kJ·mol−1,下列说法正确的是| A.反应物的总键能大于生成物的总键能 |
B.反应的平衡常数可表示为K=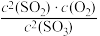 |
| C.从平衡体系中分离出SO3,正反应速率变快 |
| D.工业生产采用常压操作,可能是因为常压下SO2的转化率已经很高了 |
更新时间:2023/11/11 22:35:22
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】已知:①1molH2分子中化学键断裂时需吸收436kJ的能量;②1molCl2分子中化学键断裂时需吸收243kJ的能量;③由氢原子和氯原子形成1molHCl分子时释放431kJ的能量。则1molH2和1molCl2完全反应生成氯化氢气体时的能量变化为
| A.放出能量183kJ | B.吸收能量183kJ |
| C.放出能量248kJ | D.吸收能量862kJ |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】已知H2(g)+Br2(l)=2HBr(g) ΔH=-72kJ·mol−1.蒸发1molBr2(l)需要吸收的能量为30kJ,其它相关数据如表所示,
下列说法正确的是
| 共价键 | H-H | H-Br |
| 键能/(kJ·mol−1) | 436 | 369 |
| A.Br2(l)=Br2(g) ΔH=-30kJ·mol−1 |
| B.2Br(g)=Br2(g) ΔH=230kJ·mol−1 |
| C.2HBr(g)=H2(g)+Br2(g) ΔH=102kJ·mol−1 |
| D.H2(g)+Br2(l)=2HBr(g) ΔH=-72kJ·mol−1表示一个氢气分子和一个液溴分子完全反应放出72kJ热量 |
您最近一年使用:0次
【推荐1】已知合成氨反应可逆且为放热反应,在一定温度和压强下,以下推论不正确的是
A.  、 、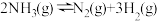  ,则 ,则 |
B.  、 、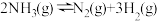  ,则 ,则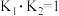 |
C.  、 、  ,则 ,则 |
D.  、 、  ,则 ,则 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】可逆反应 ,某温度下的平衡常数为
,某温度下的平衡常数为 (
(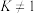 ),反应热为
),反应热为 。保持温度不变,将方程式的书写作如下改变,则
。保持温度不变,将方程式的书写作如下改变,则 和K的相应变化为
和K的相应变化为
 ,某温度下的平衡常数为
,某温度下的平衡常数为 (
(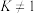 ),反应热为
),反应热为 。保持温度不变,将方程式的书写作如下改变,则
。保持温度不变,将方程式的书写作如下改变,则 和K的相应变化为
和K的相应变化为A.写成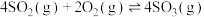 , , 、K均扩大了一倍 、K均扩大了一倍 |
B.写成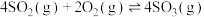 , , 扩大了一倍,K保持不变 扩大了一倍,K保持不变 |
C.写成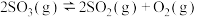 , , 、K变为原来的相反数 、K变为原来的相反数 |
D.写成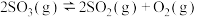 , , 变为原来的相反数,K变为原来的倒数 变为原来的相反数,K变为原来的倒数 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】德国哈伯发明以低成本制造大量氨的方法,流程图中为提高原料转化率而采取措施是


| A.①②③ | B.②④⑤ | C.①③⑤ | D.②③④ |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列有关说法正确的是
| A.合成氨生产中,为提高氢气的转化率,可增加氮气的量 |
| B.二氧化硫的催化氧化反应,△H<0,故反应温度越低越好 |
| C.△H>0、△S<0的反应在任何条件下都能发生反应 |
| D.使用催化剂可以提高工业生产中合成氨的产率 |
您最近一年使用:0次

 CO2(g)+4H2(g) 已知,破坏1mol化学键需要吸收的热量如下表所示:
CO2(g)+4H2(g) 已知,破坏1mol化学键需要吸收的热量如下表所示: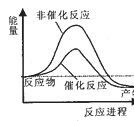

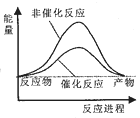


 。如图是乙烯的转化率随温度、压强的变化关系,下列说法正确的是
。如图是乙烯的转化率随温度、压强的变化关系,下列说法正确的是


