1 . 已知合成氨反应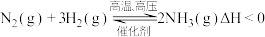 ,既要使合成氨的产率增大,又要使反应速率加快,可采取的方法是
,既要使合成氨的产率增大,又要使反应速率加快,可采取的方法是
①减压;②加压;③升温;④降温;⑤及时从平衡混合气中分离出 ;⑥补充
;⑥补充 或
或 ⑦加催化剂;
⑦加催化剂;
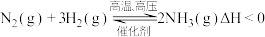 ,既要使合成氨的产率增大,又要使反应速率加快,可采取的方法是
,既要使合成氨的产率增大,又要使反应速率加快,可采取的方法是①减压;②加压;③升温;④降温;⑤及时从平衡混合气中分离出
 ;⑥补充
;⑥补充 或
或 ⑦加催化剂;
⑦加催化剂;| A.③④⑤⑦ | B.②④⑥ | C.仅②⑥ | D.②③⑥⑦ |
您最近一年使用:0次
名校
2 . 下列关于工业合成氨的叙述错误的是
| A.合成氨没有选择更大的压强是因为压强过大会增加生产投资,降低综合经济效益 |
| B.使用铁触媒能降低反应的活化能,使反应物在较低温度时能较快地发生反应 |
C.工业合成氨温度为 是因为升高温度有利于提高反应物的平衡转化率 是因为升高温度有利于提高反应物的平衡转化率 |
| D.及时从反应体系中分离出氨气有利于平衡向正反应方向移动 |
您最近一年使用:0次
名校
3 . 某温度下发生反应:3H2(g)+N2(g)⇌2NH3(g) ΔH=-92.4kJ/mol,N2的转化率(α)与体系总压强(p)的关系如图所示,下列说法中正确的是
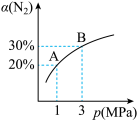

| A.将1molN2、3molH2置于1L密闭容器中发生反应,放出的热量为92.4kJ |
| B.平衡状态由A变到B时,平衡常数KA<KB |
| C.上述反应在达到平衡后,增大压强,H2的转化率增大 |
| D.合成氨工业中常采用400~500℃的高温以提高原料的转化率 |
您最近一年使用:0次
名校
解题方法
4 . 下列有关合成氨条件选择的说法正确的是
| A.适当增加氢气的浓度可提高氮气的平衡转化率 | B.温度越高,速率越快,生产效益越好 |
| C.使用铁触媒能提高合成氨反应的平衡转化率 | D.将氨及时液化分离不利于提高氨的产率 |
您最近一年使用:0次
2023-12-03更新
|
127次组卷
|
3卷引用:天津市第十四中学2023-2024学年高二上学期第二次月考化学试卷
名校
5 . 纯 遇热易发生分解,工业上通常制成
遇热易发生分解,工业上通常制成 固体以便运输和储存。制备
固体以便运输和储存。制备 的实验装置如图所示(夹持装置省略),其中A装置制备
的实验装置如图所示(夹持装置省略),其中A装置制备 ,C装置用于制备
,C装置用于制备 。回答下列问题:
。回答下列问题:
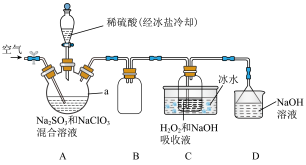
(1)仪器a的名称是___________ 。装置B的作用是___________ 。
(2)装置A中发生反应的离子方程式为___________ 。向装置A中通入空气的目的是___________ 。
(3)装置C中发生反应的化学方程式为___________ ;C装置采用“冰水浴”的目的是___________ 。
(4)研究测得C装置吸收液中的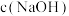 与
与 对粗产品中
对粗产品中 含量的影响如图所示。则最佳条件为
含量的影响如图所示。则最佳条件为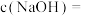
___________  ,
,
___________ 。

 遇热易发生分解,工业上通常制成
遇热易发生分解,工业上通常制成 固体以便运输和储存。制备
固体以便运输和储存。制备 的实验装置如图所示(夹持装置省略),其中A装置制备
的实验装置如图所示(夹持装置省略),其中A装置制备 ,C装置用于制备
,C装置用于制备 。回答下列问题:
。回答下列问题:
(1)仪器a的名称是
(2)装置A中发生反应的离子方程式为
(3)装置C中发生反应的化学方程式为
(4)研究测得C装置吸收液中的
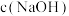 与
与 对粗产品中
对粗产品中 含量的影响如图所示。则最佳条件为
含量的影响如图所示。则最佳条件为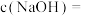
 ,
,

您最近一年使用:0次
解题方法
6 . 合成氨工业中采用了物质循环操作,主要的目的是
| A.降低氨的沸点 | B.增大化学反应速率 |
| C.提高N2和H2的利用率 | D.提高平衡混合物中氨的含量 |
您最近一年使用:0次
2023-11-08更新
|
162次组卷
|
2卷引用:天津市河西区2023-2024学年高二上学期11月期中化学试题
名校
7 . 下列有关合成氨工业的叙述,可用勒夏特列原理来解释的是
A.使用铁触媒,使 和 和 混合气体有利于合成氨 混合气体有利于合成氨 |
| B.高压比常压条件更有利于合成氨的反应 |
| C.500℃左右比室温更有利于合成氨的反应 |
| D.合成氨时,原料气必须经过净化 |
您最近一年使用:0次
2023-10-25更新
|
41次组卷
|
2卷引用:天津市武清区城关中学2023-2024学年高三上学期第二次阶段性练习化学试题
名校
解题方法
8 . 科学家一直致力于“人工固氮”的方法研究。目前合成氨的技术原理为:N2(g)+3H2(g)  2NH3(g) ΔH=−92.4kJ/mol。该反应的能量变化如图所示。
2NH3(g) ΔH=−92.4kJ/mol。该反应的能量变化如图所示。

(1)在实际工业生产中,通常采用铁触媒、在___________ ℃温度和___________ MPa的条件下合成氨。
(2)在反应体系中加入催化剂,反应速率增大,E2的变化是___________ 。(填“增大”、“减小”或“不变”)。
(3)将一定量的N2(g)和H2(g)放入2L的密闭容器中,在500°C、2×107Pa下发生反应,5分钟后达到平衡,测得N2为0.2mol, H2为0.6mol, NH3为0.2mol。氮气的平均反应速率 v(N2)=__________ ,H2的转化率为___________ (保留小数点后一位,下同),该反应在此温度下的化学平衡常数为___________ 。
(4)欲提高 (3) 容器中H2的转化率,下列措施可行的是___________。
(5)若在0.5L的密闭容器中,一定量的氮气和氢气进行反应,其化学平衡常数K与温度T的关系如表所示,请完成下列问题:
①试比较K1、K2的大小, K1___________ K2(填“>”、“<”或“=”);
②400°C时, 反应2NH3(g) N2(g)+3H2(g) 的化学平衡常数为
N2(g)+3H2(g) 的化学平衡常数为 ___________ 。当测得NH3、N2和H2物质的量分别为3mol、2mol和2mol时,则该反应的v(N2)正___________ v(N2)逆(填“>”、“<”或“=”)。
 2NH3(g) ΔH=−92.4kJ/mol。该反应的能量变化如图所示。
2NH3(g) ΔH=−92.4kJ/mol。该反应的能量变化如图所示。
(1)在实际工业生产中,通常采用铁触媒、在
(2)在反应体系中加入催化剂,反应速率增大,E2的变化是
(3)将一定量的N2(g)和H2(g)放入2L的密闭容器中,在500°C、2×107Pa下发生反应,5分钟后达到平衡,测得N2为0.2mol, H2为0.6mol, NH3为0.2mol。氮气的平均反应速率 v(N2)=
(4)欲提高 (3) 容器中H2的转化率,下列措施可行的是___________。
| A.向容器中按原比例再充入原料气 | B.向容器中再充入惰性气体 |
| C.改变反应的催化剂 | D.液化生成物分离出氨 |
| T/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
②400°C时, 反应2NH3(g)
 N2(g)+3H2(g) 的化学平衡常数为
N2(g)+3H2(g) 的化学平衡常数为
您最近一年使用:0次
9 . 下列叙述中,不能用平衡移动原理解释的是
| A.红棕色的NO2,加压后颜色先变深后变浅 | B.高压比常压有利于合成SO3的反应 |
| C.加入催化剂有利于氨的合成 | D.光照后氯水颜色变浅 |
您最近一年使用:0次
名校
解题方法
10 . 工业上制备硫酸的一步重要反应是 在400~500℃下的催化氧化反应:
在400~500℃下的催化氧化反应:
 。下列有关说法错误的是
。下列有关说法错误的是
 在400~500℃下的催化氧化反应:
在400~500℃下的催化氧化反应:
 。下列有关说法错误的是
。下列有关说法错误的是A.常通入过量的空气,以提高 的平衡转化率 的平衡转化率 |
| B.为提高反应速率和平衡转化率,采用的压强越大越好 |
| C.控制温度为400~500℃既能提升反应速率,又能使催化剂有较高的活性 |
| D.要综合考虑影响速率与平衡的各种因素、设备条件和经济成本等,寻找适宜的生产条件 |
您最近一年使用:0次
2023-08-12更新
|
405次组卷
|
8卷引用:天津市天津中学2023-2024学年高二上学期第一次月考化学试题
天津市天津中学2023-2024学年高二上学期第一次月考化学试题河南省周口市无锡天一企业管理有限公司等2校2022-2023学年高二上学期12月期末考试化学试题山东省鄄城县第一中学2023-2024学年高二上学期9月月考化学试题黑龙江省哈尔滨市第一中学校2023-2024学年高二上学期第一次质量检测化学试题(已下线)专题05 化学反应的方向 化学反应的调控 -【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(人教版2019)(已下线)寒假作业04 化学反应的方向及调控-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)四川省宜宾市叙州区第二中学校2023-2024学年高二上学期12月月考化学试题安徽省六安市裕安区新安中学2023-2024学年高二下学期第一次月考化学试题



