解题方法
1 . 下表的实验数据是在不同温度和压强下,平衡混合物中NH3含量的变化情况。
达到平衡时平衡混合物中NH3的含量(体积分数)[投料V(N2)∶V(H2)=1∶3]。
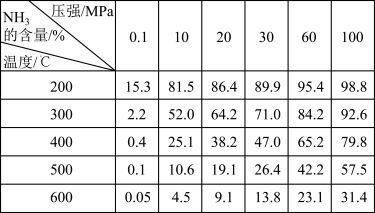
(1)比较200 ℃和300 ℃时的数据,可判断升高温度,平衡向___________ (填“正反应”或“逆反应”)方向移动,正反应方向为___________ (填“吸热”或“放热”)反应。
(2)根据平衡移动原理,合成氨适宜的条件是___________(填字母)。
(3)计算500 ℃,30 MPa时N2的转化率为___________ 。
(4)实际工业生产氨时,考虑浓度对化学平衡的影响,及500 ℃对反应速率的影响,还采取了一些措施。请分别写出其中的一个措施:___________ 。
达到平衡时平衡混合物中NH3的含量(体积分数)[投料V(N2)∶V(H2)=1∶3]。

(1)比较200 ℃和300 ℃时的数据,可判断升高温度,平衡向
(2)根据平衡移动原理,合成氨适宜的条件是___________(填字母)。
| A.高温、高压 | B.高温、低压 | C.低温、高压 | D.低温、低压 |
(4)实际工业生产氨时,考虑浓度对化学平衡的影响,及500 ℃对反应速率的影响,还采取了一些措施。请分别写出其中的一个措施:
您最近一年使用:0次
2 . 在工业合成硫酸中,其中一步反应为2SO2(g)+O2(g)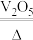 2SO3(g) ΔH=−196.6kJ·mol-1
2SO3(g) ΔH=−196.6kJ·mol-1
(1)根据反应特点,利用原理分析,增大反应速率的措施有_____ ,增大原料转化率的措施有_____ 。
(2)利用下表实验数据回答问题:
①应选择的温度是_____ ,理由是_____ 。
②应采用的压强是_____ ,理由是_____ 。
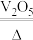 2SO3(g) ΔH=−196.6kJ·mol-1
2SO3(g) ΔH=−196.6kJ·mol-1(1)根据反应特点,利用原理分析,增大反应速率的措施有
(2)利用下表实验数据回答问题:
| 温度 | 平衡时SO2的转化率(%) | ||||
| 1×105Pa | 5×105Pa | 1×106Pa | 5×106Pa | 1×107Pa | |
| 450℃ | 97.5 | 98.9 | 99.2 | 99.6 | 99.7 |
| 550℃ | 85.6 | 92.9 | 94.9 | 97.7 | 98.3 |
②应采用的压强是
您最近一年使用:0次
名校
3 . 在一定温度和压强下,在密闭容器中充入H2、N2、NH3,开始时其物质的量之比为3∶1∶1,反应达平衡后,H2、N2、NH3的物质的量之比为9∶3∶4,则此时氮气的转化率为
| A.10% | B.20% |
| C.15% | D.30% |
您最近一年使用:0次
2023-08-27更新
|
448次组卷
|
3卷引用:作业(十五) 化学反应条件的优化--工业合成氨
22-23高一·全国·课时练习
4 . 工业炼铁是在高炉中进行的,高炉炼铁的主要反应是:①2C+O2=2CO;②Fe2O3+3CO=2Fe+3CO2。该炼铁工艺中,焦炭的实际用量远远高于按照化学方程式计算所需要的量。其主要原因是
| A.CO过量 |
| B.CO与铁矿石接触不充分 |
| C.炼铁高炉的高度不够 |
| D.反应①②都有一定限度 |
您最近一年使用:0次
22-23高一·全国·课时练习
名校
5 . 下列有关合成氨条件的选择和解释不合理的是
| A.使用催化剂,可加快N2和H2合成氨的速率 |
| B.高压比常压条件更有利于合成氨 |
| C.采用500℃左右主要考虑反应速率问题 |
| D.采用高温高压合成氨有利于提高反应速率和平衡产率 |
您最近一年使用:0次
2023-01-31更新
|
536次组卷
|
4卷引用:6.2.2 化学反应限度和化学反应条件控制——同步学习必备知识
(已下线)6.2.2 化学反应限度和化学反应条件控制——同步学习必备知识 河南大学附属中学2022-2023学年高一下学期期中考试 化学试题课时1化学反应的调控课堂例题山东省临沂市平邑县第一中学西校区2023-2024学年高二上学期第一次月考化学试题
解题方法
6 . 煤的液化是获得洁净燃料的一种形式,主要是将煤转化成乙醇(C2H5OH)。有人设想先用煤与水蒸气反应生成CO,再通过下面的反应实现煤的液化:2CO(g)+4H2(g) C2H5OH(l)+H2O(l) △H=-1709.2kJ•mol-1。你认为若要利用这个反应进行工业化生产,应采取哪些措施
C2H5OH(l)+H2O(l) △H=-1709.2kJ•mol-1。你认为若要利用这个反应进行工业化生产,应采取哪些措施____ ?
 C2H5OH(l)+H2O(l) △H=-1709.2kJ•mol-1。你认为若要利用这个反应进行工业化生产,应采取哪些措施
C2H5OH(l)+H2O(l) △H=-1709.2kJ•mol-1。你认为若要利用这个反应进行工业化生产,应采取哪些措施
您最近一年使用:0次
解题方法
7 . 工业制造硫酸的主要反应为:
SO2(g)+ O2(g)=SO3(g) △H=-99kJ•mol-1 ①
O2(g)=SO3(g) △H=-99kJ•mol-1 ①
SO3(g)+H2O(l)=H2SO4(aq) ②
反应①的平衡常数K随温度升高而减小,所用催化剂的主要成分为V2O5(6%~12%)、K2SO4(17%~20%)、SiO2(50%~70%),能使催化剂中毒的物质有砷、硒、氟等。请根据以上信息讨论二氧化硫氧化反应的工艺条件(温度、压强、原料气配比等)对工业生产硫酸的影响____ 。
SO2(g)+
 O2(g)=SO3(g) △H=-99kJ•mol-1 ①
O2(g)=SO3(g) △H=-99kJ•mol-1 ①SO3(g)+H2O(l)=H2SO4(aq) ②
反应①的平衡常数K随温度升高而减小,所用催化剂的主要成分为V2O5(6%~12%)、K2SO4(17%~20%)、SiO2(50%~70%),能使催化剂中毒的物质有砷、硒、氟等。请根据以上信息讨论二氧化硫氧化反应的工艺条件(温度、压强、原料气配比等)对工业生产硫酸的影响
您最近一年使用:0次
解题方法
8 . 你认为合成氨的化学工业生产中,选择适宜的反应条件需要从哪些角度考虑,需要考虑哪些因素____ ?适宜的工业生产条件____ 。
您最近一年使用:0次
解题方法
9 . 氮气与氢气生成氨气、二氧化硫的催化氧化都是可逆反应,研究发现降低温度有利于平衡向生成氨气或三氧化硫的方向移动,但是在实际生产中这两个反应都是在较高温度下进行的,这主要是考虑了什么因素__________ ?
您最近一年使用:0次
10 . 硫酸工业生产中有如下反应:

请回答以下问题:
(1)为什么在生产中要使用过量的空气?______
(2)为什么要使用催化剂?______
(3)为什么无须在高压下进行反应?______


请回答以下问题:
(1)为什么在生产中要使用过量的空气?
(2)为什么要使用催化剂?
(3)为什么无须在高压下进行反应?
您最近一年使用:0次



