解题方法
1 . 合成氨的反应采用400~500 ℃的原因是
| A.温度太低反应速率太小 | B.该温度时催化剂活性较高 |
| C.该温度时反应速率最大 | D.该温度时N2的转化率最高 |
您最近一年使用:0次
2 . 关于工业合成NH3的说法中不正确的是
| A.适当加压可提高氨的产率 |
| B.加入催化剂可以加快反应速率 |
| C.选择400-500℃是因该温度下氨的平衡产率最高 |
| D.将含N2和H2的原料气循环使用可以提高原料的转化率 |
您最近一年使用:0次
3 . 传统合成氨的方法需消耗大量能源。___
您最近一年使用:0次
4 . “钌单原子催化剂”合成氨体现了我国科学家在科研领域的创新。___
您最近一年使用:0次
解题方法
5 . 以钴渣(主要成分是Co2O3,含少量Al2O3、CuO、CdO、Fe2O3等)为原料制备钴和钴酸锂的流程如图,请回答下列问题:
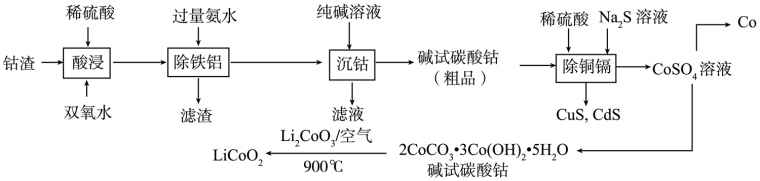
已知:①常温下,几种物质的溶度积如表所示。
②常温下,NH3·H2O的电离常数Kb=2.0×10-5。
请回答下列问题:
(1)“酸浸”前需要将钴渣粉碎,原因是____ 。
(2)滤渣的主要成分____ (写化学式)。
(3)“酸浸”时钴的浸出率与液固比的关系如图1所示。最佳液固比为____ mL·g-1;当液固比一定时,相同时间内钴的浸出率与温度的关系如图2所示,解释40℃时钴的浸出率达到峰值的原因为:____ 。
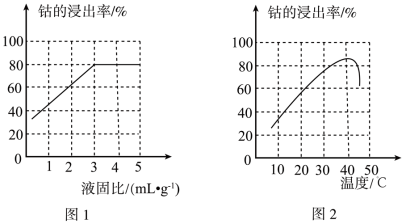
(4)“除铜镉”中,溶液中c(Co2+)=0.1mol·L-1,当c(Cd2+)=1×10-5mol·L-1时,____ (填“有”或“没有”)CoS生成。
(5)CoSO4溶液中加入小苏打溶液产生碱式碳酸钴并放出气体,写出该反应的离子方程式:____ 。

已知:①常温下,几种物质的溶度积如表所示。
| 物质 | Al(OH)3 | Fe(OH)3 | CuS | CdS | CoS |
| Ksp的近似值 | 1×10-33 | 1×10-38 | 6.4×10-44 | 8×10-27 | 4×10-21 |
请回答下列问题:
(1)“酸浸”前需要将钴渣粉碎,原因是
(2)滤渣的主要成分
(3)“酸浸”时钴的浸出率与液固比的关系如图1所示。最佳液固比为

(4)“除铜镉”中,溶液中c(Co2+)=0.1mol·L-1,当c(Cd2+)=1×10-5mol·L-1时,
(5)CoSO4溶液中加入小苏打溶液产生碱式碳酸钴并放出气体,写出该反应的离子方程式:
您最近一年使用:0次
6 . 2007年诺贝尔化学奖授予了合成氨研究领域的科学家。关于合成氨的说法正确的是
| A.该反应为吸热反应 |
| B.原料N2主要来源于化石燃料 |
| C.合成氨工业生产在常温常压下进行 |
| D.合成氨工业生产通常会使用催化剂来加快反应速率 |
您最近一年使用:0次
2020-12-11更新
|
625次组卷
|
3卷引用:2020年7月广东省普通高中学业水平合格性考试化学试卷
解题方法
7 . 合成氨工业中,采用 20MPa 到 50MPa 的压强,不需要考虑的因素是
| A.设备的制造 | B.催化剂活性 |
| C.能量消耗 | D.材料的强度 |
您最近一年使用:0次
8 . 某同学以废旧铝制易拉罐为原料制备Al(OH)3其流程如图:
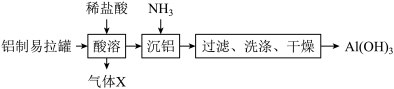
(1)“酸溶”时,增大盐酸的浓度反应速率将___ (填“增大”或“减小”)。
(2)气体X是___ (填“H2”或“CO2”)。
(3)一定条件下,将1molN2和3molH2置于lL密闭容器中合成NH3,10min后测得H2为l.2mol,则用H2表示该反应的速率为___ mol•L-1•min-1。
(4)氢氧化铝是___ (从性质上分类)氢氧化物,它与盐酸反应的化学方程式为___ 。

(1)“酸溶”时,增大盐酸的浓度反应速率将
(2)气体X是
(3)一定条件下,将1molN2和3molH2置于lL密闭容器中合成NH3,10min后测得H2为l.2mol,则用H2表示该反应的速率为
(4)氢氧化铝是
您最近一年使用:0次
9 . 《环境科学》刊发了我国科研部门采用零价铁活化过硫酸钠(过硫酸根离子如图所示)去除废水中的正五价砷[As(V)]的研究成果,其反应机制模型如图所示。设阿伏加 德罗常数的值为NA,Ksp[Fe(OH)3]=2.7×10-39。下列叙述正确的是
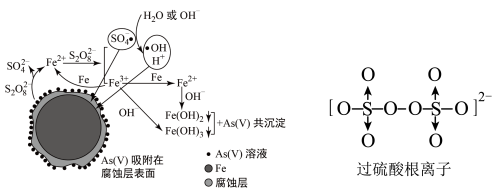

| A.室温下,中间产物 Fe(OH)3溶于水所得饱和溶液中 c(Fe3+)为2.7×10-18 mol·L-1 |
| B.若 56g Fe 参加反应,共有 NA个 S2O82-被还原 |
| C.1mol 过硫酸钠(Na2S2O8)含 2NA个过氧键 |
| D.pH 越小,越有利于去除废水中的正五价砷 |
您最近一年使用:0次
2020-05-15更新
|
348次组卷
|
3卷引用:天津市河东区2020届高三学业水平等级性考试模拟测试化学试题
10 . 硫酸是当今世界上最重要的化工产品之一,广泛应用于工业各个方面。硫酸的生产工艺几经改进,目前工业上主要采用接触法制备硫酸。接触室中发生如下反应:2SO2+O2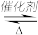 2SO3。
2SO3。
(1)上述生成SO3的反应属于__________
A.化合反应 B.分解反应
C.置换反应 D.复分解反应
(2)该反应是氧化还原反应,下列说法正确的是__________
A.SO2是氧化剂
B.O2发生氧化反应
C.O2失去电子
D.SO3既是氧化产物又是还原产物
(3)该反应也是放热反应,下列说法不正确的是__________
A.形成SO3中的硫氧键放出能量
B.断开SO2中的硫氧键放出能量
C.反应物的总能量大于生成物的总能量
D.放热反应的逆反应一定是吸热反应
(4)下列关于该反应的说法中,正确的是__________
A.增大接触室内炉气的压强对化学反应速率无影响
B.升高温度能加快反应速率
C.添加催化剂对反应速率无影响
D.增大O2的浓度能使SO2完全转化
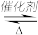 2SO3。
2SO3。(1)上述生成SO3的反应属于
A.化合反应 B.分解反应
C.置换反应 D.复分解反应
(2)该反应是氧化还原反应,下列说法正确的是
A.SO2是氧化剂
B.O2发生氧化反应
C.O2失去电子
D.SO3既是氧化产物又是还原产物
(3)该反应也是放热反应,下列说法不正确的是
A.形成SO3中的硫氧键放出能量
B.断开SO2中的硫氧键放出能量
C.反应物的总能量大于生成物的总能量
D.放热反应的逆反应一定是吸热反应
(4)下列关于该反应的说法中,正确的是
A.增大接触室内炉气的压强对化学反应速率无影响
B.升高温度能加快反应速率
C.添加催化剂对反应速率无影响
D.增大O2的浓度能使SO2完全转化
您最近一年使用:0次



