名校
1 . 合成氨工业对国民经济和社会发展具有重要的意义。
(1) 在不同温度、压强和相同催化剂条件下,初始
在不同温度、压强和相同催化剂条件下,初始 、
、 分别为0.1mol、0.3mol时,平衡后混合物中氨的体积分数(
分别为0.1mol、0.3mol时,平衡后混合物中氨的体积分数( )如图所示。
)如图所示。
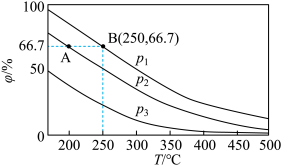
①其中,
___________  (填“>”或“<”),其原因是
(填“>”或“<”),其原因是___________ 。
②A、B两点的反应速率: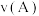
___________ 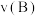 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
③若在250℃、 条件下,反应达到平衡时容器的体积为0.06L,则该条件下合成氨的平衡常数
条件下,反应达到平衡时容器的体积为0.06L,则该条件下合成氨的平衡常数
___________  (保留一位小数)。
(保留一位小数)。
(2)工业合成氨生产流程示意图如下:
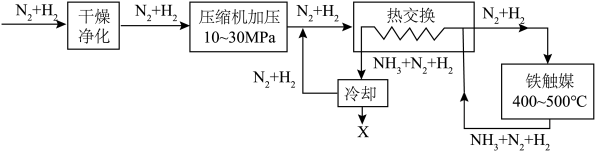
①X为___________ 。
②上述流程中,有利于提高原料利用率的措施是___________ (填标号)。
A.“净化干燥” B.“压缩机加压” C.“铁触媒400~500℃” D.原料气循环利用
③“干燥净化”中采用铜氨溶液除去CO:
 如何处理吸收CO后的铜氨溶液,请提出你的建议
如何处理吸收CO后的铜氨溶液,请提出你的建议___________ 。
(1)
 在不同温度、压强和相同催化剂条件下,初始
在不同温度、压强和相同催化剂条件下,初始 、
、 分别为0.1mol、0.3mol时,平衡后混合物中氨的体积分数(
分别为0.1mol、0.3mol时,平衡后混合物中氨的体积分数( )如图所示。
)如图所示。
①其中,

 (填“>”或“<”),其原因是
(填“>”或“<”),其原因是②A、B两点的反应速率:
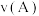
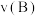 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。③若在250℃、
 条件下,反应达到平衡时容器的体积为0.06L,则该条件下合成氨的平衡常数
条件下,反应达到平衡时容器的体积为0.06L,则该条件下合成氨的平衡常数
 (保留一位小数)。
(保留一位小数)。(2)工业合成氨生产流程示意图如下:

①X为
②上述流程中,有利于提高原料利用率的措施是
A.“净化干燥” B.“压缩机加压” C.“铁触媒400~500℃” D.原料气循环利用
③“干燥净化”中采用铜氨溶液除去CO:

 如何处理吸收CO后的铜氨溶液,请提出你的建议
如何处理吸收CO后的铜氨溶液,请提出你的建议
您最近一年使用:0次
解题方法
2 . 学习“化学反应的速率和化学平衡”内容后,联系工业生产实际所发表的观点,你认为正确的是
| A.化学反应速率理论可指导怎样提高原料的平衡转化率 |
| B.化学平衡理论可指导怎样使用有限原料多出产品 |
| C.温度升高,分子动能增加,反应所需活化能减少,反应速率增大 |
| D.增大压强能提高活化分子的百分率,提高单位时间内分子有效碰撞次数 |
您最近一年使用:0次
名校
3 . 二氧化碳是主要的温室气体,也是一种工业原料。将其固定及利用,有利于缓解温室效应带来的环境问题。
(1)用二氧化碳合成甲醇。
已知:2H2(g)+O2(g)=2H2O(g) ∆H=-484kJ/mol
2CH3OH(g)+3O2(g)=2CO2(g)+4H2O(g) ∆H=-1348kJ/mol
在催化剂作用下,CO2(g)和H2(g)反应生成CH3OH(g)和H2O(g),该反应的热化学方程式是___________ 。
(2)用二氧化碳与环氧丙烷(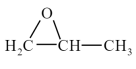 )反应合成可降解塑料PPC,同时也能生成副产物CPC,其化学反应过程中的能量变化如下图所示:在不同温度和压强下,PPC的选择性(产物中PPC的质量与产物总质量的比值)和总产率(产物总质量与反应物投料总质量的比值)如下表所示。
)反应合成可降解塑料PPC,同时也能生成副产物CPC,其化学反应过程中的能量变化如下图所示:在不同温度和压强下,PPC的选择性(产物中PPC的质量与产物总质量的比值)和总产率(产物总质量与反应物投料总质量的比值)如下表所示。
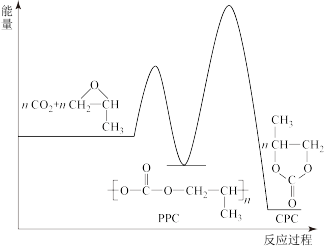
①通过表中数据ⅰ、ⅱ、ⅲ可以得出的结论是___________ 。在25℃时,实际生产中反应压强为1.5MPa,而不是2.0MPa,理由是___________ 。
②通过表中数据ⅱ、ⅳ、ⅴ可知温度升高会使PPC的选择性下降,结合上图说明其原因可能是___________ 。
(1)用二氧化碳合成甲醇。
已知:2H2(g)+O2(g)=2H2O(g) ∆H=-484kJ/mol
2CH3OH(g)+3O2(g)=2CO2(g)+4H2O(g) ∆H=-1348kJ/mol
在催化剂作用下,CO2(g)和H2(g)反应生成CH3OH(g)和H2O(g),该反应的热化学方程式是
(2)用二氧化碳与环氧丙烷(
 )反应合成可降解塑料PPC,同时也能生成副产物CPC,其化学反应过程中的能量变化如下图所示:在不同温度和压强下,PPC的选择性(产物中PPC的质量与产物总质量的比值)和总产率(产物总质量与反应物投料总质量的比值)如下表所示。
)反应合成可降解塑料PPC,同时也能生成副产物CPC,其化学反应过程中的能量变化如下图所示:在不同温度和压强下,PPC的选择性(产物中PPC的质量与产物总质量的比值)和总产率(产物总质量与反应物投料总质量的比值)如下表所示。
| 序号 | 温度/℃ | 压强/MPa | 总产率/% | PPC的选择性/% |
| ⅰ | 25 | 0.5 | 90 | 92.1 |
| ⅱ | 25 | 1.5 | 94.9 | >99 |
| ⅲ | 25 | 2.0 | 95.4 | >99 |
| ⅳ | 40 | 1.5 | 95.6 | 96.2 |
| ⅴ | 60 | 1.5 | 99 | 76 |
②通过表中数据ⅱ、ⅳ、ⅴ可知温度升高会使PPC的选择性下降,结合上图说明其原因可能是
您最近一年使用:0次
名校
解题方法
4 .  是石油化工行业尾气,是重要的氢源和硫源,工业上可以采取多种方式处理.
是石油化工行业尾气,是重要的氢源和硫源,工业上可以采取多种方式处理.
(1)电化学循环法将 转化为
转化为 和
和 ,其原理如图所示.
,其原理如图所示.
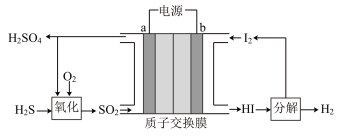
①电极a上发生反应的电极反应式为______ 。
②氧化过程中硫酸参与的反应为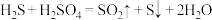 。不考虑物质和能量的损失,每处理
。不考虑物质和能量的损失,每处理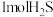 ,理论上可制得
,理论上可制得 的物质的量为
的物质的量为______ 。
(2) 时,
时, 菌在酸性环境中处理天然气中的
菌在酸性环境中处理天然气中的 的过程如图所示.
的过程如图所示.
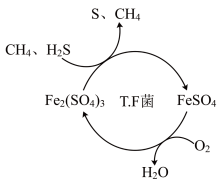
①该脱硫的过程可描述为______ 。
② 时,
时, 菌作用下,不同
菌作用下,不同 下
下 的氧化速率与
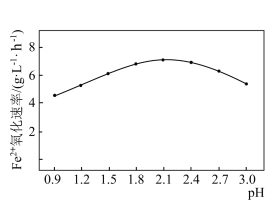
的氧化速率与 的关系如图所示.工业上选择
的关系如图所示.工业上选择 在2.1进行反应,其氧化速率最快,可能的原因是
在2.1进行反应,其氧化速率最快,可能的原因是______ .
(3)将含 尾气的空气按一定流速通入酸性
尾气的空气按一定流速通入酸性 溶液中,可实现含
溶液中,可实现含 尾气的空气脱硫.
尾气的空气脱硫. 在
在 溶液中被吸收生成硫单质的反应的化学方程式为:
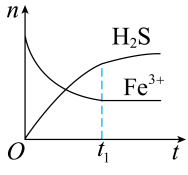
溶液中被吸收生成硫单质的反应的化学方程式为:______ .溶液中的 及被吸收的
及被吸收的 随时间
随时间 的变化如图所示.
的变化如图所示. 时刻前,溶液中
时刻前,溶液中 减小速率较快,
减小速率较快, 时刻后,溶液中
时刻后,溶液中 基本不变,其原因是
基本不变,其原因是______ .
 是石油化工行业尾气,是重要的氢源和硫源,工业上可以采取多种方式处理.
是石油化工行业尾气,是重要的氢源和硫源,工业上可以采取多种方式处理.(1)电化学循环法将
 转化为
转化为 和
和 ,其原理如图所示.
,其原理如图所示.
①电极a上发生反应的电极反应式为
②氧化过程中硫酸参与的反应为
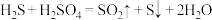 。不考虑物质和能量的损失,每处理
。不考虑物质和能量的损失,每处理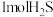 ,理论上可制得
,理论上可制得 的物质的量为
的物质的量为(2)
 时,
时, 菌在酸性环境中处理天然气中的
菌在酸性环境中处理天然气中的 的过程如图所示.
的过程如图所示.
①该脱硫的过程可描述为
②
 时,
时, 菌作用下,不同
菌作用下,不同 下
下 的氧化速率与
的氧化速率与 的关系如图所示.工业上选择
的关系如图所示.工业上选择 在2.1进行反应,其氧化速率最快,可能的原因是
在2.1进行反应,其氧化速率最快,可能的原因是
(3)将含
 尾气的空气按一定流速通入酸性
尾气的空气按一定流速通入酸性 溶液中,可实现含
溶液中,可实现含 尾气的空气脱硫.
尾气的空气脱硫. 在
在 溶液中被吸收生成硫单质的反应的化学方程式为:
溶液中被吸收生成硫单质的反应的化学方程式为: 及被吸收的
及被吸收的 随时间
随时间 的变化如图所示.
的变化如图所示. 时刻前,溶液中
时刻前,溶液中 减小速率较快,
减小速率较快, 时刻后,溶液中
时刻后,溶液中 基本不变,其原因是
基本不变,其原因是
您最近一年使用:0次
5 . 下列叙述中,不能用平衡移动原理解释的是
| A.红棕色的NO2,加压后颜色先变深后变浅 | B.高压比常压有利于合成SO3的反应 |
| C.加入催化剂有利于氨的合成 | D.光照后氯水颜色变浅 |
您最近一年使用:0次
名校
6 . 研究小组以无水正己烷为溶剂,使用特定引发剂在 下,利用异丁烯(
下,利用异丁烯(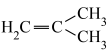 ,沸点为
,沸点为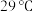 )在无水条件下合成聚异丁烯。该物质常用作润滑油添加剂。
)在无水条件下合成聚异丁烯。该物质常用作润滑油添加剂。
(1)正己烷溶剂的处理。正己烷干燥和收集的回流装置如图甲所示(夹持及加热装置略)。以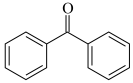 为指示剂,体系无水时呈现蓝色。
为指示剂,体系无水时呈现蓝色。

①仪器A的名称为___________ 。
②用钠丝除去正己烷中微量的水,其化学方程式为___________ 。
③若下列两过程开始时,活塞 、
、 、
、 均处于关闭状态,则:除水过程中,应打开的活塞为
均处于关闭状态,则:除水过程中,应打开的活塞为___________ ;当体系的颜色变为___________ 时,开始收集正己烷;收集过程中,应打开的活塞为___________ 。
(2)聚异丁烯的制备
①聚异丁烯的制备装置如图乙所示(夹持装置略)。三颈瓶中生成聚异丁烯的化学反应方程式为___________ 。
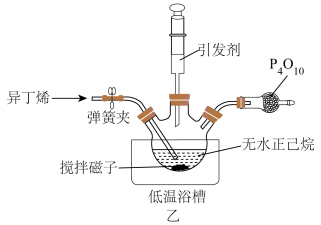
② 的作用为
的作用为___________ 。在低温浴槽中加入的最佳冷却剂为___________ (填序号)。
③将实验操作步骤补充完整:___________→d→___________→a→c→b(填序号)。________
a.搅拌下通过注射器滴加引发剂 b.经后续处理得成品
c.一定时间后加入反应终止剂停止反应 d.待三颈瓶中温度下降至既定温度
e.向三颈瓶中加入一定量无水正己烷 f.向三颈瓶中通入一定量异丁烯
(3)有研究发现,所得聚异丁烯的平均相对分子质量(M)与反应温度(T)的关系如图所示。已知T(K)=t(℃)+273,其中T为热力学温度,单位为K;t为摄氏温度,单位为℃。
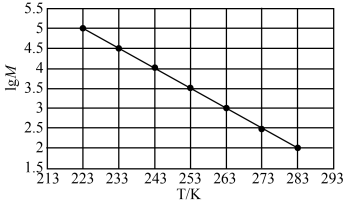
①欲合成平均相对分子质量为105的产品,则需控制反应温度t=___________ ℃。
②若控制反应温度为-30℃,则得到产品的平均聚合度为___________ (保留整数)。
 下,利用异丁烯(
下,利用异丁烯(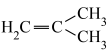 ,沸点为
,沸点为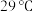 )在无水条件下合成聚异丁烯。该物质常用作润滑油添加剂。
)在无水条件下合成聚异丁烯。该物质常用作润滑油添加剂。(1)正己烷溶剂的处理。正己烷干燥和收集的回流装置如图甲所示(夹持及加热装置略)。以
 为指示剂,体系无水时呈现蓝色。
为指示剂,体系无水时呈现蓝色。
①仪器A的名称为
②用钠丝除去正己烷中微量的水,其化学方程式为
③若下列两过程开始时,活塞
 、
、 、
、 均处于关闭状态,则:除水过程中,应打开的活塞为
均处于关闭状态,则:除水过程中,应打开的活塞为(2)聚异丁烯的制备
①聚异丁烯的制备装置如图乙所示(夹持装置略)。三颈瓶中生成聚异丁烯的化学反应方程式为

②
 的作用为
的作用为| 序号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ |
| 冷却剂 | 冰水混合物 | 液氮 | 氯化钙晶体/冰 | 丙酮/干冰 | 液氨 |
| 最低温度/℃ | 0 | -195 | -55 | -78 | -33 |
a.搅拌下通过注射器滴加引发剂 b.经后续处理得成品
c.一定时间后加入反应终止剂停止反应 d.待三颈瓶中温度下降至既定温度
e.向三颈瓶中加入一定量无水正己烷 f.向三颈瓶中通入一定量异丁烯
(3)有研究发现,所得聚异丁烯的平均相对分子质量(M)与反应温度(T)的关系如图所示。已知T(K)=t(℃)+273,其中T为热力学温度,单位为K;t为摄氏温度,单位为℃。

①欲合成平均相对分子质量为105的产品,则需控制反应温度t=
②若控制反应温度为-30℃,则得到产品的平均聚合度为
您最近一年使用:0次
名校
7 . 在硫酸工业中,通过下列反应使SO2氧化为SO3:2SO2(g)+O2(g) 2SO3(g)ΔH=-196.6kJ·mol-1.下表列出了在不同温度和压强下,反应达到平衡时SO2的转化率。
2SO3(g)ΔH=-196.6kJ·mol-1.下表列出了在不同温度和压强下,反应达到平衡时SO2的转化率。
(1)从理论上分析,为了使二氧化硫尽可能多地转化为三氧化硫,应选择的条件是___________ 。
(2)在实际生产中,选定的温度为400℃~500℃,原因是___________
(3)在实际生产中,采用的压强为常压,原因是___________
(4)在实际生产中,通入过量的空气,原因是___________
(5)尾气中的SO2必须回收,原因是___________ 。
(6)在550℃、1MPa下,若SO2的起始浓度为2mol/L,O2的起始浓度为1mol/L,试求该条件下的平衡常数K=___________ 。
 2SO3(g)ΔH=-196.6kJ·mol-1.下表列出了在不同温度和压强下,反应达到平衡时SO2的转化率。
2SO3(g)ΔH=-196.6kJ·mol-1.下表列出了在不同温度和压强下,反应达到平衡时SO2的转化率。| 温度/℃ | 平衡时SO2的转化率/% | ||||
| 0.1MPa | 0.5MPa | 1MPa | 5MPa | 10MPa | |
| 450 | 97.5 | 98.9 | 99.2 | 99.6 | 99.7 |
| 550 | 85.6 | 92.9 | 95.0 | 97.7 | 98.3 |
(2)在实际生产中,选定的温度为400℃~500℃,原因是
(3)在实际生产中,采用的压强为常压,原因是
(4)在实际生产中,通入过量的空气,原因是
(5)尾气中的SO2必须回收,原因是
(6)在550℃、1MPa下,若SO2的起始浓度为2mol/L,O2的起始浓度为1mol/L,试求该条件下的平衡常数K=
您最近一年使用:0次
名校
解题方法
8 . 回答下列问题。
(1)请根据下列信息判断氢气燃烧生成水蒸气时热量变化。
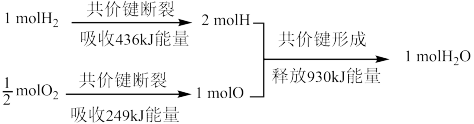
生成1mol水释放的能量___________ kJ。
(2)2SO2(g)+O2(g) 2SO3(g),是工业制硫酸的主要反应之一、某条件下,在2 L恒容容器中投入2 mol SO2和1 mol O2,如图是反应体系中部分物质的物质的量随时间的变化曲线。
2SO3(g),是工业制硫酸的主要反应之一、某条件下,在2 L恒容容器中投入2 mol SO2和1 mol O2,如图是反应体系中部分物质的物质的量随时间的变化曲线。
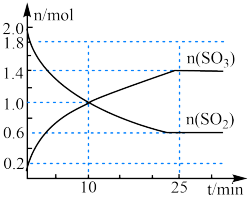
①0到10 min内, v(O2)=___________ 。
②下列情况能说明该反应达到化学平衡状态的是___________ (填字母)。
A. n(SO2) = n(SO3) B. v正 (SO2)=v逆 (SO2)
C. O2的含量保持不变 D.SO2、O2、SO3的浓度之比为2:1:2
③在密闭容器里,通入a mol SO2 (g)、b mol O2 (g)、c mol SO3 (g),发生上述反应,当改变某种条件时,反应速率会减小的是___________ (填字母)。
A.降低温度 B.加入催化剂
C.增大容器体积 D.恒容下,充入He
④工业上生产硫酸时,利用催化氧化反应将SO2转化为SO3是一个关键步骤。压强及温度对SO2转化率的影响如下表(原料气各成分的体积分数为:SO2:7%,O2:11%,N2:82%):
化工生产中,为了提高反应进行的程度而调控反应条件时,需要考虑控制反应条件的成本和实际可能性。催化氧化的生产时:温度较低时,反应速率小,需要很长时间才能达到化学平衡,生产成本高;而压强越大,对动力和生产设备的要求也越高。请结合上表,分析工业生产SO2催化氧化过程的适宜条件为:___________ 。
(1)请根据下列信息判断氢气燃烧生成水蒸气时热量变化。

生成1mol水释放的能量
(2)2SO2(g)+O2(g)
 2SO3(g),是工业制硫酸的主要反应之一、某条件下,在2 L恒容容器中投入2 mol SO2和1 mol O2,如图是反应体系中部分物质的物质的量随时间的变化曲线。
2SO3(g),是工业制硫酸的主要反应之一、某条件下,在2 L恒容容器中投入2 mol SO2和1 mol O2,如图是反应体系中部分物质的物质的量随时间的变化曲线。
①0到10 min内, v(O2)=
②下列情况能说明该反应达到化学平衡状态的是
A. n(SO2) = n(SO3) B. v正 (SO2)=v逆 (SO2)
C. O2的含量保持不变 D.SO2、O2、SO3的浓度之比为2:1:2
③在密闭容器里,通入a mol SO2 (g)、b mol O2 (g)、c mol SO3 (g),发生上述反应,当改变某种条件时,反应速率会减小的是
A.降低温度 B.加入催化剂
C.增大容器体积 D.恒容下,充入He
④工业上生产硫酸时,利用催化氧化反应将SO2转化为SO3是一个关键步骤。压强及温度对SO2转化率的影响如下表(原料气各成分的体积分数为:SO2:7%,O2:11%,N2:82%):
 | 0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
您最近一年使用:0次
2023-09-09更新
|
234次组卷
|
2卷引用:浙江省嘉兴八校联盟2021-2022学年高一下学期期中联考化学试题
名校
解题方法
9 . 下列有关合成氨工业的说法正确的是
| A.从合成塔出来的混合气体中,其中NH3只占15%,所以合成氨厂的产率都很低 |
| B.由于氨易液化,N2、H2在实际生产中可循环使用,所以总体来说合成氨的产率很高 |
| C.合成氨工业的反应温度控制在400~500℃,目的是使化学平衡向正反应方向移动 |
| D.合成氨厂采用的压强越大,产率越高,无须考虑设备、条件 |
您最近一年使用:0次
2023-09-08更新
|
278次组卷
|
2卷引用:浙江省嘉兴市八校联盟2022-2023学年高二上学期期中联考化学试题
名校
解题方法
10 . 下列关于工业合成氨的叙述错误的是
| A.反应在高压下进行,有利于提高转化率 |
| B.温度越高越有利于工业合成氨 |
| C.在工业合成氨中,N2、H2的循环利用可降低成本 |
| D.及时从反应体系中分离出氨气有利于平衡向正反应方向移动 |
您最近一年使用:0次



