名校
1 . 合成氨工业对国民经济和社会发展具有重要的意义。
(1) 在不同温度、压强和相同催化剂条件下,初始
在不同温度、压强和相同催化剂条件下,初始 、
、 分别为0.1mol、0.3mol时,平衡后混合物中氨的体积分数(
分别为0.1mol、0.3mol时,平衡后混合物中氨的体积分数( )如图所示。
)如图所示。
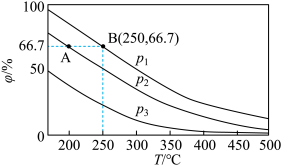
①其中,
___________  (填“>”或“<”),其原因是
(填“>”或“<”),其原因是___________ 。
②A、B两点的反应速率: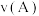
___________ 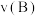 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
③若在250℃、 条件下,反应达到平衡时容器的体积为0.06L,则该条件下合成氨的平衡常数
条件下,反应达到平衡时容器的体积为0.06L,则该条件下合成氨的平衡常数
___________  (保留一位小数)。
(保留一位小数)。
(2)工业合成氨生产流程示意图如下:
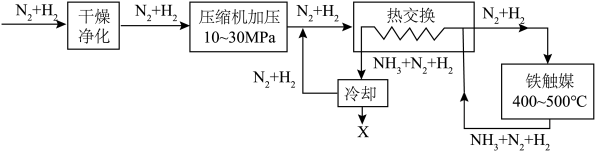
①X为___________ 。
②上述流程中,有利于提高原料利用率的措施是___________ (填标号)。
A.“净化干燥” B.“压缩机加压” C.“铁触媒400~500℃” D.原料气循环利用
③“干燥净化”中采用铜氨溶液除去CO:
 如何处理吸收CO后的铜氨溶液,请提出你的建议
如何处理吸收CO后的铜氨溶液,请提出你的建议___________ 。
(1)
 在不同温度、压强和相同催化剂条件下,初始
在不同温度、压强和相同催化剂条件下,初始 、
、 分别为0.1mol、0.3mol时,平衡后混合物中氨的体积分数(
分别为0.1mol、0.3mol时,平衡后混合物中氨的体积分数( )如图所示。
)如图所示。
①其中,

 (填“>”或“<”),其原因是
(填“>”或“<”),其原因是②A、B两点的反应速率:
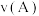
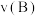 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。③若在250℃、
 条件下,反应达到平衡时容器的体积为0.06L,则该条件下合成氨的平衡常数
条件下,反应达到平衡时容器的体积为0.06L,则该条件下合成氨的平衡常数
 (保留一位小数)。
(保留一位小数)。(2)工业合成氨生产流程示意图如下:

①X为
②上述流程中,有利于提高原料利用率的措施是
A.“净化干燥” B.“压缩机加压” C.“铁触媒400~500℃” D.原料气循环利用
③“干燥净化”中采用铜氨溶液除去CO:

 如何处理吸收CO后的铜氨溶液,请提出你的建议
如何处理吸收CO后的铜氨溶液,请提出你的建议
您最近一年使用:0次
解题方法
2 . 学习“化学反应的速率和化学平衡”内容后,联系工业生产实际所发表的观点,你认为正确的是
| A.化学反应速率理论可指导怎样提高原料的平衡转化率 |
| B.化学平衡理论可指导怎样使用有限原料多出产品 |
| C.温度升高,分子动能增加,反应所需活化能减少,反应速率增大 |
| D.增大压强能提高活化分子的百分率,提高单位时间内分子有效碰撞次数 |
您最近一年使用:0次
名校
解题方法
3 .  是石油化工行业尾气,是重要的氢源和硫源,工业上可以采取多种方式处理.
是石油化工行业尾气,是重要的氢源和硫源,工业上可以采取多种方式处理.
(1)电化学循环法将 转化为
转化为 和
和 ,其原理如图所示.
,其原理如图所示.
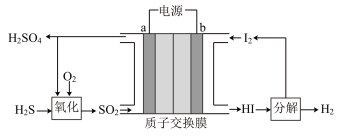
①电极a上发生反应的电极反应式为______ 。
②氧化过程中硫酸参与的反应为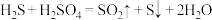 。不考虑物质和能量的损失,每处理
。不考虑物质和能量的损失,每处理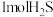 ,理论上可制得
,理论上可制得 的物质的量为
的物质的量为______ 。
(2) 时,
时, 菌在酸性环境中处理天然气中的
菌在酸性环境中处理天然气中的 的过程如图所示.
的过程如图所示.
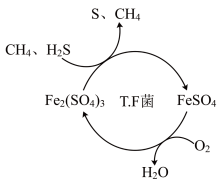
①该脱硫的过程可描述为______ 。
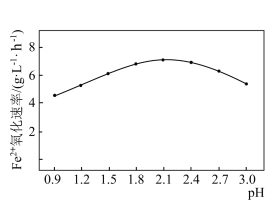
② 时,
时, 菌作用下,不同
菌作用下,不同 下
下 的氧化速率与
的氧化速率与 的关系如图所示.工业上选择
的关系如图所示.工业上选择 在2.1进行反应,其氧化速率最快,可能的原因是
在2.1进行反应,其氧化速率最快,可能的原因是______ .
(3)将含 尾气的空气按一定流速通入酸性
尾气的空气按一定流速通入酸性 溶液中,可实现含
溶液中,可实现含 尾气的空气脱硫.
尾气的空气脱硫. 在
在 溶液中被吸收生成硫单质的反应的化学方程式为:
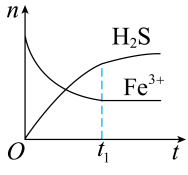
溶液中被吸收生成硫单质的反应的化学方程式为:______ .溶液中的 及被吸收的
及被吸收的 随时间
随时间 的变化如图所示.
的变化如图所示. 时刻前,溶液中
时刻前,溶液中 减小速率较快,
减小速率较快, 时刻后,溶液中
时刻后,溶液中 基本不变,其原因是
基本不变,其原因是______ .
 是石油化工行业尾气,是重要的氢源和硫源,工业上可以采取多种方式处理.
是石油化工行业尾气,是重要的氢源和硫源,工业上可以采取多种方式处理.(1)电化学循环法将
 转化为
转化为 和
和 ,其原理如图所示.
,其原理如图所示.
①电极a上发生反应的电极反应式为
②氧化过程中硫酸参与的反应为
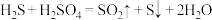 。不考虑物质和能量的损失,每处理
。不考虑物质和能量的损失,每处理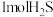 ,理论上可制得
,理论上可制得 的物质的量为
的物质的量为(2)
 时,
时, 菌在酸性环境中处理天然气中的
菌在酸性环境中处理天然气中的 的过程如图所示.
的过程如图所示.
①该脱硫的过程可描述为
②
 时,
时, 菌作用下,不同
菌作用下,不同 下
下 的氧化速率与
的氧化速率与 的关系如图所示.工业上选择
的关系如图所示.工业上选择 在2.1进行反应,其氧化速率最快,可能的原因是
在2.1进行反应,其氧化速率最快,可能的原因是
(3)将含
 尾气的空气按一定流速通入酸性
尾气的空气按一定流速通入酸性 溶液中,可实现含
溶液中,可实现含 尾气的空气脱硫.
尾气的空气脱硫. 在
在 溶液中被吸收生成硫单质的反应的化学方程式为:
溶液中被吸收生成硫单质的反应的化学方程式为: 及被吸收的
及被吸收的 随时间
随时间 的变化如图所示.
的变化如图所示. 时刻前,溶液中
时刻前,溶液中 减小速率较快,
减小速率较快, 时刻后,溶液中
时刻后,溶液中 基本不变,其原因是
基本不变,其原因是
您最近一年使用:0次
名校
4 . 在硫酸工业中,通过下列反应使SO2氧化为SO3:2SO2(g)+O2(g) 2SO3(g)ΔH=-196.6kJ·mol-1.下表列出了在不同温度和压强下,反应达到平衡时SO2的转化率。
2SO3(g)ΔH=-196.6kJ·mol-1.下表列出了在不同温度和压强下,反应达到平衡时SO2的转化率。
(1)从理论上分析,为了使二氧化硫尽可能多地转化为三氧化硫,应选择的条件是___________ 。
(2)在实际生产中,选定的温度为400℃~500℃,原因是___________
(3)在实际生产中,采用的压强为常压,原因是___________
(4)在实际生产中,通入过量的空气,原因是___________
(5)尾气中的SO2必须回收,原因是___________ 。
(6)在550℃、1MPa下,若SO2的起始浓度为2mol/L,O2的起始浓度为1mol/L,试求该条件下的平衡常数K=___________ 。
 2SO3(g)ΔH=-196.6kJ·mol-1.下表列出了在不同温度和压强下,反应达到平衡时SO2的转化率。
2SO3(g)ΔH=-196.6kJ·mol-1.下表列出了在不同温度和压强下,反应达到平衡时SO2的转化率。| 温度/℃ | 平衡时SO2的转化率/% | ||||
| 0.1MPa | 0.5MPa | 1MPa | 5MPa | 10MPa | |
| 450 | 97.5 | 98.9 | 99.2 | 99.6 | 99.7 |
| 550 | 85.6 | 92.9 | 95.0 | 97.7 | 98.3 |
(2)在实际生产中,选定的温度为400℃~500℃,原因是
(3)在实际生产中,采用的压强为常压,原因是
(4)在实际生产中,通入过量的空气,原因是
(5)尾气中的SO2必须回收,原因是
(6)在550℃、1MPa下,若SO2的起始浓度为2mol/L,O2的起始浓度为1mol/L,试求该条件下的平衡常数K=
您最近一年使用:0次
名校
解题方法
5 . 回答下列问题。
(1)请根据下列信息判断氢气燃烧生成水蒸气时热量变化。
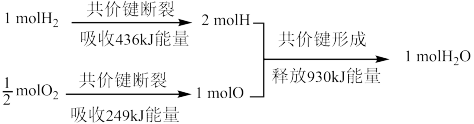
生成1mol水释放的能量___________ kJ。
(2)2SO2(g)+O2(g) 2SO3(g),是工业制硫酸的主要反应之一、某条件下,在2 L恒容容器中投入2 mol SO2和1 mol O2,如图是反应体系中部分物质的物质的量随时间的变化曲线。
2SO3(g),是工业制硫酸的主要反应之一、某条件下,在2 L恒容容器中投入2 mol SO2和1 mol O2,如图是反应体系中部分物质的物质的量随时间的变化曲线。
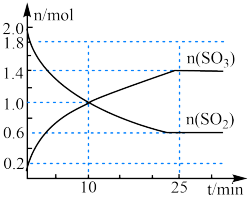
①0到10 min内, v(O2)=___________ 。
②下列情况能说明该反应达到化学平衡状态的是___________ (填字母)。
A. n(SO2) = n(SO3) B. v正 (SO2)=v逆 (SO2)
C. O2的含量保持不变 D.SO2、O2、SO3的浓度之比为2:1:2
③在密闭容器里,通入a mol SO2 (g)、b mol O2 (g)、c mol SO3 (g),发生上述反应,当改变某种条件时,反应速率会减小的是___________ (填字母)。
A.降低温度 B.加入催化剂
C.增大容器体积 D.恒容下,充入He
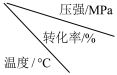
④工业上生产硫酸时,利用催化氧化反应将SO2转化为SO3是一个关键步骤。压强及温度对SO2转化率的影响如下表(原料气各成分的体积分数为:SO2:7%,O2:11%,N2:82%):
化工生产中,为了提高反应进行的程度而调控反应条件时,需要考虑控制反应条件的成本和实际可能性。催化氧化的生产时:温度较低时,反应速率小,需要很长时间才能达到化学平衡,生产成本高;而压强越大,对动力和生产设备的要求也越高。请结合上表,分析工业生产SO2催化氧化过程的适宜条件为:___________ 。
(1)请根据下列信息判断氢气燃烧生成水蒸气时热量变化。

生成1mol水释放的能量
(2)2SO2(g)+O2(g)
 2SO3(g),是工业制硫酸的主要反应之一、某条件下,在2 L恒容容器中投入2 mol SO2和1 mol O2,如图是反应体系中部分物质的物质的量随时间的变化曲线。
2SO3(g),是工业制硫酸的主要反应之一、某条件下,在2 L恒容容器中投入2 mol SO2和1 mol O2,如图是反应体系中部分物质的物质的量随时间的变化曲线。
①0到10 min内, v(O2)=
②下列情况能说明该反应达到化学平衡状态的是
A. n(SO2) = n(SO3) B. v正 (SO2)=v逆 (SO2)
C. O2的含量保持不变 D.SO2、O2、SO3的浓度之比为2:1:2
③在密闭容器里,通入a mol SO2 (g)、b mol O2 (g)、c mol SO3 (g),发生上述反应,当改变某种条件时,反应速率会减小的是
A.降低温度 B.加入催化剂
C.增大容器体积 D.恒容下,充入He
④工业上生产硫酸时,利用催化氧化反应将SO2转化为SO3是一个关键步骤。压强及温度对SO2转化率的影响如下表(原料气各成分的体积分数为:SO2:7%,O2:11%,N2:82%):
 | 0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
您最近一年使用:0次
2023-09-09更新
|
248次组卷
|
2卷引用:浙江省嘉兴八校联盟2021-2022学年高一下学期期中联考化学试题
名校
解题方法
6 . 下列关于工业合成氨的叙述错误的是
| A.反应在高压下进行,有利于提高转化率 |
| B.温度越高越有利于工业合成氨 |
| C.在工业合成氨中,N2、H2的循环利用可降低成本 |
| D.及时从反应体系中分离出氨气有利于平衡向正反应方向移动 |
您最近一年使用:0次
名校
解题方法
7 . 工业上制备硫酸的一步重要反应是 在400~500℃下的催化氧化反应:
在400~500℃下的催化氧化反应:
 。下列有关说法错误的是
。下列有关说法错误的是
 在400~500℃下的催化氧化反应:
在400~500℃下的催化氧化反应:
 。下列有关说法错误的是
。下列有关说法错误的是A.常通入过量的空气,以提高 的平衡转化率 的平衡转化率 |
| B.为提高反应速率和平衡转化率,采用的压强越大越好 |
| C.控制温度为400~500℃既能提升反应速率,又能使催化剂有较高的活性 |
| D.要综合考虑影响速率与平衡的各种因素、设备条件和经济成本等,寻找适宜的生产条件 |
您最近一年使用:0次
2023-08-12更新
|
414次组卷
|
8卷引用:河南省周口市无锡天一企业管理有限公司等2校2022-2023学年高二上学期12月期末考试化学试题
河南省周口市无锡天一企业管理有限公司等2校2022-2023学年高二上学期12月期末考试化学试题山东省鄄城县第一中学2023-2024学年高二上学期9月月考化学试题黑龙江省哈尔滨市第一中学校2023-2024学年高二上学期第一次质量检测化学试题(已下线)专题05 化学反应的方向 化学反应的调控 -【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(人教版2019)天津市天津中学2023-2024学年高二上学期第一次月考化学试题(已下线)寒假作业04 化学反应的方向及调控-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)四川省宜宾市叙州区第二中学校2023-2024学年高二上学期12月月考化学试题安徽省六安市裕安区新安中学2023-2024学年高二下学期第一次月考化学试题
名校
解题方法
8 . 金属钪可用作宇航材料、火箭和飞机的制造材料;氧化钪可提高计算机记忆元件性能。铝土矿(主要成分 )经碱初步溶解后得到的赤泥含有丰富的钪元素,另含少量CaO、
)经碱初步溶解后得到的赤泥含有丰富的钪元素,另含少量CaO、 、
、 、
、 等氧化物。一种从赤泥中提取氧化钪的工艺流程如下图所示,已知:P2O4(磷酸酯浸取剂)是一种酸性萃取剂。
等氧化物。一种从赤泥中提取氧化钪的工艺流程如下图所示,已知:P2O4(磷酸酯浸取剂)是一种酸性萃取剂。
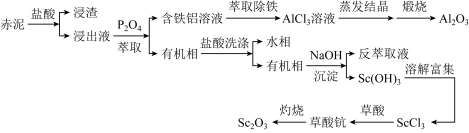
回答下列问题:
(1)写出铝土矿经碱初步溶解时所发生的主要离子方程式:_____ 。
(2)写出赤泥经盐酸处理后所得“浸渣”的一种用途:_____ 。
(3)反萃取时, 完全沉淀(浓度为
完全沉淀(浓度为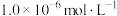 )时,反萃取液的pH为
)时,反萃取液的pH为_____ 。(已知: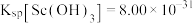 ,
, ,结果保留小数点后2位)。
,结果保留小数点后2位)。
(4)草酸钪灼烧分解在无氧环境下进行,其反应的化学方程式为_____ 。
(5)在流程中可循环使用的物质有_____ 。
 )经碱初步溶解后得到的赤泥含有丰富的钪元素,另含少量CaO、
)经碱初步溶解后得到的赤泥含有丰富的钪元素,另含少量CaO、 、
、 、
、 等氧化物。一种从赤泥中提取氧化钪的工艺流程如下图所示,已知:P2O4(磷酸酯浸取剂)是一种酸性萃取剂。
等氧化物。一种从赤泥中提取氧化钪的工艺流程如下图所示,已知:P2O4(磷酸酯浸取剂)是一种酸性萃取剂。
回答下列问题:
(1)写出铝土矿经碱初步溶解时所发生的主要离子方程式:
(2)写出赤泥经盐酸处理后所得“浸渣”的一种用途:
(3)反萃取时,
 完全沉淀(浓度为
完全沉淀(浓度为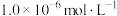 )时,反萃取液的pH为
)时,反萃取液的pH为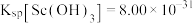 ,
, ,结果保留小数点后2位)。
,结果保留小数点后2位)。(4)草酸钪灼烧分解在无氧环境下进行,其反应的化学方程式为
(5)在流程中可循环使用的物质有
您最近一年使用:0次
名校
9 . 硫酸是一种重要的化工产品,目前主要采用“接触法”进行生产。有关反应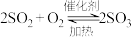 的说法中不正确的是
的说法中不正确的是
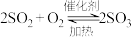 的说法中不正确的是
的说法中不正确的是A.实际生产中, 、 、 再循环使用提高原料利用率 再循环使用提高原料利用率 |
| B.实际生产中,为了提高反应速率,压强越高越好 |
C.在生产中,通入过量空气的目的是提高 的转化率 的转化率 |
| D.实际生产中,选定400~500℃作为操作温度的主要原因是催化剂的活性最高 |
您最近一年使用:0次
2023-06-08更新
|
258次组卷
|
3卷引用:广东省大埔县虎山中学等五校2022-2023学年高二上学期(11月)期中考试化学试题
名校
10 . 氨既是一种重要的化工产品,又是一种重要的化工原料。下图为合成氨以及氨催化制硝酸的流程示意图。下列说法不正确 的是
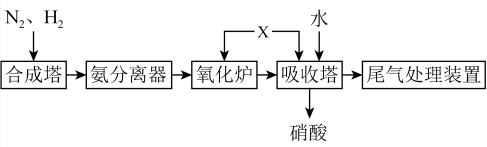

A.可以利用 易液化的性质分离出 易液化的性质分离出 |
B.X为 ,其作用是将氮氧化物充分氧化为 ,其作用是将氮氧化物充分氧化为 |
C.可以用 进行氮氧化物的尾气处理 进行氮氧化物的尾气处理 |
| D.合成氨以及氨催化制硝酸的流程中氮元素均被氧化 |
您最近一年使用:0次



