2024高三·全国·专题练习
1 . 以Cl2、SO2和PCl3为原料,制备POCl3和氯化亚砜(SOCl2)的原理为PCl3(g)+Cl2(g)+SO2(g) POCl3(s)+SOCl2(g);ΔH<0,下列说法正确的是
POCl3(s)+SOCl2(g);ΔH<0,下列说法正确的是
 POCl3(s)+SOCl2(g);ΔH<0,下列说法正确的是
POCl3(s)+SOCl2(g);ΔH<0,下列说法正确的是| A.使用催化剂可以同时降低正反应和逆反应的活化能 |
| B.1molCl-Cl键断裂的同时有2molS-Cl键形成,说明反应到达该条件下的平衡状态 |
C.反应平衡常数K= |
| D.上述反应中消耗3.36LCl2,转移电子数为0.3×6.02×1023 |
您最近半年使用:0次
2024高三·全国·专题练习
2 . 工业合成氨常选择反应:N2+3H2 2NH3,设NA为阿伏加德罗常数的值,下列说法正确的是
2NH3,设NA为阿伏加德罗常数的值,下列说法正确的是
 2NH3,设NA为阿伏加德罗常数的值,下列说法正确的是
2NH3,设NA为阿伏加德罗常数的值,下列说法正确的是| A.28 g N2完全反应,转移的电子数为3NA |
| B.混合气中物质的沸点:NH3>N2>H2 |
| C.在一定温度的固定容器中进行反应,通入氦气,能提高氢气的转化率 |
| D.反应物断裂NA个σ键的同时生成物断裂NA个σ键,反应达到平衡状态 |
您最近半年使用:0次
2024高三·全国·专题练习
解题方法
3 . Ⅰ.H2S与CH4重整,不但可以消除污染,还可以制氢。主要反应为 ;ΔH>0。
;ΔH>0。
(1)在恒温恒容条件下,可作为上述反应达到平衡状态的判断依据的是_______。
Ⅱ.在恒压条件下,以n(CH4)∶n(H2S)=1∶2组成的混合气体发生反应: ;ΔH>0,达到平衡状态时,四种组分物质的量分数随温度的变化如下图所示。
;ΔH>0,达到平衡状态时,四种组分物质的量分数随温度的变化如下图所示。_______ 、_______ (填化学式)。
(3)M点对应温度下,H2S的转化率是_______ 。
Ⅲ.在研究反应发生的适宜条件时发现:过多的CH4会导致Al2O3催化剂失活;Co助剂有稳定催化剂的作用。如下图表示800 ℃,Al2O3催化剂条件下投入等量H2S,投料比[n(CH4)∶n(H2S)]分别为1∶1、1∶3、12∶1,达平衡时H2S转化率、平均反应速率。_______ (填“A”“B”或“C”)组图像。三组图像中,C组图像中平均反应速率最低的可能原因是_______ 。
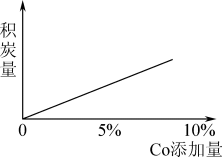
(5)未添加Co助剂时,无积炭,随着Co添加量的变化,积炭量变化如下图所示,Co助剂可能催化原料气发生反应的化学方程式为____ 。
 ;ΔH>0。
;ΔH>0。(1)在恒温恒容条件下,可作为上述反应达到平衡状态的判断依据的是_______。
| A.混合气体密度不变 |
| B.容器内压强不变 |
| C.2v正(H2S)=v逆(CS2) |
| D.CH4与H2的物质的量分数之比保持不变 |
Ⅱ.在恒压条件下,以n(CH4)∶n(H2S)=1∶2组成的混合气体发生反应:
 ;ΔH>0,达到平衡状态时,四种组分物质的量分数随温度的变化如下图所示。
;ΔH>0,达到平衡状态时,四种组分物质的量分数随温度的变化如下图所示。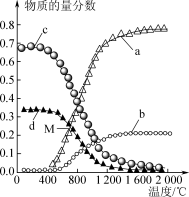
(3)M点对应温度下,H2S的转化率是
Ⅲ.在研究反应发生的适宜条件时发现:过多的CH4会导致Al2O3催化剂失活;Co助剂有稳定催化剂的作用。如下图表示800 ℃,Al2O3催化剂条件下投入等量H2S,投料比[n(CH4)∶n(H2S)]分别为1∶1、1∶3、12∶1,达平衡时H2S转化率、平均反应速率。
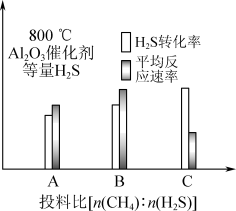
(5)未添加Co助剂时,无积炭,随着Co添加量的变化,积炭量变化如下图所示,Co助剂可能催化原料气发生反应的化学方程式为
您最近半年使用:0次
4 . I.将等物质的量A、B混合于1L的密闭容器中,发生反应,3A(g)+B(g) xC(g)+2D(s),经5min后达到平衡,测得D的物质的量为2mol,c(A):c(B)=3:5,C的平均反应速率是0.2mol/(L•min)。请计算:
xC(g)+2D(s),经5min后达到平衡,测得D的物质的量为2mol,c(A):c(B)=3:5,C的平均反应速率是0.2mol/(L•min)。请计算:
(1)前5min内用B表示的平均反应速率___________ 。
(2)平衡时容器内气体的压强与起始时容器内压强的比值为___________ 。
(3)将一定量纯净的氨基甲酸铵(NH2COONH4)置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s) 2NH3(g)+CO2(g)。下列不能判断该分解反应已经达到化学平衡状态的是
2NH3(g)+CO2(g)。下列不能判断该分解反应已经达到化学平衡状态的是___________ (填序号)。
①v正(NH3)=2v逆(CO2) ②密闭容器中NH3的物质的量不变
③容器中NH3与CO2的物质的量之比保持不变 ④密闭容器中气体总压强保持不变
⑤CO2(g)的体积分数保持不变 ⑥形成2molNH3的同时消耗1molCO2
⑦气体的平均相对分子质量保持不变 ⑧混合气体的密度保持不变
Ⅱ.汽车尾气有污染,汽车尾气中含有CO、NO等有害气体。利用催化技术可将汽车尾气中的CO和NO转化为CO2和N2,化学方程式为:2NO+2CO 2CO2+N2,在反应物初始浓度相同,实验温度为200℃和300℃条件下,进行以下实验:
2CO2+N2,在反应物初始浓度相同,实验温度为200℃和300℃条件下,进行以下实验:
【实验分析与结论】
(4)补全表格:a.___________ ;b. ___________ 。
(5)测得 ,对比实验1、3,可得结论:
,对比实验1、3,可得结论:___________ 。
(6)通过实验可得到“温度相同时,增大催化剂的比表面积,可增大尾气的转化速率”的结论,证据是对比实验1、2,
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
 xC(g)+2D(s),经5min后达到平衡,测得D的物质的量为2mol,c(A):c(B)=3:5,C的平均反应速率是0.2mol/(L•min)。请计算:
xC(g)+2D(s),经5min后达到平衡,测得D的物质的量为2mol,c(A):c(B)=3:5,C的平均反应速率是0.2mol/(L•min)。请计算:(1)前5min内用B表示的平均反应速率
(2)平衡时容器内气体的压强与起始时容器内压强的比值为
(3)将一定量纯净的氨基甲酸铵(NH2COONH4)置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)
 2NH3(g)+CO2(g)。下列不能判断该分解反应已经达到化学平衡状态的是
2NH3(g)+CO2(g)。下列不能判断该分解反应已经达到化学平衡状态的是①v正(NH3)=2v逆(CO2) ②密闭容器中NH3的物质的量不变
③容器中NH3与CO2的物质的量之比保持不变 ④密闭容器中气体总压强保持不变
⑤CO2(g)的体积分数保持不变 ⑥形成2molNH3的同时消耗1molCO2
⑦气体的平均相对分子质量保持不变 ⑧混合气体的密度保持不变
Ⅱ.汽车尾气有污染,汽车尾气中含有CO、NO等有害气体。利用催化技术可将汽车尾气中的CO和NO转化为CO2和N2,化学方程式为:2NO+2CO
 2CO2+N2,在反应物初始浓度相同,实验温度为200℃和300℃条件下,进行以下实验:
2CO2+N2,在反应物初始浓度相同,实验温度为200℃和300℃条件下,进行以下实验:| 实验编号 | 实验目的 | 温度 (℃) | 同种催化剂的比表面积(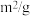 ) ) | 达平衡时所用时间(s) |
| 1 | 对照试验 | 200 | 50 |  |
| 2 | 研究催化剂的比表面积对尾气转化速率的影响 | 200 | 80 |  |
| 3 | a | 300 | b |  |
(4)补全表格:a.
(5)测得
 ,对比实验1、3,可得结论:
,对比实验1、3,可得结论:(6)通过实验可得到“温度相同时,增大催化剂的比表面积,可增大尾气的转化速率”的结论,证据是对比实验1、2,

 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
您最近半年使用:0次
解题方法
5 . 我国向国际社会承诺,2023年买现“碳达峰”,2060年实现“碳中和”。已知500℃时,在2L恒容密闭容器中充入2mol  和6mol
和6mol  ,发生反应:
,发生反应: ,∆H=-49kJ/mol平衡时体系压强为
,∆H=-49kJ/mol平衡时体系压强为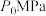 ,测得
,测得 和
和 的浓度随时间变化如图所示。
的浓度随时间变化如图所示。
_______ mol/(L∙min)。 H2和CO2转化率关系_______ (相等、不相等),15分钟后平衡,平衡时H2的转化率为_______ 。
(2)下列能说明该反应已达到平衡状态的是_________ 。
A.气体的密度不再变化
B.容器内气体的压强不再变化
C.
D. 、
、 、
、 和
和 浓度之比为1:3:1:1
浓度之比为1:3:1:1
该温度下平衡常数
________ (用各气体分压代入K的公式,用含 的代数式表示,
的代数式表示, 为以分压表示的平衡常数,分压=总压×物质的量分数)。
为以分压表示的平衡常数,分压=总压×物质的量分数)。
一定比例的 和
和 在装有催化剂的反应器中反应12小时。体系中甲醇的产率和催化剂的催化活性与温度的关系如图所示。
在装有催化剂的反应器中反应12小时。体系中甲醇的产率和催化剂的催化活性与温度的关系如图所示。________ (填是或不是)处于平衡状态,如果P不是平衡的,继续反应则平衡转化率________ 。490K之后,甲醇产率下降的原因是________________ 。
电解法转化 可实现
可实现 的资源化利用,电解
的资源化利用,电解 制
制 的原理示意图如图所示:
的原理示意图如图所示:______ 极相连,反应时阴极电极反应式为_____________ 。
 和6mol
和6mol  ,发生反应:
,发生反应: ,∆H=-49kJ/mol平衡时体系压强为
,∆H=-49kJ/mol平衡时体系压强为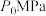 ,测得
,测得 和
和 的浓度随时间变化如图所示。
的浓度随时间变化如图所示。

(2)下列能说明该反应已达到平衡状态的是
A.气体的密度不再变化
B.容器内气体的压强不再变化
C.

D.
 、
、 、
、 和
和 浓度之比为1:3:1:1
浓度之比为1:3:1:1该温度下平衡常数

 的代数式表示,
的代数式表示, 为以分压表示的平衡常数,分压=总压×物质的量分数)。
为以分压表示的平衡常数,分压=总压×物质的量分数)。一定比例的
 和
和 在装有催化剂的反应器中反应12小时。体系中甲醇的产率和催化剂的催化活性与温度的关系如图所示。
在装有催化剂的反应器中反应12小时。体系中甲醇的产率和催化剂的催化活性与温度的关系如图所示。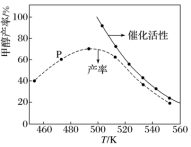
电解法转化
 可实现
可实现 的资源化利用,电解
的资源化利用,电解 制
制 的原理示意图如图所示:
的原理示意图如图所示: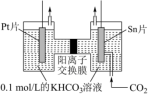
您最近半年使用:0次
名校
解题方法
6 . 对 和
和 进行回收利用是节能减排的重要课题。某温度下,向恒容密闭容器中充入
进行回收利用是节能减排的重要课题。某温度下,向恒容密闭容器中充入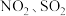 发生反应:
发生反应: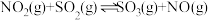 。
。
(1)①只改变下列某一反应条件时,能使上述反应速率加快的是_______ 。
A.使用高效催化剂 B. 向容器中充入氩气
C. 降低温度 D. 减小 的物质的量
的物质的量
②下列能说明反应达到平衡状态的是_______ 。
A.混合气体的密度保持不变
B. 的物质的量保持不变
的物质的量保持不变
C.容器内混合气体原子总数不变
D.每生成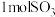 的同时消耗
的同时消耗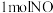
(2)在体积为 密闭容器中充入
密闭容器中充入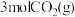 和
和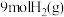 ,发生反应
,发生反应 ,测得
,测得 的物质的量随时间变化如图所示。
的物质的量随时间变化如图所示。 时,
时,
_______  (填>“<”或“=)。
(填>“<”或“=)。
②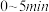 内,
内,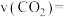
_______  。
。
③反应达到平衡状态时,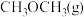 的体积分数为
的体积分数为_______  (保留1位小数)。
(保留1位小数)。
④a、b、c三点中代表达到平衡的是_______ ,a点的正反应速率_______ (填>、<或=)b点的逆反应速率
⑤“二甲醚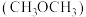 酸性燃料电池”的工作原理示意图如图所示。A电极为
酸性燃料电池”的工作原理示意图如图所示。A电极为_______ (填“正”或“负”)极:该电极的电极反应式为:_______ ,当消耗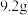 的二甲醚时,转移电子的数目为:
的二甲醚时,转移电子的数目为:_______ 。
 和
和 进行回收利用是节能减排的重要课题。某温度下,向恒容密闭容器中充入
进行回收利用是节能减排的重要课题。某温度下,向恒容密闭容器中充入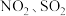 发生反应:
发生反应: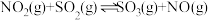 。
。(1)①只改变下列某一反应条件时,能使上述反应速率加快的是
A.使用高效催化剂 B. 向容器中充入氩气
C. 降低温度 D. 减小
 的物质的量
的物质的量②下列能说明反应达到平衡状态的是
A.混合气体的密度保持不变
B.
 的物质的量保持不变
的物质的量保持不变C.容器内混合气体原子总数不变
D.每生成
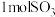 的同时消耗
的同时消耗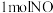
(2)在体积为
 密闭容器中充入
密闭容器中充入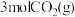 和
和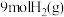 ,发生反应
,发生反应 ,测得
,测得 的物质的量随时间变化如图所示。
的物质的量随时间变化如图所示。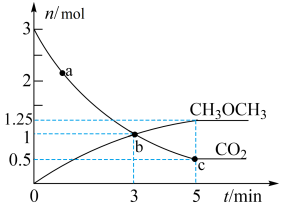
 时,
时,
 (填>“<”或“=)。
(填>“<”或“=)。②
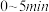 内,
内,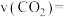
 。
。 ③反应达到平衡状态时,
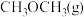 的体积分数为
的体积分数为 (保留1位小数)。
(保留1位小数)。④a、b、c三点中代表达到平衡的是
⑤“二甲醚
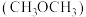 酸性燃料电池”的工作原理示意图如图所示。A电极为
酸性燃料电池”的工作原理示意图如图所示。A电极为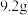 的二甲醚时,转移电子的数目为:
的二甲醚时,转移电子的数目为:
您最近半年使用:0次
名校
7 . 研究硫及其化合物的性质具有重要意义。
Ⅰ.已知 可以催化二氧化硫在水溶液中发生的歧化反应:
可以催化二氧化硫在水溶液中发生的歧化反应:

 ,催化原理分为两步,
,催化原理分为两步,
第一步反应为吸热的慢反应:
第二步反应为放热的快反应: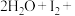 ______
______ ______+______
______+______
(1)请补充第二步反应:______ 。
(2)能正确表示 催化
催化 歧化反应原理的能量变化示意图为______(填标号)。
歧化反应原理的能量变化示意图为______(填标号)。
Ⅱ.工业制硫酸,在接触室发生反应: ,在1L的恒容密闭容器中充入2mol
,在1L的恒容密闭容器中充入2mol 和1mol
和1mol ,在不同温度下测得
,在不同温度下测得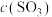 与时间的关系如图A:
与时间的关系如图A:
______ 0(填“>”“<”或“=”)。
(4)能证明反应已经达到平衡状态的是______ (填序号)。
①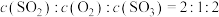
②单位时间内生成n mol 的同时消耗n mol
的同时消耗n mol
③反应速率
④温度和体积一定时,容器内压强不再变化
⑤温度和体积一定时,混合气体的密度不再变化
(5)反应开始到10min时 的平均反应速率
的平均反应速率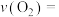
______ mol/(L·min); 时该反应的平衡常数
时该反应的平衡常数
______ L/mol。
(6)一定条件下在恒温恒容的密闭容器中按一定比例充入 和
和 ,平衡时
,平衡时 的体积分数随
的体积分数随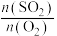 的变化如图B,则A、B、C三状态中,
的变化如图B,则A、B、C三状态中, 的转化率最小的是
的转化率最小的是______ 点,当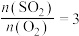 时,达到平衡状态
时,达到平衡状态 的体积分数可能是D、E、F三点中的
的体积分数可能是D、E、F三点中的______ 点。
Ⅰ.已知
 可以催化二氧化硫在水溶液中发生的歧化反应:
可以催化二氧化硫在水溶液中发生的歧化反应:
 ,催化原理分为两步,
,催化原理分为两步,第一步反应为吸热的慢反应:

第二步反应为放热的快反应:
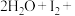 ______
______ ______+______
______+______
(1)请补充第二步反应:
(2)能正确表示
 催化
催化 歧化反应原理的能量变化示意图为______(填标号)。
歧化反应原理的能量变化示意图为______(填标号)。A.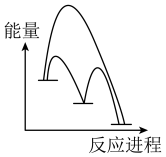 | B.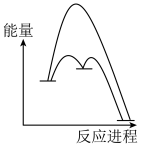 |
C.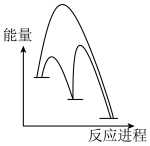 | D.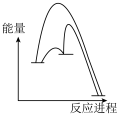 |
Ⅱ.工业制硫酸,在接触室发生反应:
 ,在1L的恒容密闭容器中充入2mol
,在1L的恒容密闭容器中充入2mol 和1mol
和1mol ,在不同温度下测得
,在不同温度下测得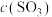 与时间的关系如图A:
与时间的关系如图A: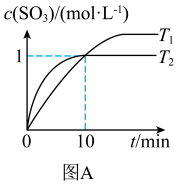

(4)能证明反应已经达到平衡状态的是
①
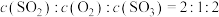
②单位时间内生成n mol
 的同时消耗n mol
的同时消耗n mol
③反应速率

④温度和体积一定时,容器内压强不再变化
⑤温度和体积一定时,混合气体的密度不再变化
(5)反应开始到10min时
 的平均反应速率
的平均反应速率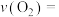
 时该反应的平衡常数
时该反应的平衡常数
(6)一定条件下在恒温恒容的密闭容器中按一定比例充入
 和
和 ,平衡时
,平衡时 的体积分数随
的体积分数随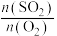 的变化如图B,则A、B、C三状态中,
的变化如图B,则A、B、C三状态中, 的转化率最小的是
的转化率最小的是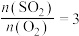 时,达到平衡状态
时,达到平衡状态 的体积分数可能是D、E、F三点中的
的体积分数可能是D、E、F三点中的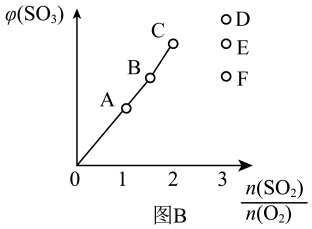
您最近半年使用:0次
解题方法
8 . CH3OH是一种绿色能源,也是一种化工原料。回答下列问题:
Ⅰ.合成甲醇。
工业上常用CO和H2制备CH3OH,反应原理是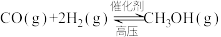
 。
。
(1)已知:①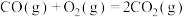
 kJ⋅mol
kJ⋅mol
②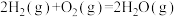
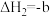 kJ⋅mol
kJ⋅mol
③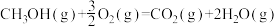
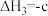 kJ⋅mol
kJ⋅mol
上述反应的
___________ kJ⋅mol (用含a、b、c的代数式表示)。
(用含a、b、c的代数式表示)。
(2)在恒温恒容密闭容器中充入1 mol 和1 mol
和1 mol  合成
合成 。下列情况表明该反应一定达到平衡状态的是___________(填字母)。
。下列情况表明该反应一定达到平衡状态的是___________(填字母)。
(3)向体积相同的甲、乙恒容密闭容器中均充入1 mol 和3 mol
和3 mol  同时发生反应合成
同时发生反应合成 ,相对甲,乙仅改变温度,测得甲醇的物质的量与时间的关系如图所示。
,相对甲,乙仅改变温度,测得甲醇的物质的量与时间的关系如图所示。___________ (填“高于”或“低于”)乙,判断依据是___________ 。
②
___________ (填“>”“<”或“=”)0,判断依据是___________ 。
③若容器体积为1 L,甲容器中0~4 min内用H2表示的平均反应速率为___________ mol⋅L ⋅min
⋅min 。
。
Ⅱ.可用于合成有机物。
近日,中国科学院大连化学物理研究所丁云杰团队利用Rh单核配合物催化剂以和CO为原料合成了CH3COOH,相关反应为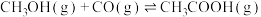 、
、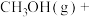
 。
。
(4)以CH3OH和CO为原料,从原子利用率分析,合成___________ (填“CH3COOH”或“CH3COOCH3”)是最理想的绿色化学工艺。
(5)一定温度下,总压强保持1.5a kPa,向反应器中充入1 mol 和1 mol
和1 mol  ,在一定条件下合成
,在一定条件下合成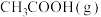 和
和 。达到平衡时,
。达到平衡时, 的转化率为60%,
的转化率为60%,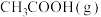 的选择性为80%,(
的选择性为80%,( 的选择性
的选择性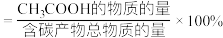 )。该温度下合成
)。该温度下合成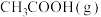 反应的平衡常数
反应的平衡常数
___________  (用含a的代数式表示,
(用含a的代数式表示, 为用分压表示的平衡常数,分压=总压×物质的量分数)。
为用分压表示的平衡常数,分压=总压×物质的量分数)。
Ⅰ.合成甲醇。
工业上常用CO和H2制备CH3OH,反应原理是
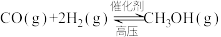
 。
。(1)已知:①
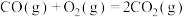
 kJ⋅mol
kJ⋅mol
②
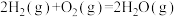
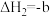 kJ⋅mol
kJ⋅mol
③
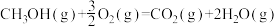
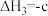 kJ⋅mol
kJ⋅mol
上述反应的

 (用含a、b、c的代数式表示)。
(用含a、b、c的代数式表示)。(2)在恒温恒容密闭容器中充入1 mol
 和1 mol
和1 mol  合成
合成 。下列情况表明该反应一定达到平衡状态的是___________(填字母)。
。下列情况表明该反应一定达到平衡状态的是___________(填字母)。| A.气体压强不随时间变化 | B.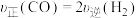 |
| C.气体密度不随时间变化 | D.气体平均摩尔质量不随时间变化 |
(3)向体积相同的甲、乙恒容密闭容器中均充入1 mol
 和3 mol
和3 mol  同时发生反应合成
同时发生反应合成 ,相对甲,乙仅改变温度,测得甲醇的物质的量与时间的关系如图所示。
,相对甲,乙仅改变温度,测得甲醇的物质的量与时间的关系如图所示。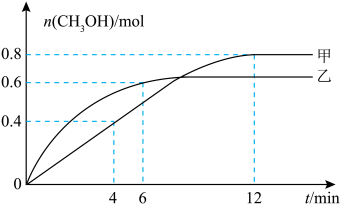
②

③若容器体积为1 L,甲容器中0~4 min内用H2表示的平均反应速率为
 ⋅min
⋅min 。
。Ⅱ.可用于合成有机物。
近日,中国科学院大连化学物理研究所丁云杰团队利用Rh单核配合物催化剂以和CO为原料合成了CH3COOH,相关反应为
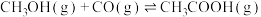 、
、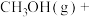
 。
。(4)以CH3OH和CO为原料,从原子利用率分析,合成
(5)一定温度下,总压强保持1.5a kPa,向反应器中充入1 mol
 和1 mol
和1 mol  ,在一定条件下合成
,在一定条件下合成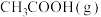 和
和 。达到平衡时,
。达到平衡时, 的转化率为60%,
的转化率为60%,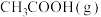 的选择性为80%,(
的选择性为80%,( 的选择性
的选择性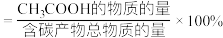 )。该温度下合成
)。该温度下合成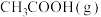 反应的平衡常数
反应的平衡常数
 (用含a的代数式表示,
(用含a的代数式表示, 为用分压表示的平衡常数,分压=总压×物质的量分数)。
为用分压表示的平衡常数,分压=总压×物质的量分数)。
您最近半年使用:0次
9 . 一定温度下,向恒容密闭容器中投入E和M发生如下反应:E(g)+M(g)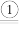 F(g)
F(g) G(g)。已知反应初始c0(E)=c0(M)=0.10mol/L,部分物质的浓度(c)随时间(t)的变化关系如图所示,t2后反应体系达到平衡状态。下列说法正确的是
G(g)。已知反应初始c0(E)=c0(M)=0.10mol/L,部分物质的浓度(c)随时间(t)的变化关系如图所示,t2后反应体系达到平衡状态。下列说法正确的是
 F(g)
F(g) G(g)。已知反应初始c0(E)=c0(M)=0.10mol/L,部分物质的浓度(c)随时间(t)的变化关系如图所示,t2后反应体系达到平衡状态。下列说法正确的是
G(g)。已知反应初始c0(E)=c0(M)=0.10mol/L,部分物质的浓度(c)随时间(t)的变化关系如图所示,t2后反应体系达到平衡状态。下列说法正确的是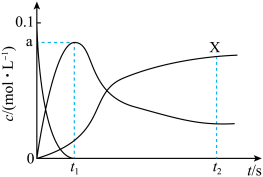
A.X为c(F)随 的变化曲线 的变化曲线 | B.0~t1内,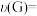 = = mol•L-1•s-1 mol•L-1•s-1 |
| C.反应的活化能:①>② | D.t2时,扩大容器的体积,n(F)减小 |
您最近半年使用:0次
名校
10 . 煤的间接液化是煤的综合利用的一种重要方法。首先是煤燃烧生成 ,再在钼系催化剂的催化作用下与
,再在钼系催化剂的催化作用下与 反应,最终生成
反应,最终生成 过程中主要发生如下反应:
过程中主要发生如下反应:
反应Ⅰ: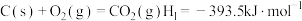
反应Ⅱ: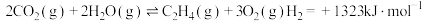
反应Ⅲ: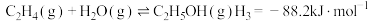
1.已知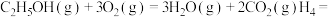
___________ 。
2.反应Ⅰ中属于共价化合物的电子式:___________ 。
为更好地研究煤的液化过程,某学习小组对反应Ⅱ进行了系统的研究。在一个 的恒容容器中加入
的恒容容器中加入 气体及
气体及 水蒸气,在
水蒸气,在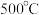 及钼系催化剂(固体)存在条件下只发生反应Ⅱ。
及钼系催化剂(固体)存在条件下只发生反应Ⅱ。
3.下列不能说明该反应已达到平衡状态的有___________(填标号)。
4.如图为四种组分的平衡时物质的量分数随温度的变化曲线。图中曲线 表示的物质是
表示的物质是___________ ,原因是___________ 。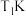 时,某同学在该容器中加入
时,某同学在该容器中加入 和
和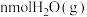 ,同时加入了
,同时加入了 和
和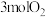 ,达到平衡后各组分体积分数仍与图中所示相同,则
,达到平衡后各组分体积分数仍与图中所示相同,则
___________ (用含 的代数式表示)。
的代数式表示)。
 ,再在钼系催化剂的催化作用下与
,再在钼系催化剂的催化作用下与 反应,最终生成
反应,最终生成 过程中主要发生如下反应:
过程中主要发生如下反应:反应Ⅰ:
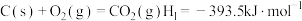
反应Ⅱ:
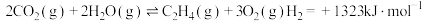
反应Ⅲ:
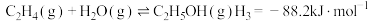
1.已知
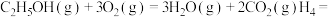
2.反应Ⅰ中属于共价化合物的电子式:
为更好地研究煤的液化过程,某学习小组对反应Ⅱ进行了系统的研究。在一个
 的恒容容器中加入
的恒容容器中加入 气体及
气体及 水蒸气,在
水蒸气,在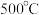 及钼系催化剂(固体)存在条件下只发生反应Ⅱ。
及钼系催化剂(固体)存在条件下只发生反应Ⅱ。3.下列不能说明该反应已达到平衡状态的有___________(填标号)。
A. 的体积分数不再改变 的体积分数不再改变 | B.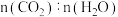 不再改变 不再改变 |
| C.容器的总压不再改变 | D.容器中气体的密度不再改变 |
 表示的物质是
表示的物质是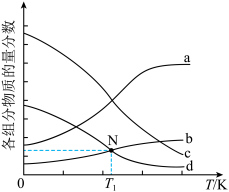
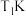 时,某同学在该容器中加入
时,某同学在该容器中加入 和
和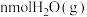 ,同时加入了
,同时加入了 和
和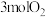 ,达到平衡后各组分体积分数仍与图中所示相同,则
,达到平衡后各组分体积分数仍与图中所示相同,则
 的代数式表示)。
的代数式表示)。
您最近半年使用:0次



