名校
解题方法
1 . 苯硫酚( )是一种医药中间体,可做麻醉剂,其工业制备原理如下。
)是一种医药中间体,可做麻醉剂,其工业制备原理如下。
主反应I: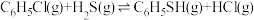
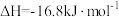
副反应Ⅱ: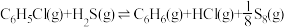

已知:① 的选择性
的选择性
②改变温度对热效应(吸收或释放)大的反应影响大
请回答下列问题:
(1)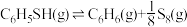 的活化能
的活化能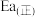
___________ 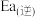 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
恒温恒容条件下,该分解反应达平衡时,减小反应物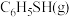 浓度,再次达平衡时,
浓度,再次达平衡时, 的转化率
的转化率___________ (填“增大”、“减小”或“不变”)。
(2)工业制备苯硫酚的反应常在高压容器内进行,该措施的优点有___________ (写出两点)
(3) 时向恒容密闭容器中充入等物质的量的
时向恒容密闭容器中充入等物质的量的 和
和 ,只发生上述主、副反应。反应达到平衡时
,只发生上述主、副反应。反应达到平衡时 的体积分数为m,
的体积分数为m, 的体积分数为n。
的体积分数为n。
①下列有关上述过程说法正确的是___________ 。
A.已知主反应 ,则该反应在高温下自发进行
,则该反应在高温下自发进行
B.平衡时 的选择性为
的选择性为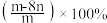
C.平衡时正反应速率: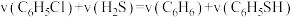
D.升高体系的温度,达新平衡后 比值变大
比值变大
② 时,主反应的压强平衡常数
时,主反应的压强平衡常数
___________ (用含m、n的代数式表示)
③上述条件下,实验测得 和
和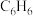 的产率在相同时间内随温度的变化如图所示。在温度高于
的产率在相同时间内随温度的变化如图所示。在温度高于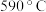 时两种产物的产率呈现图中变化趋势的原因是
时两种产物的产率呈现图中变化趋势的原因是___________ ;
由此可知主反应I和副反应Ⅱ的活化能大小为: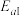
___________  (填写“>”、“<”或=)。
(填写“>”、“<”或=)。
 )是一种医药中间体,可做麻醉剂,其工业制备原理如下。
)是一种医药中间体,可做麻醉剂,其工业制备原理如下。主反应I:
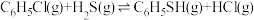
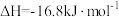
副反应Ⅱ:
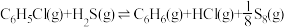

已知:①
 的选择性
的选择性
②改变温度对热效应(吸收或释放)大的反应影响大
请回答下列问题:
(1)
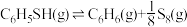 的活化能
的活化能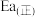
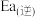 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。恒温恒容条件下,该分解反应达平衡时,减小反应物
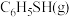 浓度,再次达平衡时,
浓度,再次达平衡时, 的转化率
的转化率(2)工业制备苯硫酚的反应常在高压容器内进行,该措施的优点有
(3)
 时向恒容密闭容器中充入等物质的量的
时向恒容密闭容器中充入等物质的量的 和
和 ,只发生上述主、副反应。反应达到平衡时
,只发生上述主、副反应。反应达到平衡时 的体积分数为m,
的体积分数为m, 的体积分数为n。
的体积分数为n。①下列有关上述过程说法正确的是
A.已知主反应
 ,则该反应在高温下自发进行
,则该反应在高温下自发进行B.平衡时
 的选择性为
的选择性为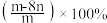
C.平衡时正反应速率:
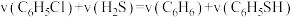
D.升高体系的温度,达新平衡后
 比值变大
比值变大②
 时,主反应的压强平衡常数
时,主反应的压强平衡常数
③上述条件下,实验测得
 和
和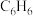 的产率在相同时间内随温度的变化如图所示。在温度高于
的产率在相同时间内随温度的变化如图所示。在温度高于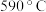 时两种产物的产率呈现图中变化趋势的原因是
时两种产物的产率呈现图中变化趋势的原因是由此可知主反应I和副反应Ⅱ的活化能大小为:
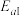
 (填写“>”、“<”或=)。
(填写“>”、“<”或=)。
您最近一年使用:0次
解题方法
2 . 甲醇是重要的化工原料,应用前景广阔。工业上一般采用以下方法合成:
(1)反应Ⅰ:
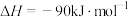
反应Ⅱ:

则反应Ⅲ: 的
的
________ 
(2)在催化剂M的作用下,反应Ⅱ的微观反应历程和相对能量(E)如下表所示,其中吸附在催化剂表面上的物种用“*”标注。已知;●表示C,·表示O,○表示H。
①历程c对应的反应________ 。
②决定反应Ⅱ总反应速率的是历程________ (填“a”、“b”或“c”)。
(3)将 和
和 按物质的量之比1:3充入一恒容密闭容器中
按物质的量之比1:3充入一恒容密闭容器中
①若只发生反应Ⅲ,下列叙述能说明该反应达到平衡状态的是________ 。
A. 和
和 的转化率相等
的转化率相等
B.生成3molO-H键的同时生成3molH-H键
C. 时
时
D.混合气体的密度保持不变
②若同时发生反应Ⅱ和反应Ⅲ,测得 的平衡转化率随温度、压强变化的情况如图所示。
的平衡转化率随温度、压强变化的情况如图所示。 、
、 、
、 的大小关系为
的大小关系为________ 。
ii.A点、B点的化学反应速率大小: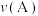
________  (填“<”、“=”或“>”)。
(填“<”、“=”或“>”)。
③图中M点对应的温度下,已知CO的选择性(生成的CO与转化的 的百分比)为50%,该温度下反应Ⅱ的平衡常数为
的百分比)为50%,该温度下反应Ⅱ的平衡常数为________ (结果保留3位小数)。
(1)反应Ⅰ:

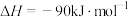
反应Ⅱ:


则反应Ⅲ:
 的
的

(2)在催化剂M的作用下,反应Ⅱ的微观反应历程和相对能量(E)如下表所示,其中吸附在催化剂表面上的物种用“*”标注。已知;●表示C,·表示O,○表示H。
历程 | 反应 |
历程a |
|
历程b
|
|
历程c | ________ |
②决定反应Ⅱ总反应速率的是历程
(3)将
 和
和 按物质的量之比1:3充入一恒容密闭容器中
按物质的量之比1:3充入一恒容密闭容器中①若只发生反应Ⅲ,下列叙述能说明该反应达到平衡状态的是
A.
 和
和 的转化率相等
的转化率相等B.生成3molO-H键的同时生成3molH-H键
C.
 时
时D.混合气体的密度保持不变
②若同时发生反应Ⅱ和反应Ⅲ,测得
 的平衡转化率随温度、压强变化的情况如图所示。
的平衡转化率随温度、压强变化的情况如图所示。
 、
、 、
、 的大小关系为
的大小关系为ii.A点、B点的化学反应速率大小:
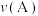
 (填“<”、“=”或“>”)。
(填“<”、“=”或“>”)。③图中M点对应的温度下,已知CO的选择性(生成的CO与转化的
 的百分比)为50%,该温度下反应Ⅱ的平衡常数为
的百分比)为50%,该温度下反应Ⅱ的平衡常数为
您最近一年使用:0次
名校
解题方法
3 . 我国科学家根据 在HZSM-5载体上的单层分散行为设计催化剂用于
在HZSM-5载体上的单层分散行为设计催化剂用于 选择性还原
选择性还原 。回答下列问题:
。回答下列问题:
已知:①
 kJ⋅mol
kJ⋅mol (
( )
)
②
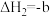 kJ⋅mol
kJ⋅mol (
( )
)
(1)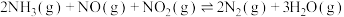

______ kJ⋅mol 。
。
(2)向恒容密闭容器中充入0.4 mol 和0.6 mol
和0.6 mol ,只发生反应①。下列叙述正确的是______(填标号)。
,只发生反应①。下列叙述正确的是______(填标号)。
(3)一定温度下,起始投料不变,单位时间内氮氧化物转化率、表面活泼氧量比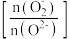 与催化剂组成类型的关系如下图所示。催化效能最佳的催化剂组成是
与催化剂组成类型的关系如下图所示。催化效能最佳的催化剂组成是______ (填具体催化剂名称)。 、2 mol
、2 mol  和4 mol
和4 mol  ,在不同组成的催化剂作用下,单位时间内氮氧化物的转化率与温度的关系如下图所示。
,在不同组成的催化剂作用下,单位时间内氮氧化物的转化率与温度的关系如下图所示。______ 。
②a→b段氮氧化物转化率变化的原因是____________ 。
③M点反应______ (填“达到”或“未达到”)平衡状态,判断依据是______ ,M→N段氮氧化物转化率变化的原因可能是____________ 。
(5)一定温度下,向体积为1 L的恒容密闭容器中充入1 mol 和2 mol
和2 mol ,在催化剂作用下发生反应:①
,在催化剂作用下发生反应:① :②
:②
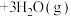 达到平衡时,NO转化率为70%,
达到平衡时,NO转化率为70%, 的选择性为50%[
的选择性为50%[ 的选择性
的选择性 ]该温度下,反应①的平衡常数
]该温度下,反应①的平衡常数
______ mol·L (列出计算式即可)。
(列出计算式即可)。
 在HZSM-5载体上的单层分散行为设计催化剂用于
在HZSM-5载体上的单层分散行为设计催化剂用于 选择性还原
选择性还原 。回答下列问题:
。回答下列问题:已知:①

 kJ⋅mol
kJ⋅mol (
( )
)②

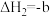 kJ⋅mol
kJ⋅mol (
( )
)(1)
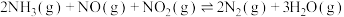

 。
。(2)向恒容密闭容器中充入0.4 mol
 和0.6 mol
和0.6 mol ,只发生反应①。下列叙述正确的是______(填标号)。
,只发生反应①。下列叙述正确的是______(填标号)。| A.恒温条件下,压强不随时间变化时反应达到平衡状态 |
B.平衡时温度不变,再充入1 mol  时平衡常数减小 时平衡常数减小 |
| C.反应达到平衡时放出的热量为0.1a kJ |
| D.加入高效催化剂,反应达到平衡时NO的转化率增大 |
(3)一定温度下,起始投料不变,单位时间内氮氧化物转化率、表面活泼氧量比
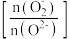 与催化剂组成类型的关系如下图所示。催化效能最佳的催化剂组成是
与催化剂组成类型的关系如下图所示。催化效能最佳的催化剂组成是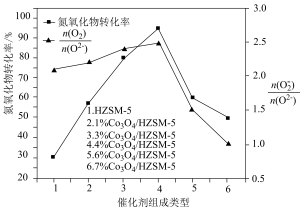
 、2 mol
、2 mol  和4 mol
和4 mol  ,在不同组成的催化剂作用下,单位时间内氮氧化物的转化率与温度的关系如下图所示。
,在不同组成的催化剂作用下,单位时间内氮氧化物的转化率与温度的关系如下图所示。
②a→b段氮氧化物转化率变化的原因是
③M点反应
(5)一定温度下,向体积为1 L的恒容密闭容器中充入1 mol
 和2 mol
和2 mol ,在催化剂作用下发生反应:①
,在催化剂作用下发生反应:① :②
:②
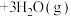 达到平衡时,NO转化率为70%,
达到平衡时,NO转化率为70%, 的选择性为50%[
的选择性为50%[ 的选择性
的选择性 ]该温度下,反应①的平衡常数
]该温度下,反应①的平衡常数
 (列出计算式即可)。
(列出计算式即可)。
您最近一年使用:0次
2024-05-06更新
|
496次组卷
|
2卷引用:2024届辽宁省抚顺市六校协作体高三下学期第三次模拟化学试卷
解题方法
4 . 一定压强下,向 密闭容器中充入
密闭容器中充入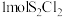 和
和 ,发生反应
,发生反应 。
。 与
与 的消耗速率
的消耗速率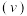 与温度
与温度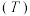 的关系如图,下列说法正确的是
的关系如图,下列说法正确的是
 密闭容器中充入
密闭容器中充入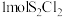 和
和 ,发生反应
,发生反应 。
。 与
与 的消耗速率
的消耗速率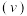 与温度
与温度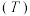 的关系如图,下列说法正确的是
的关系如图,下列说法正确的是
A. 四点中只有 四点中只有 点达到平衡状态 点达到平衡状态 |
| B.正反应的活化能小于逆反应的活化能 |
C.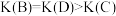 |
D. ,反应达平衡后缩小容器体积,各物质浓度不变 ,反应达平衡后缩小容器体积,各物质浓度不变 |
您最近一年使用:0次
5 . 反应N2(g)+3H2(g)  2NH3(g) ΔH<0,若在恒压绝热的容器中发生,下列选项表明一定已达平衡状态的是
2NH3(g) ΔH<0,若在恒压绝热的容器中发生,下列选项表明一定已达平衡状态的是
 2NH3(g) ΔH<0,若在恒压绝热的容器中发生,下列选项表明一定已达平衡状态的是
2NH3(g) ΔH<0,若在恒压绝热的容器中发生,下列选项表明一定已达平衡状态的是| A.容器内的温度不再变化 |
| B.容器内的压强不再变化 |
| C.相同时间内,断开H-H键的数目和生成N-H键的数目之比1:1 |
| D.容器内气体的浓度c(N2):c(H2):c(NH3)=1:3:2 |
您最近一年使用:0次
名校
6 . 乙烯的产量是衡量一个国家石油化工发展水平的重要标志。一定条件下 和
和 合成乙烯的反应为
合成乙烯的反应为 。向1L恒容密闭容器中充入1mol
。向1L恒容密闭容器中充入1mol  和3mol
和3mol  ,测得不同温度下
,测得不同温度下 的平衡转化率及催化剂的催化效率如题图所示。下列说法正确的是
的平衡转化率及催化剂的催化效率如题图所示。下列说法正确的是
 和
和 合成乙烯的反应为
合成乙烯的反应为 。向1L恒容密闭容器中充入1mol
。向1L恒容密闭容器中充入1mol  和3mol
和3mol  ,测得不同温度下
,测得不同温度下 的平衡转化率及催化剂的催化效率如题图所示。下列说法正确的是
的平衡转化率及催化剂的催化效率如题图所示。下列说法正确的是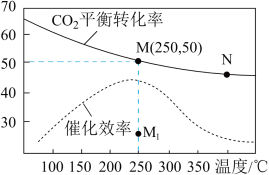
| A.升高温度,平衡向逆反应方向移动,催化剂的催化效率降低 |
| B.图中M点乙烯的体积分数约为7.7% |
C.250℃时,当 的转化率位于 的转化率位于 点时,保持其他条件不变,仅延长反应时间不可能使转化率达到50% 点时,保持其他条件不变,仅延长反应时间不可能使转化率达到50% |
D.向N点的平衡体系中充入1mol  和3mol 和3mol  ,其他条件不变,再次达到平衡时, ,其他条件不变,再次达到平衡时, 增大 增大 |
您最近一年使用:0次
7 . 下列实验根据现象得出相应结论不正确的是
| 选项 | 实验 | 现象 | |
| A | 取少量乙酰水杨酸样品,加入3mL蒸馏水和少量乙醇,振荡,再加入1~2滴 |溶液 |溶液 | 呈紫色溶液 | 乙酰水杨酸样品中含有水杨酸 |
| B | 在25℃和50℃时,分别测量0.1  溶液的pH 溶液的pH | 升高温度,溶液的pH下降 | pH变化是 的改变与水解平衡移动共同作用的结果 的改变与水解平衡移动共同作用的结果 |
| C | 将石油裂解产生的气体通入 的 的 溶液 溶液 | 溶液褪色 | 石油裂解产物中含乙烯 |
| D | 室温下,取1mL 0.1 KI溶液和1mL 0.1 KI溶液和1mL 0.1  溶液充分反应后,再加2mL 溶液充分反应后,再加2mL  振荡、静置后,取上层清液滴加少色量KSCN溶液 振荡、静置后,取上层清液滴加少色量KSCN溶液 | 溶液变成红色 |  和 和 的反应有一定的限度 的反应有一定的限度 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
8 . 在2L密闭容器中进行反应: ,式中a、b、c、d为化学计量数。在
,式中a、b、c、d为化学计量数。在 内,各物质的物质的量(单位为mol)的变化如下表所示:
内,各物质的物质的量(单位为mol)的变化如下表所示:
已知2min内 ,
,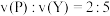 。
。
(1)起始时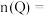
___________ ,2min末是否达到平衡___________ (填“是”或“否”)。
(2)上述反应的化学方程式为___________ 。
(3)下列各项为1min内各物质所表示的反应速率,其中最快的是___________ 。
a. b.
b. c.
c.
(4)用Y表示2min内的反应速率为___________ 。2min末,Q在混合气体中的体积分数为___________ 。
(5)在保持绝热和容积不变的情况下,下列关于上述反应的叙述不正确的是___________ 。
a.向容器内加入固体X,会使反应速率明显提高
b.向容器内充入稀有气体Ar(不参与反应),会导致体系压强增大,反应速率加快
c.随着反应的进行,混合气体的平均相对分子质量不再改变即说明反应已经达到平衡
d.随着反应的进行,混合气体的密度不再改变即说明反应已经达到平衡
e.随着反应的进行,混合气体的压强不再改变即说明反应已经达到平衡
 ,式中a、b、c、d为化学计量数。在
,式中a、b、c、d为化学计量数。在 内,各物质的物质的量(单位为mol)的变化如下表所示:
内,各物质的物质的量(单位为mol)的变化如下表所示:| 物质 时间 | X | Y | P | Q |
| 起始 | 0.5 | 2.2 | 1.0 | |
| 2min末 | 0.7 | 2.7 | 1.2 | |
| 3min末 | 0.8 |
 ,
,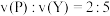 。
。(1)起始时
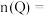
(2)上述反应的化学方程式为
(3)下列各项为1min内各物质所表示的反应速率,其中最快的是
a.
 b.
b. c.
c.
(4)用Y表示2min内的反应速率为
(5)在保持绝热和容积不变的情况下,下列关于上述反应的叙述不正确的是
a.向容器内加入固体X,会使反应速率明显提高
b.向容器内充入稀有气体Ar(不参与反应),会导致体系压强增大,反应速率加快
c.随着反应的进行,混合气体的平均相对分子质量不再改变即说明反应已经达到平衡
d.随着反应的进行,混合气体的密度不再改变即说明反应已经达到平衡
e.随着反应的进行,混合气体的压强不再改变即说明反应已经达到平衡
您最近一年使用:0次
名校
解题方法
9 . 一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇: ,分别在300℃和500℃下生成甲醇的量如图所示。根据图像,计算在500℃时,从反应开始到平衡的氢气的平均反应速率为
,分别在300℃和500℃下生成甲醇的量如图所示。根据图像,计算在500℃时,从反应开始到平衡的氢气的平均反应速率为
 ,分别在300℃和500℃下生成甲醇的量如图所示。根据图像,计算在500℃时,从反应开始到平衡的氢气的平均反应速率为
,分别在300℃和500℃下生成甲醇的量如图所示。根据图像,计算在500℃时,从反应开始到平衡的氢气的平均反应速率为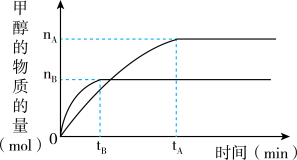
A.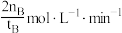 | B. | C. | D.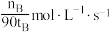 |
您最近一年使用:0次
名校
10 . 利用间接转化法可将氮氧化物转化为化工产品以实现氮氧化物的充分利用。
已知①
②
③
若某温度下,向VL密闭容器中加入2molNO和2molICl发生上述反应,达平衡时容器中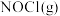 为amol,
为amol, 为bmol。下列说法不正确的是
为bmol。下列说法不正确的是
已知①

②

③

若某温度下,向VL密闭容器中加入2molNO和2molICl发生上述反应,达平衡时容器中
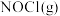 为amol,
为amol, 为bmol。下列说法不正确的是
为bmol。下列说法不正确的是A.此时 的浓度为 的浓度为 |
| B.若该密闭容器中气体颜色保持不变,说明各反应已达平衡状态 |
C.NO转化率为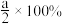 |
| D.若反应①②为吸热反应,③为放热反应,则升高温度①、②速率增大,③速率减小 |
您最近一年使用:0次