解题方法
1 . 下列叙述正确的是
A.恒容容器中发生反应N2(g)+O2(g)  2NO(g),若平衡后在容器中充入He,正、逆反应的速率均不变 2NO(g),若平衡后在容器中充入He,正、逆反应的速率均不变 |
B.当一定量的锌粉和过量的6 盐酸反应时,为了减慢反应速率,又不影响产生 盐酸反应时,为了减慢反应速率,又不影响产生 的总量,可向反应器中加入一些水、 的总量,可向反应器中加入一些水、 溶液或 溶液或 溶液 溶液 |
C.已知反应:CaCO3(s)  CaO(s)+CO2(g),在密闭的反应炉内达到平衡后,若其他条件均不改变,将反应炉体积缩小一半,则达到新平衡时CO2(g)的浓度将升高至原来的2倍 CaO(s)+CO2(g),在密闭的反应炉内达到平衡后,若其他条件均不改变,将反应炉体积缩小一半,则达到新平衡时CO2(g)的浓度将升高至原来的2倍 |
D.在一定温度下,容积一定的密闭容器中的反应A(s)+2B(g) C(g)+D(g),当混合气体的总压强不变时,则表明该反应已达平衡状态 C(g)+D(g),当混合气体的总压强不变时,则表明该反应已达平衡状态 |
您最近一年使用:0次
名校
解题方法
2 . 向绝热恒容密闭容器中通入 和
和 ,一定条件下使反应
,一定条件下使反应 达到平衡,正反应速率随时间变化的示意图如下所示。下列叙述不正确的是
达到平衡,正反应速率随时间变化的示意图如下所示。下列叙述不正确的是
 和
和 ,一定条件下使反应
,一定条件下使反应 达到平衡,正反应速率随时间变化的示意图如下所示。下列叙述不正确的是
达到平衡,正反应速率随时间变化的示意图如下所示。下列叙述不正确的是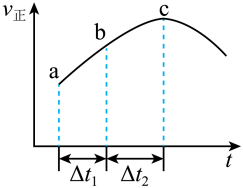
| A.反应在c点未达到平衡状态 |
| B.反应物浓度:c点大于b点 |
| C.反应物的总能量高于生成物的总能量 |
D. 时, 时, 的转化率:a~b段小于b~c段 的转化率:a~b段小于b~c段 |
您最近一年使用:0次
名校
解题方法
3 . 在2L密闭容器中进行反应: ,式中a、b、c、d为化学计量数。在
,式中a、b、c、d为化学计量数。在 内,各物质的物质的量(单位为mol)的变化如下表所示:
内,各物质的物质的量(单位为mol)的变化如下表所示:
已知2min内 ,
,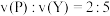 。
。
(1)起始时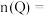
___________ ,2min末是否达到平衡___________ (填“是”或“否”)。
(2)上述反应的化学方程式为___________ 。
(3)下列各项为1min内各物质所表示的反应速率,其中最快的是___________ 。
a. b.
b. c.
c.
(4)用Y表示2min内的反应速率为___________ 。2min末,Q在混合气体中的体积分数为___________ 。
(5)在保持绝热和容积不变的情况下,下列关于上述反应的叙述不正确的是___________ 。
a.向容器内加入固体X,会使反应速率明显提高
b.向容器内充入稀有气体Ar(不参与反应),会导致体系压强增大,反应速率加快
c.随着反应的进行,混合气体的平均相对分子质量不再改变即说明反应已经达到平衡
d.随着反应的进行,混合气体的密度不再改变即说明反应已经达到平衡
e.随着反应的进行,混合气体的压强不再改变即说明反应已经达到平衡
 ,式中a、b、c、d为化学计量数。在
,式中a、b、c、d为化学计量数。在 内,各物质的物质的量(单位为mol)的变化如下表所示:
内,各物质的物质的量(单位为mol)的变化如下表所示:| 物质 时间 | X | Y | P | Q |
| 起始 | 0.5 | 2.2 | 1.0 | |
| 2min末 | 0.7 | 2.7 | 1.2 | |
| 3min末 | 0.8 |
 ,
,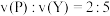 。
。(1)起始时
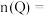
(2)上述反应的化学方程式为
(3)下列各项为1min内各物质所表示的反应速率,其中最快的是
a.
 b.
b. c.
c.
(4)用Y表示2min内的反应速率为
(5)在保持绝热和容积不变的情况下,下列关于上述反应的叙述不正确的是
a.向容器内加入固体X,会使反应速率明显提高
b.向容器内充入稀有气体Ar(不参与反应),会导致体系压强增大,反应速率加快
c.随着反应的进行,混合气体的平均相对分子质量不再改变即说明反应已经达到平衡
d.随着反应的进行,混合气体的密度不再改变即说明反应已经达到平衡
e.随着反应的进行,混合气体的压强不再改变即说明反应已经达到平衡
您最近一年使用:0次
名校
解题方法
4 . 一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇: ,分别在300℃和500℃下生成甲醇的量如图所示。根据图像,计算在500℃时,从反应开始到平衡的氢气的平均反应速率为
,分别在300℃和500℃下生成甲醇的量如图所示。根据图像,计算在500℃时,从反应开始到平衡的氢气的平均反应速率为
 ,分别在300℃和500℃下生成甲醇的量如图所示。根据图像,计算在500℃时,从反应开始到平衡的氢气的平均反应速率为
,分别在300℃和500℃下生成甲醇的量如图所示。根据图像,计算在500℃时,从反应开始到平衡的氢气的平均反应速率为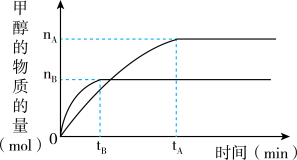
A.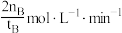 | B. | C. | D.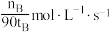 |
您最近一年使用:0次
名校
5 . 利用间接转化法可将氮氧化物转化为化工产品以实现氮氧化物的充分利用。
已知①
②
③
若某温度下,向VL密闭容器中加入2molNO和2molICl发生上述反应,达平衡时容器中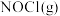 为amol,
为amol, 为bmol。下列说法不正确的是
为bmol。下列说法不正确的是
已知①

②

③

若某温度下,向VL密闭容器中加入2molNO和2molICl发生上述反应,达平衡时容器中
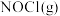 为amol,
为amol, 为bmol。下列说法不正确的是
为bmol。下列说法不正确的是A.此时 的浓度为 的浓度为 |
| B.若该密闭容器中气体颜色保持不变,说明各反应已达平衡状态 |
C.NO转化率为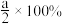 |
| D.若反应①②为吸热反应,③为放热反应,则升高温度①、②速率增大,③速率减小 |
您最近一年使用:0次
名校
解题方法
6 . I.汽车尾气中含有CO、NO等有害气体,某新型催化剂能促使NO、CO转化为两种无毒气体。T ℃时,将0.8 mol NO和0.8 mol CO充入容积为2 L的密闭容器中,模拟汽车尾气转化,容器中NO的物质的量随时间变化如图所示。___________ 。
(2)反应开始至10 min,v(NO)=___________ mol/(L·min)。
(3)下列说法正确的是___________ 。
a.新型催化剂可以加快NO、CO的转化
b.该反应进行到10 min时达到化学平衡状态
c.平衡时CO的浓度是0.4 mol/L
Ⅱ.在恒温下,将4mol的H2(g)和2mol的CO(g)充入1L恒容的密闭容器中发生如下反应:CO(g) + 2H2(g) CH3OH(g)。下图是CO(g)和 CH3OH(g)的浓度随时间变化的关系图,
CH3OH(g)。下图是CO(g)和 CH3OH(g)的浓度随时间变化的关系图,
(4)0-5min内,H2 (g)的平均反应速率是___________ mol/(L·min)。
(5)12min时,v正___________ v逆(填“>”“<”或“=”)。
(6)设起始压强为P,平衡时压强为P0,则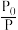 的值为
的值为___________ 。
(7)根据反应原理下列描述能说明反应达到最大限度的是___________。
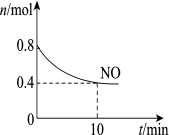
(2)反应开始至10 min,v(NO)=
(3)下列说法正确的是
a.新型催化剂可以加快NO、CO的转化
b.该反应进行到10 min时达到化学平衡状态
c.平衡时CO的浓度是0.4 mol/L
Ⅱ.在恒温下,将4mol的H2(g)和2mol的CO(g)充入1L恒容的密闭容器中发生如下反应:CO(g) + 2H2(g)
 CH3OH(g)。下图是CO(g)和 CH3OH(g)的浓度随时间变化的关系图,
CH3OH(g)。下图是CO(g)和 CH3OH(g)的浓度随时间变化的关系图,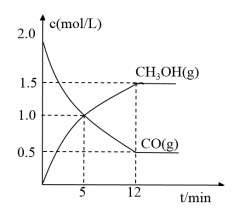
(4)0-5min内,H2 (g)的平均反应速率是
(5)12min时,v正
(6)设起始压强为P,平衡时压强为P0,则
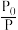 的值为
的值为(7)根据反应原理下列描述能说明反应达到最大限度的是___________。
| A.CO(g)、H2(g)、CH3OH(g)的物质的量比为1∶2∶1 |
| B.混合气体的压强不随时间的变化而改变 |
| C.单位时间内每消耗2amolH2(g),同时生成amolCH3OH(g) |
| D.反应速率:v(H2)=2v(CO) |
您最近一年使用:0次
2024-03-17更新
|
1024次组卷
|
3卷引用:重难点04 化学反应速率及平衡图像问题的分析-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(辽宁专用)
(已下线)重难点04 化学反应速率及平衡图像问题的分析-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(辽宁专用)湖南省邵阳市绥宁县第一中2022-2023学年高一下学期期末考试化学试题名校期末好题汇编-化学反应与能量(非选择题)
解题方法
7 . Ⅰ.为了探究化学反应的热效应,某兴趣小组进行了如下实验:

(1)如图a所示,室温下,观察到甲处液面上升,乙处液面下降,则该反应是___________ (填“放热”或“吸热”)反应,写出该反应的化学方程式:___________ 。
(2)如图b所示,室温下,把装有固体A的试管放入盛有饱和澄清石灰水的烧杯中,向该试管中滴入一定量的液体B,观察到烧杯中的饱和澄清石灰水变浑浊,则该反应是___________ (填“放热”或“吸热”)反应,写出一个符合该条件的化学方程式:___________ 。
(3)如图c所示,室温下,通过仪器丙向仪器丁中的一定浓度的盐酸中加入一定浓度的氢氧化钠溶液,仪器丙的名称为___________ 。
Ⅱ.
(4)在一定温度下,容积为1 L的恒容密闭容器中某一反应中所涉及的物质仅有M、N,其物质的量随反应时间变化的曲线如图所示。下列表述中错误的是___________ 。
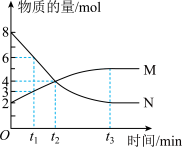
A.该反应的化学方程式为2N(g)⇌M(g)
B.0~t2,该反应的平均反应速率v(N)=4 mol•L-1•min-1
C.t3时,反应达到平衡
D.t1时,N的浓度是M的2倍
E.t3时,反应停止
Ⅲ.
(5)铜锌原电池是人类最早研究的化学电源之一,其简易装置如图所示,可观察到的现象是锌片溶解,铜片表面产生气泡,电流计指针偏向铜电极,根据上述原理,以下各种原电池的分析正确的是___________ 。
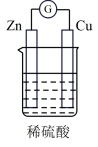

(1)如图a所示,室温下,观察到甲处液面上升,乙处液面下降,则该反应是
(2)如图b所示,室温下,把装有固体A的试管放入盛有饱和澄清石灰水的烧杯中,向该试管中滴入一定量的液体B,观察到烧杯中的饱和澄清石灰水变浑浊,则该反应是
(3)如图c所示,室温下,通过仪器丙向仪器丁中的一定浓度的盐酸中加入一定浓度的氢氧化钠溶液,仪器丙的名称为
Ⅱ.
(4)在一定温度下,容积为1 L的恒容密闭容器中某一反应中所涉及的物质仅有M、N,其物质的量随反应时间变化的曲线如图所示。下列表述中错误的是

A.该反应的化学方程式为2N(g)⇌M(g)
B.0~t2,该反应的平均反应速率v(N)=4 mol•L-1•min-1
C.t3时,反应达到平衡
D.t1时,N的浓度是M的2倍
E.t3时,反应停止
Ⅲ.
(5)铜锌原电池是人类最早研究的化学电源之一,其简易装置如图所示,可观察到的现象是锌片溶解,铜片表面产生气泡,电流计指针偏向铜电极,根据上述原理,以下各种原电池的分析正确的是

| 选项 | A | B | C | D |
| 装置 | 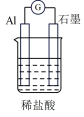 |  | 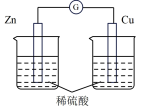 | 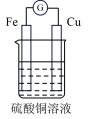 |
| 分析 | Al电极为负极,H+在该极发生还原反应 | 电流计指针偏向Al,溶液中的OH-移向Mg电极 | 电流由Cu电极流向Zn电极,Cu片表面产生气泡 | 电子由Fe电极流向Cu电极,Fe发生氧化反应 |
您最近一年使用:0次
解题方法
8 . 甲醇( )既是重要的化工原料,也是性能优良的能源,利用
)既是重要的化工原料,也是性能优良的能源,利用 生产甲醇是实现“碳中和”的重要途径之一。在体积为2L的恒容密闭容器中,充入1.0mol
生产甲醇是实现“碳中和”的重要途径之一。在体积为2L的恒容密闭容器中,充入1.0mol  和3.0mol
和3.0mol  ,一定条件下发生反应
,一定条件下发生反应 ,测得
,测得 和
和 的物质的量随时间的变化如图所示。
的物质的量随时间的变化如图所示。_______ 逆反应速率(填“>”“<”或“=”,下同),t=15 min时,正反应速率_______ 逆反应速率。
(2)反应达到平衡时,消耗 的物质的量为
的物质的量为_______ mol, 的转化率为
的转化率为_______ , 的体积分数为
的体积分数为_______ 。
(3)下列事实能说明该反应达到平衡状态的是_______(填字母)。
(4)若其他条件不变,反应开始充入2 mol氦气,反应达到最大限度所需时间t_______ 10 min(填“>”“<”或“=”)。
 )既是重要的化工原料,也是性能优良的能源,利用
)既是重要的化工原料,也是性能优良的能源,利用 生产甲醇是实现“碳中和”的重要途径之一。在体积为2L的恒容密闭容器中,充入1.0mol
生产甲醇是实现“碳中和”的重要途径之一。在体积为2L的恒容密闭容器中,充入1.0mol  和3.0mol
和3.0mol  ,一定条件下发生反应
,一定条件下发生反应 ,测得
,测得 和
和 的物质的量随时间的变化如图所示。
的物质的量随时间的变化如图所示。
(2)反应达到平衡时,消耗
 的物质的量为
的物质的量为 的转化率为
的转化率为 的体积分数为
的体积分数为(3)下列事实能说明该反应达到平衡状态的是_______(填字母)。
A.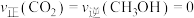 | B.体系压强不再变化 |
| C.容器内气体的密度不再变化 | D.容器内混合气体的平均摩尔质量不再变化 |
(4)若其他条件不变,反应开始充入2 mol氦气,反应达到最大限度所需时间t
您最近一年使用:0次
名校
9 . 下列说法正确的是(设NA为阿伏加德罗常数的值)
| A.向5 mL 0.1 mol·L-1 FeCl3溶液中滴入0.1 mol·L-1 KI溶液5~6滴,加2 mL CCl4振荡,静置后取上层清液滴加KSCN溶液,溶液变红,说明Fe3+与I-的反应有一定限度 |
| B.32g Cu与足量硫黄加热后反应,转移的电子数为NA |
| C.标准状况下,11.2L CO2和SO2的混合气体中含有的氧原子数为NA |
| D.已知N2(g)和H2(g)反应生成2 mol NH3(g)时放出的热量为Q kJ,那么1 mol N2(g) 和3 mol H2(g)在适宜的条件下混合后发生反应生成NH3(g)时,放出的热量为Q kJ |
您最近一年使用:0次
名校
10 . 2 L恒容密闭容器中通入A、B各10 mol,在一定温度下进行反应:3A(g)+B(g)⇌2C(g)+2D(s),ΔH<0,4 min时达到平衡,生成4 mol D。下列说法不正确的是
| A.①体系气体密度不变;②A的体积分数不变;③2v逆(A)=3v正(C),三种现象均可以说明该反应达到平衡 |
| B.①增加D的质量;②向体系中充入He;③抽出A减小体系压强,三种操作都不能增大逆反应速率 |
| C.4 min末时,C的平均反应速率为0.5 mol·L-1·min-1 |
| D.保持温度不变,起始时四种物质的物质的量均为6 mol,则此时反应v正(A) < v逆(A) |
您最近一年使用:0次



