名校
解题方法
1 . 相同温度下,有恒容密闭容器 和恒压密闭容器
和恒压密闭容器 ,两容器中均充入
,两容器中均充入 和
和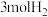 ,此时两容器的体积相等。在一定条件下反应达到平衡状态,
,此时两容器的体积相等。在一定条件下反应达到平衡状态, 中
中 的体积分数为
的体积分数为 ,放出热量
,放出热量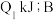 中
中 的体积分数为
的体积分数为 ,放出热量
,放出热量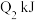 。
。
已知: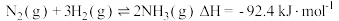
则:a___________ b (填选项), 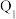
___________  ,
,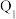
___________ 92.4(填选项)。
A B.
B. C.
C.
 和恒压密闭容器
和恒压密闭容器 ,两容器中均充入
,两容器中均充入 和
和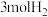 ,此时两容器的体积相等。在一定条件下反应达到平衡状态,
,此时两容器的体积相等。在一定条件下反应达到平衡状态, 中
中 的体积分数为
的体积分数为 ,放出热量
,放出热量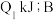 中
中 的体积分数为
的体积分数为 ,放出热量
,放出热量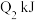 。
。已知:
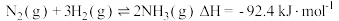
则:a
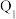
 ,
,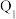
A
 B.
B. C.
C.
您最近半年使用:0次
2 . 用 和
和  在催化剂的作用下合成甲醇,发生的反应如下:
在催化剂的作用下合成甲醇,发生的反应如下: 。在体积一定的密闭容器中按物质的量之比
。在体积一定的密闭容器中按物质的量之比  充入
充入  和
和  ,测得平衡混合物中
,测得平衡混合物中  的体积分数在不同压强下随温度的变化如图所示。下列说法正确的是
的体积分数在不同压强下随温度的变化如图所示。下列说法正确的是
 和
和  在催化剂的作用下合成甲醇,发生的反应如下:
在催化剂的作用下合成甲醇,发生的反应如下: 。在体积一定的密闭容器中按物质的量之比
。在体积一定的密闭容器中按物质的量之比  充入
充入  和
和  ,测得平衡混合物中
,测得平衡混合物中  的体积分数在不同压强下随温度的变化如图所示。下列说法正确的是
的体积分数在不同压强下随温度的变化如图所示。下列说法正确的是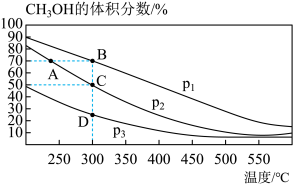
A.该反应的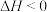 ,且 ,且 |
B.反应速率: (状态 (状态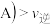 (状态 (状态 ) ) |
C.在 点时, 点时, 转化率为 转化率为 |
D.在恒温恒压条件下向密闭容器中充入不同量的 ,达平衡时 ,达平衡时  的体积分数不同 的体积分数不同 |
您最近半年使用:0次
3 . 煤的间接液化是煤的综合利用的一种重要方法。首先是煤燃烧生成 ,再在钼系催化剂的催化作用下与
,再在钼系催化剂的催化作用下与 反应,最终生成
反应,最终生成 。过程中主要发生如下反应:
。过程中主要发生如下反应:
反应I: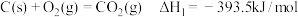
反应Ⅱ:
反应Ⅲ: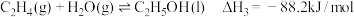
(1)钼 的基态原子中未成对电子数为
的基态原子中未成对电子数为_______ 。
(2)已知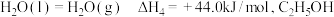 的燃烧热
的燃烧热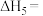
___  。
。
(3)为更好地研究煤的液化过程,某学习小组对反应Ⅱ进行了系统的研究。在一个 的刚性容器中加入
的刚性容器中加入 气体及
气体及 水蒸气,在
水蒸气,在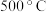 及钼系催化剂(固体)存在条件下只发生反应Ⅱ。
及钼系催化剂(固体)存在条件下只发生反应Ⅱ。
①下列能说明该反应已达到平衡状态的有_______ (填标号) 。
A. 的体积分数不再改变 B.
的体积分数不再改变 B.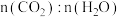 不再改变
不再改变
C.容器的总压不再改变 D.容器中气体的密度不再改变
②下图为四种组分的平衡时物质的量分数随温度的变化曲线。图中曲线b表示的物质是_______ ,原因是_______ 。 时该反应的平衡常数为
时该反应的平衡常数为_______ 。
④ 时,某同学在该容器中加入
时,某同学在该容器中加入 和
和 ,同时加入了
,同时加入了 和
和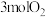 ,达到平衡后
,达到平衡后 的体积分数仍与N点相同,则
的体积分数仍与N点相同,则
_______ (用含m的代数式表示)。
 ,再在钼系催化剂的催化作用下与
,再在钼系催化剂的催化作用下与 反应,最终生成
反应,最终生成 。过程中主要发生如下反应:
。过程中主要发生如下反应:反应I:
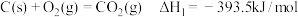
反应Ⅱ:

反应Ⅲ:
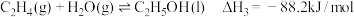
(1)钼
 的基态原子中未成对电子数为
的基态原子中未成对电子数为(2)已知
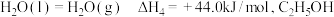 的燃烧热
的燃烧热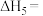
 。
。(3)为更好地研究煤的液化过程,某学习小组对反应Ⅱ进行了系统的研究。在一个
 的刚性容器中加入
的刚性容器中加入 气体及
气体及 水蒸气,在
水蒸气,在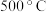 及钼系催化剂(固体)存在条件下只发生反应Ⅱ。
及钼系催化剂(固体)存在条件下只发生反应Ⅱ。①下列能说明该反应已达到平衡状态的有
A.
 的体积分数不再改变 B.
的体积分数不再改变 B.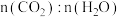 不再改变
不再改变C.容器的总压不再改变 D.容器中气体的密度不再改变
②下图为四种组分的平衡时物质的量分数随温度的变化曲线。图中曲线b表示的物质是
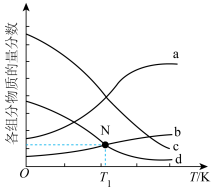
 时该反应的平衡常数为
时该反应的平衡常数为④
 时,某同学在该容器中加入
时,某同学在该容器中加入 和
和 ,同时加入了
,同时加入了 和
和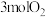 ,达到平衡后
,达到平衡后 的体积分数仍与N点相同,则
的体积分数仍与N点相同,则
您最近半年使用:0次
解题方法
4 . 燃油汽车尾气中含有NO和CO等有毒气体,某研究小组用新型催化剂对NO、CO在不同条件下的催化转化进行研究,反应原理为:
 。在密闭容器中充入2 mol NO和2 mol CO,平衡时NO的体积分数随温度、压强的变化关系如图。下列说法正确的是
。在密闭容器中充入2 mol NO和2 mol CO,平衡时NO的体积分数随温度、压强的变化关系如图。下列说法正确的是

 。在密闭容器中充入2 mol NO和2 mol CO,平衡时NO的体积分数随温度、压强的变化关系如图。下列说法正确的是
。在密闭容器中充入2 mol NO和2 mol CO,平衡时NO的体积分数随温度、压强的变化关系如图。下列说法正确的是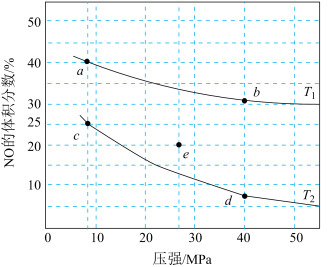
| A.a点CO的平衡转化率为25% |
| B.c点和b点的反应速率可能相同 |
| C.若在e点扩大容器体积并加热,可能达到c点状态 |
| D.恒温恒压条件下,向d点平衡体系中再充入2 mol NO和2 mol CO,重新达到平衡后,与d点状态相比,NO的体积分数将增大 |
您最近半年使用:0次
2024-04-17更新
|
293次组卷
|
3卷引用:广西壮族自治区柳州市2024届高三第三次模拟考试化学试题
广西壮族自治区柳州市2024届高三第三次模拟考试化学试题广西柳州市2024届高三下学期第三次模拟考试(三模)化学试题(已下线)题型7 化学反应速率与化学平衡 水溶液中的离子反应与平衡(25题)-2024年高考化学常考点必杀300题(新高考通用)
名校
5 . 在恒温恒容的密闭容器中,发生反应3A(g)+B(g)⇌xC(g)。
I.将3molA和2moB在一定条件下反应,达平衡时C的体积分数为a;
II.若起始时A、B、C投入的物质的量分别为nA、nB、nC,平衡时C的体积分数也为a
下列说法正确的是
I.将3molA和2moB在一定条件下反应,达平衡时C的体积分数为a;
II.若起始时A、B、C投入的物质的量分别为nA、nB、nC,平衡时C的体积分数也为a
下列说法正确的是
| A.若I达平衡时,A、B、C各增加1mol,则B的转化率将一定增大 |
| B.若向I平衡体系中再加入3molA和2molB,C的体积分数若大于a,可断定x<4 |
| C.若x=2,则II体系起始物质的量应当满足3nB=nA+3 |
| D.若II体系起始物质的量满足3nC+8nA=12nB时,可判断x=4 |
您最近半年使用:0次
6 . 已知: △H=-14.9 kJ·mol-1。某温度下在甲、乙两个恒容密闭容器中充入反应物,其起始浓度如下表所示。甲中反应达到平衡时,测得c(H2)=0.008 mol·L-1。下列判断正确的是
△H=-14.9 kJ·mol-1。某温度下在甲、乙两个恒容密闭容器中充入反应物,其起始浓度如下表所示。甲中反应达到平衡时,测得c(H2)=0.008 mol·L-1。下列判断正确的是
 △H=-14.9 kJ·mol-1。某温度下在甲、乙两个恒容密闭容器中充入反应物,其起始浓度如下表所示。甲中反应达到平衡时,测得c(H2)=0.008 mol·L-1。下列判断正确的是
△H=-14.9 kJ·mol-1。某温度下在甲、乙两个恒容密闭容器中充入反应物,其起始浓度如下表所示。甲中反应达到平衡时,测得c(H2)=0.008 mol·L-1。下列判断正确的是起始浓度 | c(H2)/(mol·L-1) | c(I2)/(mol·L-1) | c(HI)/(mol·L-1) |
甲 | 0.01 | 0.01 | 0 |
乙 | 0.02 | 0.02 | 0 |
| A.平衡时,乙中H2的转化率与甲中的相等 |
| B.平衡时,甲中混合物的颜色比乙中深 |
| C.平衡时,甲、乙中热量的变化值相等 |
| D.该温度下,反应的平衡常数K=4 |
您最近半年使用:0次
7 . 工业上合成甲醇的反应:CO(g)+2H2(g) CH3OH(g)
CH3OH(g)  =-90.8kJ·mol-1.恒温恒容,按不同方式投入反应物,3个密闭容器体积相等,测得反应达到平衡时的有关数据如下,下列说法错误的是
=-90.8kJ·mol-1.恒温恒容,按不同方式投入反应物,3个密闭容器体积相等,测得反应达到平衡时的有关数据如下,下列说法错误的是
 CH3OH(g)
CH3OH(g)  =-90.8kJ·mol-1.恒温恒容,按不同方式投入反应物,3个密闭容器体积相等,测得反应达到平衡时的有关数据如下,下列说法错误的是
=-90.8kJ·mol-1.恒温恒容,按不同方式投入反应物,3个密闭容器体积相等,测得反应达到平衡时的有关数据如下,下列说法错误的是| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1molCO 、2molH2 | 1mol CH3OH | 2molCO、4molH2 |
| H2的浓度(mol/L) | c1 | c2 | c3 |
| 反应的能量变化 | 放出Q1 kJ | 吸收Q2 kJ | 放出Q3 kJ |
| CH3OH体积分数 | φ1 | φ2 | φ3 |
| 反应物转化率 | α 1 | α 2 | α 3 |
| A.2c1>c3 | B.Q1+Q2=90.8 | C.α2+α3>100% | D.φ2>φ3 |
您最近半年使用:0次
名校
解题方法
8 . 在一定温度下,在A容器充入2molSO2(g)、1molO2(g),B容器充入2molSO3(g)并保持体积不变。起始时A和B容积相等。加入催化剂在400℃发生反应2SO2(g)+O2(g) 2SO3(g) ΔH<0,为使c(SO2)相等,下列措施不可行的是
2SO3(g) ΔH<0,为使c(SO2)相等,下列措施不可行的是
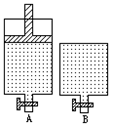
 2SO3(g) ΔH<0,为使c(SO2)相等,下列措施不可行的是
2SO3(g) ΔH<0,为使c(SO2)相等,下列措施不可行的是
| A.向A容器中再充入一定量的氦气 | B.向B容器中再充入一定量的SO3气体 |
| C.适当降低B容器的温度 | D.将A的活塞往上拉至反应前的位置 |
您最近半年使用:0次
解题方法
9 . 硫酸是基础化工的重要产品,硫酸的消费量可作为衡量一个国家工业发展水平的标志。生产硫酸的主要反应为: 。
。
(1)该反应的催化剂为 ,其催化反应过程为:
,其催化反应过程为: 、
、 

 。则在相同温度下
。则在相同温度下 的平衡常数
的平衡常数
_______ (以含 、
、 的代数式表示)。
的代数式表示)。 加快反应速率的原因是
加快反应速率的原因是_______ 。
(2) 催化氧化生成
催化氧化生成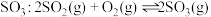
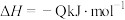 。某温度下,将
。某温度下,将 和
和 按物质的量之比2:1置于10L恒容密闭容器中反应,
按物质的量之比2:1置于10L恒容密闭容器中反应, 的平衡转化率(a)与体系总压强(P)的关系如下图所示。根据图示回答下列问题:
的平衡转化率(a)与体系总压强(P)的关系如下图所示。根据图示回答下列问题:
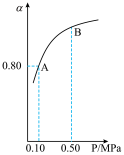
①若起始时充入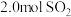 和
和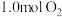 ,反应达平衡后,体系总压强为0.10MPa,则该反应的平衡常数等于
,反应达平衡后,体系总压强为0.10MPa,则该反应的平衡常数等于_______ L/mol。
②改在容器中加入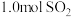 、
、 和
和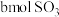 ,保持温度不变反应达平衡后,体系总压强也为0.10MPa,则b=
,保持温度不变反应达平衡后,体系总压强也为0.10MPa,则b=_______ mol,反应开始时
_______ 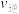 。反应中吸收或释放的热量为
。反应中吸收或释放的热量为_______ kJ。
③平衡状态由A变到B时,平衡常数
_______  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(3)工业上可以用NaOH溶液或氨水吸收过量的 ,分别生成
,分别生成 、
、 ,其水溶液均呈酸性。相同条件下,同浓度的两种酸式盐的水溶液中
,其水溶液均呈酸性。相同条件下,同浓度的两种酸式盐的水溶液中 较小的是
较小的是_______ (填化学式),用文字和化学用语解释原因_______ 。
 。
。(1)该反应的催化剂为
 ,其催化反应过程为:
,其催化反应过程为: 、
、 

 。则在相同温度下
。则在相同温度下 的平衡常数
的平衡常数
 、
、 的代数式表示)。
的代数式表示)。 加快反应速率的原因是
加快反应速率的原因是(2)
 催化氧化生成
催化氧化生成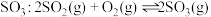
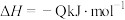 。某温度下,将
。某温度下,将 和
和 按物质的量之比2:1置于10L恒容密闭容器中反应,
按物质的量之比2:1置于10L恒容密闭容器中反应, 的平衡转化率(a)与体系总压强(P)的关系如下图所示。根据图示回答下列问题:
的平衡转化率(a)与体系总压强(P)的关系如下图所示。根据图示回答下列问题:
①若起始时充入
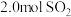 和
和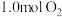 ,反应达平衡后,体系总压强为0.10MPa,则该反应的平衡常数等于
,反应达平衡后,体系总压强为0.10MPa,则该反应的平衡常数等于②改在容器中加入
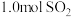 、
、 和
和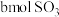 ,保持温度不变反应达平衡后,体系总压强也为0.10MPa,则b=
,保持温度不变反应达平衡后,体系总压强也为0.10MPa,则b=
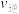 。反应中吸收或释放的热量为
。反应中吸收或释放的热量为③平衡状态由A变到B时,平衡常数

 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。(3)工业上可以用NaOH溶液或氨水吸收过量的
 ,分别生成
,分别生成 、
、 ,其水溶液均呈酸性。相同条件下,同浓度的两种酸式盐的水溶液中
,其水溶液均呈酸性。相同条件下,同浓度的两种酸式盐的水溶液中 较小的是
较小的是
您最近半年使用:0次
名校
解题方法
10 . 向相同容积的甲、乙两容器中分别充入 和
和 ,发生如下反应:
,发生如下反应: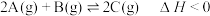 。若甲容器保持恒温恒容,乙容器保持绝热恒容,分别达到平衡。甲容器中平衡时生成
。若甲容器保持恒温恒容,乙容器保持绝热恒容,分别达到平衡。甲容器中平衡时生成 为
为 ,同时放出热量
,同时放出热量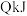 。下列说法正确的是
。下列说法正确的是
 和
和 ,发生如下反应:
,发生如下反应: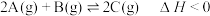 。若甲容器保持恒温恒容,乙容器保持绝热恒容,分别达到平衡。甲容器中平衡时生成
。若甲容器保持恒温恒容,乙容器保持绝热恒容,分别达到平衡。甲容器中平衡时生成 为
为 ,同时放出热量
,同时放出热量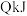 。下列说法正确的是
。下列说法正确的是| A.平衡时,反应放出的热量:甲>乙 |
B.平衡时, 的质量:甲>乙 的质量:甲>乙 |
C.乙容器若把条件“绝热恒压”改为“恒温恒压”,则平衡后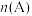 大于 大于 |
D.相同条件下,若仅向甲容器充入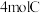 ,平衡时生成 ,平衡时生成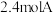 ,同时吸收热量 ,同时吸收热量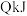 |
您最近半年使用:0次



