Ⅰ.H2S与CH4重整,不但可以消除污染,还可以制氢。主要反应为 ;ΔH>0。
;ΔH>0。
(1)在恒温恒容条件下,可作为上述反应达到平衡状态的判断依据的是_______。
Ⅱ.在恒压条件下,以n(CH4)∶n(H2S)=1∶2组成的混合气体发生反应: ;ΔH>0,达到平衡状态时,四种组分物质的量分数随温度的变化如下图所示。
;ΔH>0,达到平衡状态时,四种组分物质的量分数随温度的变化如下图所示。_______ 、_______ (填化学式)。
(3)M点对应温度下,H2S的转化率是_______ 。
Ⅲ.在研究反应发生的适宜条件时发现:过多的CH4会导致Al2O3催化剂失活;Co助剂有稳定催化剂的作用。如下图表示800 ℃,Al2O3催化剂条件下投入等量H2S,投料比[n(CH4)∶n(H2S)]分别为1∶1、1∶3、12∶1,达平衡时H2S转化率、平均反应速率。_______ (填“A”“B”或“C”)组图像。三组图像中,C组图像中平均反应速率最低的可能原因是_______ 。
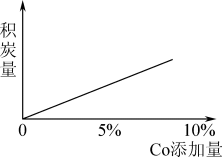
(5)未添加Co助剂时,无积炭,随着Co添加量的变化,积炭量变化如下图所示,Co助剂可能催化原料气发生反应的化学方程式为____ 。
 ;ΔH>0。
;ΔH>0。(1)在恒温恒容条件下,可作为上述反应达到平衡状态的判断依据的是_______。
| A.混合气体密度不变 |
| B.容器内压强不变 |
| C.2v正(H2S)=v逆(CS2) |
| D.CH4与H2的物质的量分数之比保持不变 |
Ⅱ.在恒压条件下,以n(CH4)∶n(H2S)=1∶2组成的混合气体发生反应:
 ;ΔH>0,达到平衡状态时,四种组分物质的量分数随温度的变化如下图所示。
;ΔH>0,达到平衡状态时,四种组分物质的量分数随温度的变化如下图所示。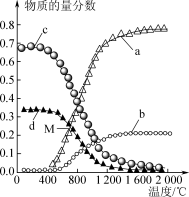
(3)M点对应温度下,H2S的转化率是
Ⅲ.在研究反应发生的适宜条件时发现:过多的CH4会导致Al2O3催化剂失活;Co助剂有稳定催化剂的作用。如下图表示800 ℃,Al2O3催化剂条件下投入等量H2S,投料比[n(CH4)∶n(H2S)]分别为1∶1、1∶3、12∶1,达平衡时H2S转化率、平均反应速率。
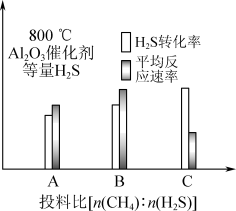
(5)未添加Co助剂时,无积炭,随着Co添加量的变化,积炭量变化如下图所示,Co助剂可能催化原料气发生反应的化学方程式为
2024高三·全国·专题练习 查看更多[1]
(已下线)FHgkyldyjhx07
更新时间:2024-05-03 10:06:02
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】(Ⅰ)某化学反应A B+C在三种不同条件下进行,B、C的起始浓度为0,反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表所示,表中温度为摄氏度(℃)。
B+C在三种不同条件下进行,B、C的起始浓度为0,反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表所示,表中温度为摄氏度(℃)。
(1)该反应属于__________ 反应(填“可逆”或“不可逆”)。
(2)在实验1、2中,有一个实验使用了催化剂。请你利用表中数据判断实验___ (填1或2)使用了催化剂,理由是_______________ 。
(3)该实验表明,影响化学反应速率的因素还有__________ 。
(Ⅱ)下图是1molNO2和1molCO反应生成1molCO2和1molNO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:__________________ 。
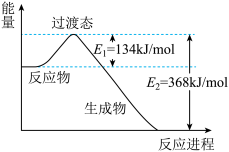
该反应的活化能等于____________________
 B+C在三种不同条件下进行,B、C的起始浓度为0,反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表所示,表中温度为摄氏度(℃)。
B+C在三种不同条件下进行,B、C的起始浓度为0,反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表所示,表中温度为摄氏度(℃)。| 实验 序号 | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
| 1 | 800 | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800 | 1.0 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 820 | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
(1)该反应属于
(2)在实验1、2中,有一个实验使用了催化剂。请你利用表中数据判断实验
(3)该实验表明,影响化学反应速率的因素还有
(Ⅱ)下图是1molNO2和1molCO反应生成1molCO2和1molNO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:

该反应的活化能等于
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】将二氧化碳转化为甲醇等液体燃料实现“人工碳循环”,不仅能缓解温室效应,还将成为理想的能源补充形式。
中国团队研究出的铂(Pt)—硫化钼原子级分散催化剂,能有效拉近催化剂表面Pt原子之间的距离,将CO2高效转化为甲醇。实验表明,近邻Pt原子在CO2加氢转化为甲醇的过程中表现出比孤立Pt原子更高的催化活性。理论研究揭示了催化CO2加氢过程中相邻Pt原子间的协同作用。
针对这种“两个近邻Pt原子的催化活性高于两个孤立Pt原子的催化活性之和”的现象,他们创造性地提出了“单中心近邻原子协同催化”的新概念,突破了人们对单原子之间互不干扰的传统认识,为操纵催化性能创造新的途径。
请依据以上短文,判断下列说法是否正确(填“正确”或“错误”)。
1.CO2转化为甲醇属于化学变化。(_______)
2.新型催化剂的研发,能将CO2高效转化为甲醇。(_______)
3.在催化CO2加氢转化为甲醇的过程中,两个近邻Pt原子的催化活性低于两个孤立Pt原子的催化活性之和。(_______)
中国团队研究出的铂(Pt)—硫化钼原子级分散催化剂,能有效拉近催化剂表面Pt原子之间的距离,将CO2高效转化为甲醇。实验表明,近邻Pt原子在CO2加氢转化为甲醇的过程中表现出比孤立Pt原子更高的催化活性。理论研究揭示了催化CO2加氢过程中相邻Pt原子间的协同作用。
针对这种“两个近邻Pt原子的催化活性高于两个孤立Pt原子的催化活性之和”的现象,他们创造性地提出了“单中心近邻原子协同催化”的新概念,突破了人们对单原子之间互不干扰的传统认识,为操纵催化性能创造新的途径。
请依据以上短文,判断下列说法是否正确(填“正确”或“错误”)。
1.CO2转化为甲醇属于化学变化。(_______)
2.新型催化剂的研发,能将CO2高效转化为甲醇。(_______)
3.在催化CO2加氢转化为甲醇的过程中,两个近邻Pt原子的催化活性低于两个孤立Pt原子的催化活性之和。(_______)
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】化学反应是有历程的。研究反应机理对于认识反应和调控反应意义重大。
I:NO和H2可以反应生成N2和水蒸气,该反应的历程包含下列两步:
① (慢)
(慢) 
②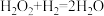 (快)
(快) 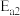
(1)该反应速率由___________ (填①或②)决定。
(2)活化能
___________ 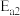 (填“>或<或=”)。
(填“>或<或=”)。
II:催化剂参与反应过程,能加快反应速率。
(3) 的速率很慢,NO和
的速率很慢,NO和 都可以作为该反应的催化剂,发生两步基元反应,快速生成
都可以作为该反应的催化剂,发生两步基元反应,快速生成 。请结合催化剂的特点,写出NO做催化剂时,这两步基元反应的方程式
。请结合催化剂的特点,写出NO做催化剂时,这两步基元反应的方程式___________ 、___________ 。
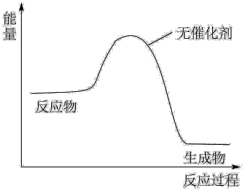
(4)请在下图中画出加入催化剂时的能量变化过程(在图上画出)(已知该两步反应均为放热反应)______ 。
I:NO和H2可以反应生成N2和水蒸气,该反应的历程包含下列两步:
①
 (慢)
(慢) 
②
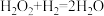 (快)
(快) 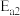
(1)该反应速率由
(2)活化能

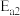 (填“>或<或=”)。
(填“>或<或=”)。II:催化剂参与反应过程,能加快反应速率。
(3)
 的速率很慢,NO和
的速率很慢,NO和 都可以作为该反应的催化剂,发生两步基元反应,快速生成
都可以作为该反应的催化剂,发生两步基元反应,快速生成 。请结合催化剂的特点,写出NO做催化剂时,这两步基元反应的方程式
。请结合催化剂的特点,写出NO做催化剂时,这两步基元反应的方程式(4)请在下图中画出加入催化剂时的能量变化过程(在图上画出)(已知该两步反应均为放热反应)

您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】化学平衡状态的判断方法
(1)在密闭容器中进行反应: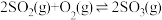 ,当SO2、O2、SO3的浓度之比为2∶1∶2时,能否说明该反应达到化学平衡状态
,当SO2、O2、SO3的浓度之比为2∶1∶2时,能否说明该反应达到化学平衡状态______ ?
(2)判断依据
①v(正)=v(逆):
a.同一物质的正、逆反应速率______ 。
b.不同物质的正、逆反应速率与对应化学方程式中的______ 成正比。
②浓度保持一定:
各组分的______ 不随时间的改变而改变。
(1)在密闭容器中进行反应:
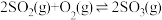 ,当SO2、O2、SO3的浓度之比为2∶1∶2时,能否说明该反应达到化学平衡状态
,当SO2、O2、SO3的浓度之比为2∶1∶2时,能否说明该反应达到化学平衡状态(2)判断依据
①v(正)=v(逆):
a.同一物质的正、逆反应速率
b.不同物质的正、逆反应速率与对应化学方程式中的
②浓度保持一定:
各组分的
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】(1)在两个恒温、恒容的密闭容器中进行下列两个可逆反应:
(甲)2X(g)⇋Y(g)+Z(s);
(乙)A(s)+2B(g)⇋C(g)+D(g),
当下列物理量不再发生变化时,可以表明甲和乙均达到平衡状态的有:____________________________ 。
①混合气体密度 ②反应容器中生成物的百分含量 ③反应物的消耗速率与生成物的消耗速率之比等于化学计量数之比 ④混合气体的平均相对分子质量 ⑤混合气体的压强 ⑥混合气体的总物质的量
(2)下列说法中,有几种说法是正确的:_______ (填数值如“1”或“2”等)。
a.糖类、油脂、蛋白质都能发生水解反应
b.糖类、油脂、蛋白质都是高分子化合物
c.油脂有油和脂肪之分,但都属于酯
d.糖类、油脂、蛋白质的组成中都有C、H、O、N等元素
e.人体需要的二十多种氨基酸都可以通过人体自身合成
f.油脂都是高级脂肪酸的甘油酯,是一种高热量营养素
g.馒头、米饭在口腔内越嚼越甜,是因为它们含有的淀粉发生了酯化反应
h.豆油、牛油、花生油属于酯类
i.淀粉与纤维素的分子式同为(C6H10O5)n,两者互为同分异构体
j.我们不需要从食物中摄取维生素,因为多数维生素能在人体内合成
k.由于缺碘会引起甲状腺肿大,所以我们要多食用加碘食盐
l.由于霉变食物中含有能损害人的肝脏、诱发肝癌等疾病的黄曲霉毒素,因此,我们不能食用霉变食物
(甲)2X(g)⇋Y(g)+Z(s);
(乙)A(s)+2B(g)⇋C(g)+D(g),
当下列物理量不再发生变化时,可以表明甲和乙均达到平衡状态的有:
①混合气体密度 ②反应容器中生成物的百分含量 ③反应物的消耗速率与生成物的消耗速率之比等于化学计量数之比 ④混合气体的平均相对分子质量 ⑤混合气体的压强 ⑥混合气体的总物质的量
(2)下列说法中,有几种说法是正确的:
a.糖类、油脂、蛋白质都能发生水解反应
b.糖类、油脂、蛋白质都是高分子化合物
c.油脂有油和脂肪之分,但都属于酯
d.糖类、油脂、蛋白质的组成中都有C、H、O、N等元素
e.人体需要的二十多种氨基酸都可以通过人体自身合成
f.油脂都是高级脂肪酸的甘油酯,是一种高热量营养素
g.馒头、米饭在口腔内越嚼越甜,是因为它们含有的淀粉发生了酯化反应
h.豆油、牛油、花生油属于酯类
i.淀粉与纤维素的分子式同为(C6H10O5)n,两者互为同分异构体
j.我们不需要从食物中摄取维生素,因为多数维生素能在人体内合成
k.由于缺碘会引起甲状腺肿大,所以我们要多食用加碘食盐
l.由于霉变食物中含有能损害人的肝脏、诱发肝癌等疾病的黄曲霉毒素,因此,我们不能食用霉变食物
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】已知体积为2L的恒容密闭容器中发生反应:2SO2(g) + O2(g)  2SO3(g),请根据化学反应的有关原理回答下列问题:
2SO3(g),请根据化学反应的有关原理回答下列问题:
(1)一定条件下,充入2molSO2(g)和2molO2(g),20 s后,测得SO2的体积百分含量为12.5%,则用SO2表示该反应在这20s内的反应速率为____ 。
(2)下面的叙述可作为判断(1)中可逆反应达到平衡状态依据的是(填序号)____ 。
①v正(SO2)=2v逆(O2)②混合气体的密度不变③混合气体的平均相对分子质量不变④各气体的浓度都不再发生变化
(3)下图表示该反应的速率(v)随时间(t)的变化的关系。则下列不同时间段中,SO3的百分含量最高的是( )
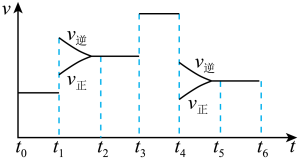
A、t2→t3 ) B、t0→t1 C、t5→t6 D、t3→t4
据图分析:你认为t3时改变的外界条件可能是_____ ; t6时保持体积不变向体系中充人少量SO3,再次平衡后SO2的体积百分含量比t6时____ (填“大”“小”或“等于”)。
(4)下图中P是可自由平行滑动的活塞。在相同温度时,向A容器中充入4 molSO3(g),关闭K,向B容器中充入2 molSO3(g),两容器分别发生反应。已知起始时容器A和B的体积均为aL。试回答:
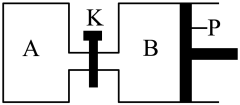
①反应达到平衡时容器B的体积为1.2aL,容器B中SO3转化率为____ 。
②若打开K,一段时间后重新达到平衡,容器B的体积为_____ L(连通管中气体体积忽略不计,且不考虑温度的影响)。
 2SO3(g),请根据化学反应的有关原理回答下列问题:
2SO3(g),请根据化学反应的有关原理回答下列问题:(1)一定条件下,充入2molSO2(g)和2molO2(g),20 s后,测得SO2的体积百分含量为12.5%,则用SO2表示该反应在这20s内的反应速率为
(2)下面的叙述可作为判断(1)中可逆反应达到平衡状态依据的是(填序号)
①v正(SO2)=2v逆(O2)②混合气体的密度不变③混合气体的平均相对分子质量不变④各气体的浓度都不再发生变化
(3)下图表示该反应的速率(v)随时间(t)的变化的关系。则下列不同时间段中,SO3的百分含量最高的是

A、t2→t3 ) B、t0→t1 C、t5→t6 D、t3→t4
据图分析:你认为t3时改变的外界条件可能是
(4)下图中P是可自由平行滑动的活塞。在相同温度时,向A容器中充入4 molSO3(g),关闭K,向B容器中充入2 molSO3(g),两容器分别发生反应。已知起始时容器A和B的体积均为aL。试回答:

①反应达到平衡时容器B的体积为1.2aL,容器B中SO3转化率为
②若打开K,一段时间后重新达到平衡,容器B的体积为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】在1L密闭容器中通入CO2、H2各2mol,在一定条件下发生反应:CO2(g)+H2(g) CO(g)+H2O(g),回答下列问题:
CO(g)+H2O(g),回答下列问题:
(1)在830℃条件下,反应达到平衡时CO2的转化率为50%。求该条件下的化学平衡常数K1=_______ 。(写出该反应的化学平衡常数的表达式并计算出结果)
(2)在(1)的基础上,把体系温度降至800℃。已知该条件下的平衡常数K2=0.81,可以推知该反应的正反应为_______ 反应(填“吸热”或“放热”)。
(3)在(1)的基础上,压缩容器体积为0.5L。该条件下的平衡常数为K3。则K3_______ K1(填“<”或”>”或“=”)。
(4)830℃时,某时刻测得体系中各物质的量如下:n(CO2)=1.2mol,n(H2)=1.5mol,n(CO)=0.9mol,n(H2O)=0.9mol,则此时该反应_______ (填“向正反应方向进行”或“向逆反应方向进行”或“处于平衡状态”)。
(5)某温度时,在2L密闭容器中发生:C(s)+H2O(g) CO(g)+H2(g)。起始时C为2mol, H2O 为3mol,平衡时CO转化率为60%,则平衡时氢气的浓度为
CO(g)+H2(g)。起始时C为2mol, H2O 为3mol,平衡时CO转化率为60%,则平衡时氢气的浓度为_______ ,此时容器内总压强与起始时的压强之比为_______ 。
 CO(g)+H2O(g),回答下列问题:
CO(g)+H2O(g),回答下列问题:(1)在830℃条件下,反应达到平衡时CO2的转化率为50%。求该条件下的化学平衡常数K1=
(2)在(1)的基础上,把体系温度降至800℃。已知该条件下的平衡常数K2=0.81,可以推知该反应的正反应为
(3)在(1)的基础上,压缩容器体积为0.5L。该条件下的平衡常数为K3。则K3
(4)830℃时,某时刻测得体系中各物质的量如下:n(CO2)=1.2mol,n(H2)=1.5mol,n(CO)=0.9mol,n(H2O)=0.9mol,则此时该反应
(5)某温度时,在2L密闭容器中发生:C(s)+H2O(g)
 CO(g)+H2(g)。起始时C为2mol, H2O 为3mol,平衡时CO转化率为60%,则平衡时氢气的浓度为
CO(g)+H2(g)。起始时C为2mol, H2O 为3mol,平衡时CO转化率为60%,则平衡时氢气的浓度为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】研究化学反应的快慢和限度具有十分重要的意义,已知:反应aA(g)+bB(g)⇌cC(g),某温度下,在2L的密闭容器中投入一定量的A和B,两种气体的物质的量浓度随时间变化的曲线如图所示。

(1)经测定,前4s内v(C)=0.05mol·L-1·s-1,4s时容器内C的物质的量为___________ ,则该反应的化学方程式为___________ 。
(2)该反应达到化学反应限度时,A的转化率为___________ 。
(3)若上述反应分别在甲、乙、丙三个相同的密闭容器中进行,反应相同时间后,测得三个容器中的化学反应速率分别为:
甲:v(A)=0.3mol·L-1·s-1;
乙:v(B)=0.2mol·L-1·s-1;
丙:v(C)=0.6mol·L-1·min-1。
则甲、乙、丙三个容器中化学反应速率由快到慢的顺序为___________ (用甲、乙、丙表示)。
(4)下列条件的改变能减小上述反应的反应速率的是___________ 。
①保持体积不变,充入He
②保持压强不变,充入He
③降低温度
④增大C的浓度
(5)下列叙述能说明该反应达到化学平衡状态的是___________ 。
①混合气体的总质量不随时间变化而变化
②单位时间内每消耗3molA,同时生成1molB
③3v(A)正=v(B)逆
④混合气体的密度不随时间变化而变化
⑤A物质的物质的量分数不随时间变化而变化

(1)经测定,前4s内v(C)=0.05mol·L-1·s-1,4s时容器内C的物质的量为
(2)该反应达到化学反应限度时,A的转化率为
(3)若上述反应分别在甲、乙、丙三个相同的密闭容器中进行,反应相同时间后,测得三个容器中的化学反应速率分别为:
甲:v(A)=0.3mol·L-1·s-1;
乙:v(B)=0.2mol·L-1·s-1;
丙:v(C)=0.6mol·L-1·min-1。
则甲、乙、丙三个容器中化学反应速率由快到慢的顺序为
(4)下列条件的改变能减小上述反应的反应速率的是
①保持体积不变,充入He
②保持压强不变,充入He
③降低温度
④增大C的浓度
(5)下列叙述能说明该反应达到化学平衡状态的是
①混合气体的总质量不随时间变化而变化
②单位时间内每消耗3molA,同时生成1molB
③3v(A)正=v(B)逆
④混合气体的密度不随时间变化而变化
⑤A物质的物质的量分数不随时间变化而变化
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】红磷P(s)和Cl2(g)发生反应生成PCl3和PCl5,反应过程和能量关系如图所示(图中的ΔH表示生成1 mol产物的数据),根据下图回答下列问题:

(1)PCl5分解生成PCl3和Cl2的热化学方程式__________________________ ;上述分解反应是一个可逆反应,温度T1时,在密闭容器中加入0.8 mol PCl5,反应达到平衡时生成标准状况下4.48LCl2,其分解率a1为_________ ;若反应温度由T1升高到T2,平衡时PCl5的分解率a2,a2______ a1(填“大于”、“小于”或“等于”)。
(2)工业上制备PCl5通常分两步进行,先将P和Cl2反应生成中间产物PCl3,然后降温,再和Cl2反应生成PCl5。原因是__________________________________________ 。
(3)P和Cl2分两步反应生成1 mol PCl5的ΔH3=__________________ 。

(1)PCl5分解生成PCl3和Cl2的热化学方程式
(2)工业上制备PCl5通常分两步进行,先将P和Cl2反应生成中间产物PCl3,然后降温,再和Cl2反应生成PCl5。原因是
(3)P和Cl2分两步反应生成1 mol PCl5的ΔH3=
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】可逆反应:aA(g)+ bB(g) cC(g)+ dD(g);根据图回答:
cC(g)+ dD(g);根据图回答:
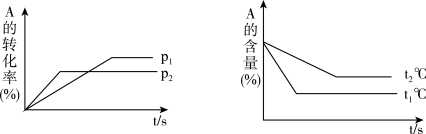
(1)压强p1_________ p2(填“>”或“<”);
(2)a +b__________ c +d(填“>”或“<”);
(3)温度t1℃_________ t2℃(填“>”或“<”);
(4)正反应为_________ 反应。(填吸热或放热)
 cC(g)+ dD(g);根据图回答:
cC(g)+ dD(g);根据图回答:
(1)压强p1
(2)a +b
(3)温度t1℃
(4)正反应为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】向1L恒容密闭容器中充入3molCO2、7molH2的混合气体,控制适当条件发生反应: 。如图为不同温度下,反应经过10min时容器中c(CH3OH)变化情况。
。如图为不同温度下,反应经过10min时容器中c(CH3OH)变化情况。
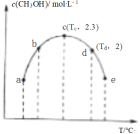
回答下列问题:
(1)第10min时,正反应速率υ(c)_______ (填“>”“<”或“=”,下同)υ(d),c点处对应反应体系中c(H2)=_______  。
。
(2)该反应的
_______ (填“>”或“<”)0,a、b、c、d、e五点对应温度下,反应肯定处于非平衡状态的是_______ (填字母)。
(3)实际生产中,通常会采用下列方法以提高单位时间内CH3OH的产率_______(填字母)。
(4)若d点时容器总压为12kPa,则Kp=_______ (用平衡分压代替平衡浓度,分压=总压 物质的量分数)。
物质的量分数)。
 。如图为不同温度下,反应经过10min时容器中c(CH3OH)变化情况。
。如图为不同温度下,反应经过10min时容器中c(CH3OH)变化情况。
回答下列问题:
(1)第10min时,正反应速率υ(c)
 。
。(2)该反应的

(3)实际生产中,通常会采用下列方法以提高单位时间内CH3OH的产率_______(填字母)。
| A.使用催化剂 | B.不断分离出产物 |
| C.低温下进行反应 | D.不断补充原料 |
 物质的量分数)。
物质的量分数)。
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】二氧化碳的转化和利用成为实现“碳达峰”、“碳中和”的重要研究课题。回答下列问题:
(1)利用CO2和H2可生产乙烯。相关热化学方程式为:
反应I:2CO2(g)+6H2(g) CH2=CH2(g)+4H2O(g) △H1=−246.4 kJ∙mol−1
CH2=CH2(g)+4H2O(g) △H1=−246.4 kJ∙mol−1
反应II:CO2(g)+4H2(g) CH4(g)+2H2O(g) △H2=−166.8 kJ∙mol−1
CH4(g)+2H2O(g) △H2=−166.8 kJ∙mol−1
某催化剂作用下,在容积为2.0L的恒容密闭容器中充入lmolCO2和3molH2,体系中主要发生上述反应I和反应II两个竞争反应。反应进行tmin时测得两种烃的物质的量随温度的变化如图所示,该催化剂在840℃时主要选择反应________ (填“I”或“II”);840℃之后,C2H4产量下降的原因是_______ 。

520℃时,0~tmin内用氢气表示反应II的平均反应速率:υ(H2)=_______ mol/(L·min)(用含t的代数式表示)。
(2)利用工业废气CO2制甲醇,发生反应III:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H3<0,可一定程度摆脱当下对化石燃料的依赖。
CH3OH(g)+H2O(g) △H3<0,可一定程度摆脱当下对化石燃料的依赖。
①上述反应自发的条件是________ 。
②在aL密闭容器中,充入不同氢碳比的原料气体,控制温度600K,发生反应III,请在图中画出CH3OH在混合气体中的平衡体积分数随氢碳比递增的变化趋势_________ 。

③一定条件下,将1molCO2和1molH2置于恒容密闭容器中,发生反应III。下列能说明反应达到平衡状态的是_________ 。
A.混合气体的密度保持不变
B.CO2的消耗速率与H2O的消耗速率相等
C.CO2的体积分数保持不变
D.混合气体的平均相对分子质量保持不变
(1)利用CO2和H2可生产乙烯。相关热化学方程式为:
反应I:2CO2(g)+6H2(g)
 CH2=CH2(g)+4H2O(g) △H1=−246.4 kJ∙mol−1
CH2=CH2(g)+4H2O(g) △H1=−246.4 kJ∙mol−1反应II:CO2(g)+4H2(g)
 CH4(g)+2H2O(g) △H2=−166.8 kJ∙mol−1
CH4(g)+2H2O(g) △H2=−166.8 kJ∙mol−1某催化剂作用下,在容积为2.0L的恒容密闭容器中充入lmolCO2和3molH2,体系中主要发生上述反应I和反应II两个竞争反应。反应进行tmin时测得两种烃的物质的量随温度的变化如图所示,该催化剂在840℃时主要选择反应

520℃时,0~tmin内用氢气表示反应II的平均反应速率:υ(H2)=
(2)利用工业废气CO2制甲醇,发生反应III:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H3<0,可一定程度摆脱当下对化石燃料的依赖。
CH3OH(g)+H2O(g) △H3<0,可一定程度摆脱当下对化石燃料的依赖。①上述反应自发的条件是
②在aL密闭容器中,充入不同氢碳比的原料气体,控制温度600K,发生反应III,请在图中画出CH3OH在混合气体中的平衡体积分数随氢碳比递增的变化趋势

③一定条件下,将1molCO2和1molH2置于恒容密闭容器中,发生反应III。下列能说明反应达到平衡状态的是
A.混合气体的密度保持不变
B.CO2的消耗速率与H2O的消耗速率相等
C.CO2的体积分数保持不变
D.混合气体的平均相对分子质量保持不变
您最近一年使用:0次



