名校
解题方法
1 . V2O5(五氧化二钒)可作化学工业中的催化剂。为回收利用含钒催化剂,研制了一种利用废催化剂(含有V2O5、VOSO4、不溶性硅酸盐)回收V2O5的新工艺流程如下:
②部分含钒物质常温下在水中的溶解性如表所示:
③ +2OH-
+2OH-
 +H2O
+H2O
回答下列问题:
(1)在滤渣1中加入Na2SO3和过量H2SO4溶液发生反应生成VOSO4的化学方程式为___________ 。
(2)在第Ⅱ步中需要加入氨水,请结合 +2OH-
+2OH-
 +H2O,用平衡移动原理解释加入氨水的作用为
+H2O,用平衡移动原理解释加入氨水的作用为___________ 。
(3)需在流动空气中加热NH4VO3的原因可能是___________ 。
(4)将0.250g产品溶于强碱溶液中,加热煮沸,调节pH为8~8.5,向反应后的溶液中加入硫酸酸化的KI溶液(过量),溶液中的还原产物为V3+离子,滴加指示剂,用0.250mol/LNa2S2O3溶液滴定,达到终点时消耗Na2S2O3标准溶液20.00mL,则该产品的纯度为___________ (保留4位有效数字)。(已知:I2+2 Na2S2O3= Na2S4O6+2NaI,写出计算过程)

②部分含钒物质常温下在水中的溶解性如表所示:
| 物质 | VOSO4 | V2O5 | NH4VO3 | (VO2)2SO4 |
| 溶解性 | 可溶 | 难溶 | 难溶 | 易溶 |
 +2OH-
+2OH-
 +H2O
+H2O回答下列问题:
(1)在滤渣1中加入Na2SO3和过量H2SO4溶液发生反应生成VOSO4的化学方程式为
(2)在第Ⅱ步中需要加入氨水,请结合
 +2OH-
+2OH-
 +H2O,用平衡移动原理解释加入氨水的作用为
+H2O,用平衡移动原理解释加入氨水的作用为(3)需在流动空气中加热NH4VO3的原因可能是
(4)将0.250g产品溶于强碱溶液中,加热煮沸,调节pH为8~8.5,向反应后的溶液中加入硫酸酸化的KI溶液(过量),溶液中的还原产物为V3+离子,滴加指示剂,用0.250mol/LNa2S2O3溶液滴定,达到终点时消耗Na2S2O3标准溶液20.00mL,则该产品的纯度为
您最近半年使用:0次
2 . 向绝热恒容密闭容器中通入一定量SO2与NO2的混合气体,在一定条件下发生反应:SO2(g)+NO2(g) SO3(g)+NO(g)。其正反应速率
SO3(g)+NO(g)。其正反应速率 正随时间t变化的曲线如下,不考虑副反应的影响,下列说法正确的是
正随时间t变化的曲线如下,不考虑副反应的影响,下列说法正确的是
 SO3(g)+NO(g)。其正反应速率
SO3(g)+NO(g)。其正反应速率 正随时间t变化的曲线如下,不考虑副反应的影响,下列说法正确的是
正随时间t变化的曲线如下,不考虑副反应的影响,下列说法正确的是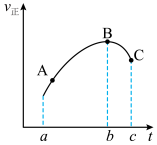
A. 逆随t变化的曲线在a~c时间段内与 逆随t变化的曲线在a~c时间段内与 正的趋势相同 正的趋势相同 |
| B.从A点到C点,NO的分压一直增大 |
| C.其他条件不变时,若在恒温条件下发生此反应,则SO2的平衡转化率减小 |
| D.A、B、C三点的Q值:QA>QB>Qc |
您最近半年使用:0次
名校
解题方法
3 . 下列有关实验装置或操作能达到相应目的的是
|
|
| A.通过注射器活塞移动验证钠与水反应放热 | B.探究浓度对反应速率的影响 |
|
|
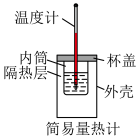
| C.检查容量瓶是否漏液 | D.测定中和热 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
4 . 向绝热恒容密闭容器中通入SO2和NO2,在一定条件下发生反应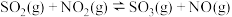 ,正反应速率随时间变化的示意图如下图,下列结论中正确的个数为
,正反应速率随时间变化的示意图如下图,下列结论中正确的个数为
②SO2浓度:a点小于c点
③反应物的总能量低于生成物的总能量
④ ,ab段NO2的消耗量小于bc段NO2的消耗量
,ab段NO2的消耗量小于bc段NO2的消耗量
⑤混合物颜色不再变化,说明反应达到平衡
⑥体系压强不再变化,说明反应达到平衡
⑦逆反应速率图象在此时间段内和上图趋势相同
⑧达到平衡后,改变容器体积增大压强,逆反应速率可能先增大后减小
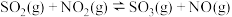 ,正反应速率随时间变化的示意图如下图,下列结论中正确的个数为
,正反应速率随时间变化的示意图如下图,下列结论中正确的个数为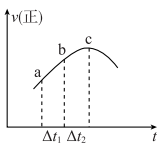
②SO2浓度:a点小于c点
③反应物的总能量低于生成物的总能量
④
 ,ab段NO2的消耗量小于bc段NO2的消耗量
,ab段NO2的消耗量小于bc段NO2的消耗量⑤混合物颜色不再变化,说明反应达到平衡
⑥体系压强不再变化,说明反应达到平衡
⑦逆反应速率图象在此时间段内和上图趋势相同
⑧达到平衡后,改变容器体积增大压强,逆反应速率可能先增大后减小
| A.3个 | B.4个 | C.5个 | D.6个 |
您最近半年使用:0次
名校
5 . 下列各组反应(表中物质均为反应物)在反应刚开始时,放出H2的速率最大的是
选项 | 金属(粉末状)及其物质的量/mol | 酸的浓度及体积 | 反应温度/℃ |
A. | Mg 0.1 | 8 mol∙L-1硝酸 10mL | 30 |
B. | Mg 0.1 | 3 mol∙L-1盐酸 10mL | 30 |
C. | Fe 0.1 | 6 mol∙L-1盐酸 10mL | 30 |
D. | Mg 0.1 | 3 mol∙L-1硫酸 10mL | 30 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
6 . 下列实验事实引出的结论不正确的是
| 选项 | 事实 | 结论 |
| A | 室温下,分别向2支试管中加入相同体积、相同浓度的Na2S2O3溶液,再分别加入相同体积不同浓度的稀硫酸,比较析出沉淀所需时间 | 当其他条件不变时,反应物浓度增大,化学反应速率加快 |
| B | 向FeCl3溶液中加入几滴KSCN溶液,溶液变红,然后加入少量铁粉,红色变浅 | 铁粉与KSCN溶液反应,减少了FeCl3与KSCN的反应 |
| C | 往浅黄色固体难溶物AgBr中加水,振荡,静置。取上层清液,然后加入NaI固体,产生黄色沉淀 | 难溶物存在沉淀溶解平衡 |
| D | A、B两支试管中分别加入等体积5%的H2O2溶液,在B中加入2~3滴FeCl3溶液,B试管中产生气泡快 | 当其他条件不变时,催化剂可以改变化学反应速率 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
7 . 13g锌粒与足量2 稀硫酸反应生成
稀硫酸反应生成 ,下列措施可以加快反应速率,但减少
,下列措施可以加快反应速率,但减少 的最终生成量的是
的最终生成量的是
 稀硫酸反应生成
稀硫酸反应生成 ,下列措施可以加快反应速率,但减少
,下列措施可以加快反应速率,但减少 的最终生成量的是
的最终生成量的是| A.将锌粒换成等质量的锌粉 | B.向稀硫酸中加入少量 固体 固体 |
C.向稀硫酸中加入少量 溶液 溶液 | D.将该稀硫酸换成足量0.5 稀硫酸 稀硫酸 |
您最近半年使用:0次
8 . 某兴趣小组探究高锰酸钾和氨水的反应,实验如下:
注:实验中c(KMnO4) = 0.01 mol·L-1。
下列说法不正确 的是
| 序号 | 试剂 | 实验现象 |
| ① | 2 mL KMnO4溶液 + 1 mL 10 mol·L-1氨水+0.5 mL蒸馏水 | 溶液完全褪色所需时间:③<②<①。实验均产生棕褐色固体(经检验为MnO2),都伴有少量气泡产生(经检验为N2)。 |
| ② | 2 mL KMnO4溶液 + 1 mL 10 mol·L-1氨水 + 0.5 mL 1 mol·L-1稀硫酸 | |
| ③ | 2 mL KMnO4溶液 + 1 mL 10 mol·L-1氨水 + 0.5 mL 1 mol·L-1 Na2SO4溶液 | |
| ④ | 2 mL KMnO4溶液 + 1 mL 5 mol·L-1 (NH4)2SO4溶液 + 0.5 mL蒸馏水 | 无明显变化 |
下列说法
A.实验①中发生了反应2 MnO + 2NH3 = 2MnO2 + N2↑ + 2OH- + 2H2O + 2NH3 = 2MnO2 + N2↑ + 2OH- + 2H2O |
B.溶液完全褪色所需时间② < ①的主要原因:c(H+)增大,MnO 的氧化性增强 的氧化性增强 |
C.对比实验③④可得出,还原性:NH3 > NH |
| D.在实验④的试剂中,逐滴加入浓NaOH溶液,可观察到溶液褪色 |
您最近半年使用:0次
名校
9 . 氯化亚铜化学式为CuCl,白色立方结晶或白色粉末,难溶于水,在潮湿的空气中易氧化,不溶于乙醇,常用作催化剂、杀菌剂、媒染剂、脱色剂等。
I.CuCl的制备
取25g CuSO4∙5H2O和6.43gNaCl并加少量水溶解,将溶液倒入如图所示的三颈烧瓶中,加热至50℃,向三颈烧瓶中缓慢滴加Na2SO3和Na2CO3的混合溶液,使其持续反应30min。待反应结束后将混合物静置一段时间,抽滤,沉淀依次用36%的乙酸、无水乙醇、无水乙醚洗涤多次,得白色固体,真空或者充氮气保存。___________ 。
(2)反应时使用NaCl浓溶液,主要目的是___________ 。
(3)三颈烧瓶中CuSO4、NaCl、Na2SO3反应生成CuCl的离子方程式为___________ ;缓慢滴加Na2SO3和Na2CO3的混合溶液的主要原因是___________ 。
(4)沉淀用无水乙醇洗涤的目的是___________ 。
II.CuCl样品纯度的测定
准确称取CuCl样品0.25g,将其置于足量FeCl3溶液中,待固体完全溶解后,加水50mL和邻菲啰啉指示剂2滴,立即用amol∙L-1 Ce(SO4)2标准溶液滴定至绿色出现且30s不褪色,即为终点,重复2~3次,平均消耗Ce(SO4)2标准溶液bmL(已知: ,
, )
)
(5)滴定时应将Ce(SO4)2标准溶液加入___________ (填“酸式滴定管”或“碱式滴定管”)中;该样品中CuCl的质量分数为___________ ×100%。(用含a、b的代数式表示,列出计算式即可)
(6)下列操作可能会导致样品纯度测量结果偏低的是___________。(填标号)
I.CuCl的制备
取25g CuSO4∙5H2O和6.43gNaCl并加少量水溶解,将溶液倒入如图所示的三颈烧瓶中,加热至50℃,向三颈烧瓶中缓慢滴加Na2SO3和Na2CO3的混合溶液,使其持续反应30min。待反应结束后将混合物静置一段时间,抽滤,沉淀依次用36%的乙酸、无水乙醇、无水乙醚洗涤多次,得白色固体,真空或者充氮气保存。

(2)反应时使用NaCl浓溶液,主要目的是
(3)三颈烧瓶中CuSO4、NaCl、Na2SO3反应生成CuCl的离子方程式为
(4)沉淀用无水乙醇洗涤的目的是
II.CuCl样品纯度的测定
准确称取CuCl样品0.25g,将其置于足量FeCl3溶液中,待固体完全溶解后,加水50mL和邻菲啰啉指示剂2滴,立即用amol∙L-1 Ce(SO4)2标准溶液滴定至绿色出现且30s不褪色,即为终点,重复2~3次,平均消耗Ce(SO4)2标准溶液bmL(已知:
 ,
, )
)(5)滴定时应将Ce(SO4)2标准溶液加入
(6)下列操作可能会导致样品纯度测量结果偏低的是___________。(填标号)
| A.样品在空气中放置时间过长 |
| B.盛装Ce(SO4)2标准溶液的滴定管未用标准溶液润洗 |
| C.锥形瓶中装待测液前未干燥 |
| D.滴定管内部滴定前无气泡,滴定后有气泡 |
您最近半年使用:0次
昨日更新
|
250次组卷
|
3卷引用:山西省太原市2024届高三一模理综试卷-高中化学
山西省太原市2024届高三一模理综试卷-高中化学(已下线)题型9 实验综合题(25题)-2024年高考化学常考点必杀300题(新高考通用)河南省郑州市宇华实验学校2024届高三下学期第三次模拟考试化学试题
名校
解题方法
10 . 下列指定反应的离子方程式书写正确的是
| A.AlCl3溶液中加入过量氨水:Al3++3OH-=A1(OH)3↓ |
B.K3[Fe(CN)6]溶液滴入FeCl2溶液中: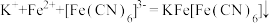 |
C.Cu与浓HNO3反应: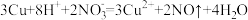 |
D.酸性KMnO4溶液滴定H2C2O4溶液: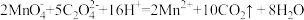 |
您最近半年使用:0次
昨日更新
|
184次组卷
|
2卷引用:安徽省合肥市第一中学2024届高三第一次教学质量检测化学试题